Clear Sky Science · de
Eine integrative klinische und bioinformatische Analyse identifiziert MicroRNAs als Biomarker für die Schwere eines ischämischen Schlaganfalls
Warum ein Bluttest für Schlaganfall wichtig ist
Bei einem Schlaganfall zählt jede Minute. Selbst mit modernen Hirnbildgebungen ist es jedoch nicht immer einfach, schnell einzuschätzen, wie schwer die Schädigung ist und wer das höchste Risiko für eine schlechte Erholung hat. Diese Studie untersucht, ob winzige Moleküle im Blut, sogenannte MicroRNAs, als schnelle, verlässliche Fingerabdrücke dessen dienen können, was im Gehirn während eines ischämischen Schlaganfalls vor sich geht. Gelingt das, könnte ein solcher Bluttest Ärzten helfen, Patienten besser zu triagieren, Behandlungsentscheidungen zu lenken und Angehörigen wahrscheinliche Verläufe besser zu erklären.
Kleine Botenstoffe im Blutkreislauf
MicroRNAs sind sehr kleine Stücke genetischen Materials, die mitsteuern, wie Gene an- und ausgeschaltet werden. Zellen des Körpers, darunter Blut- und Gehirnzellen, setzen MicroRNAs in den Blutkreislauf frei, wo sie überraschend stabil und gut messbar sind. Frühere Tier- und Humanstudien deuteten darauf hin, dass sich bestimmte MicroRNAs nach einem Schlaganfall verändern und die Schwere der Hirnschädigung widerspiegeln könnten. Die Autoren konzentrierten sich auf ein Panel von MicroRNAs, die bereits mit Herz‑ und Hirnerkrankungen in Verbindung gebracht wurden, insbesondere miR-16-5p und zwei eng verwandte Formen, miR-125a-3p und miR-125a-5p, um zu prüfen, ob deren Spiegel im Vollblut Schlaganfallpatienten von Hochrisikokontrollen unterscheiden und die Schlaganfallschwere widerspiegeln können.
Wie die Studie durchgeführt wurde
Das Forscherteam rekrutierte 60 Personen, die mit einem akuten ischämischen Schlaganfall aufgenommen wurden, und verglich sie mit 30 alters- und geschlechtsangepassten Personen mit kardiovaskulären Risikofaktoren, aber ohne Schlaganfall. Blutproben wurden kurz nach Klinikaufnahme und erneut sieben Tage später entnommen. Mit einer empfindlichen Labormethode, der quantitativen PCR, bestimmten die Wissenschaftler die Menge jeder ausgewählten MicroRNA im Blut. Anschließend verglichen sie die Spiegel zwischen den Gruppen und verfolgten deren Veränderung im Zeitverlauf. Zur Beurteilung der klinischen Schwere und des Verlaufs nutzten sie zwei in der Schlaganfallmedizin gebräuchliche Skalen: die NIH Stroke Scale, die das neurologische Defizit bewertet, und die modifizierte Rankin-Skala, die die Alltagsbehinderung einer Person misst.
Was die Blutwerte offenbarten
Die Studie zeigte klare Unterschiede in den MicroRNA-Mustern zwischen Schlaganfallpatienten und Kontrollen. MiR-125a-3p war bei Schlaganfallpatienten sowohl bei der Aufnahme als auch an Tag sieben durchgehend niedriger, während miR-125a-5p bei Aufnahme erhöht war, bis es bis Ende der ersten Woche wieder abfiel. Beide zeigten eine moderate Fähigkeit, Schlaganfallpatienten von Kontrollen zu unterscheiden, was auf diagnostisches Potenzial hindeutet. Das auffälligste Signal stammte jedoch von miR-16-5p. Patienten mit höheren miR-16-5p-Spiegeln bei Aufnahme hatten häufiger mäßige bis schwere neurologische Defizite und schlechtere funktionelle Ergebnisse einen Monat später. Selbst nach Adjustierung für Alter, Geschlecht, Entzündungswerte (gemessen als C‑reaktives Protein), Rauchen, Herzkrankheit und Thrombozytenzahl blieben hohe miR-16-5p-Spiegel und erhöhte C‑reaktive-Protein-Werte unabhängige Prädiktoren für ein ungünstiges frühes Outcome.
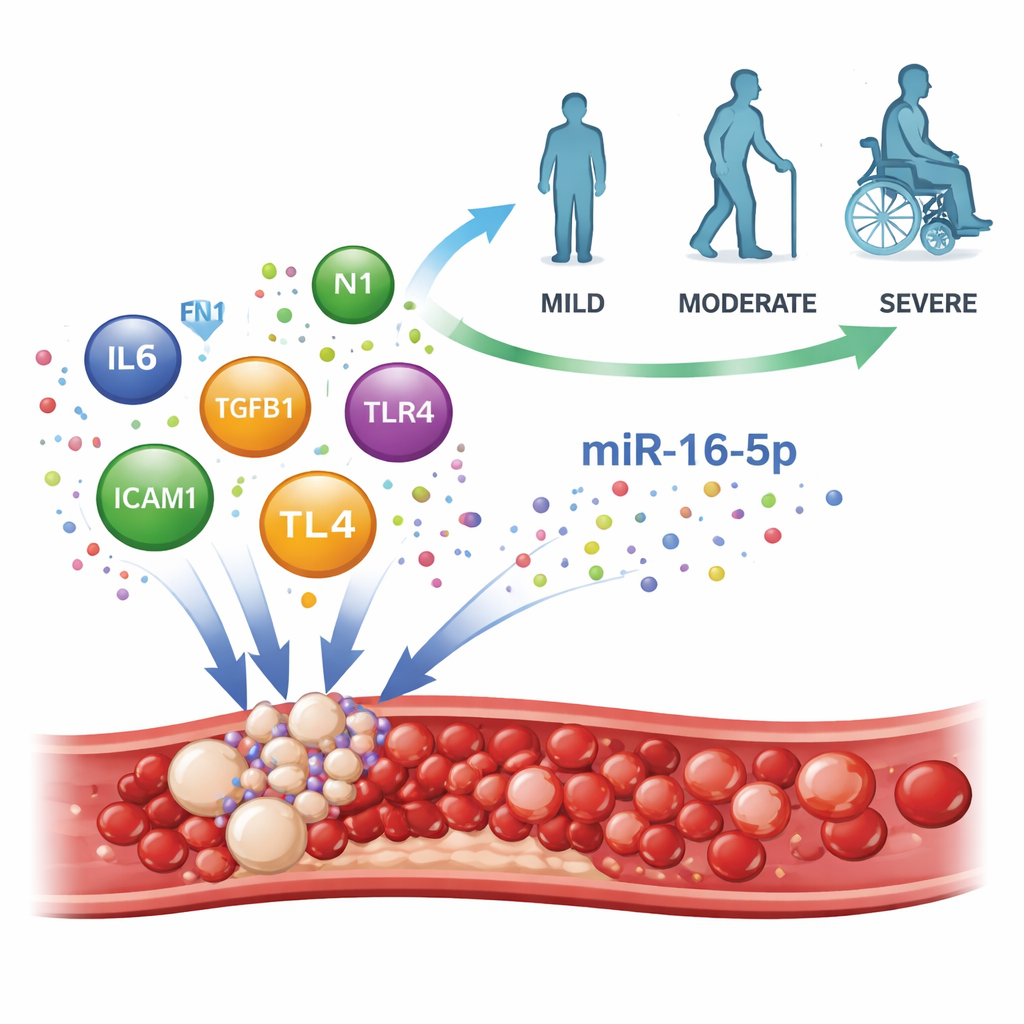
Hinweise zur zugrundeliegenden Biologie
Um zu verstehen, warum miR-16-5p die Schlaganfallschwere widerspiegeln könnte, nutzten die Autoren große biologische Datenbanken und Computermodelle, um zu kartieren, welche Gene und Signalwege von dieser MicroRNA beeinflusst werden können. Sie fanden heraus, dass die Ziele von miR-16-5p stark an Reaktionen auf Sauerstoffmangel, Blutgerinnung, Thrombozytenaktivierung und Entzündung beteiligt sind – Kernprozesse beim ischämischen Schlaganfall. Netzwerkanalysen hoben mehrere Schlüsselmoleküle hervor, darunter IL‑6, Fibronectin (FN1), TGF‑β1, ICAM‑1 und TLR4, die bekannt dafür sind, das Verhalten von Blutgefäßen, Thrombozyten und Immunzellen nach einem Schlaganfall zu prägen. Maschinelle Lernverfahren unterstrichen zusätzlich, dass hohe miR-16-5p-Spiegel zusammen mit Entzündungszeichen halfen, Patienten mit schwererer Behinderung zu klassifizieren, was die Idee stützt, dass diese MicroRNA an der Schnittstelle von Gerinnung und entzündlichem Schaden steht.
Was das für Patientinnen und Patienten bedeuten könnte
Für Nicht‑Spezialisten lautet die Quintessenz: Eine einfache Blutabnahme könnte eines Tages Ärzten helfen, über das Hirnbild hinauszublicken und den unsichtbaren molekularen Sturm eines Schlaganfalls sichtbar zu machen. In dieser Studie zeigten verschiedene MicroRNAs kurz nach einem ischämischen Schlaganfall unterschiedliche Muster, wobei miR-16-5p als Marker für größere frühe Hirnschädigung und schlechtere kurzfristige Ergebnisse hervorstach, während miR-125a-3p und miR-125a-5p beim Unterscheiden von Schlaganfall und Hochrisikokontrollen hilfreich waren. Diese Befunde stärken die Vorstellung, dass thrombozyten‑ und entzündungsbezogene MicroRNAs die biologischen Ereignisse widerspiegeln, die den Schlaganfallschaden antreiben. Die Autoren warnen jedoch, dass miR-16-5p nicht spezifisch für Schlaganfall ist und auch von Alter und anderen kardiovaskulären Erkrankungen beeinflusst wird. Größere, langfristige Studien sind erforderlich, bevor solche Tests den klinischen Alltag leiten können, doch diese Arbeit legt wichtige Grundlagen für blutbasierte Instrumente, die Diagnostik und Prognose beim Schlaganfall personalisieren könnten.
Zitation: Eyileten, C., Wicik, Z., Shahzadi, A. et al. An integrative clinical and bioinformatic analysis identifies MicroRNAs as biomarkers of ischemic stroke severity. Sci Rep 16, 6242 (2026). https://doi.org/10.1038/s41598-026-36494-2
Schlüsselwörter: ischämischer Schlaganfall, MicroRNA-Biomarker, Schwere des Schlaganfalls, Thrombozytenaktivierung, Entzündung