Clear Sky Science · de
NEK7-Phosphorylierung von Cortactin moduliert die Wanderfähigkeit von Zellen, die EML4-ALK V3 exprimieren
Warum Zellbewegung beim Lungenkrebs wichtig ist
Krebs wird lebensbedrohlich, wenn Zellen lernen, sich zu verbreiten. Beim nicht-kleinzelligen Lungenkrebs breiten sich manche Tumoren schneller im Körper aus als andere, und ein Schuldiger ist ein fehlerhaftes Fusionsprotein namens EML4-ALK. Eine besondere Variante, bekannt als Variante 3 (V3), steht in Verbindung mit besonders aggressiver Erkrankung und schlechteren Ansprechraten auf zielgerichtete Therapien. Diese Studie stellt eine einfache, aber entscheidende Frage: Was befähigt diese von V3 getriebenen Krebszellen dazu, ihre Form so effizient zu verändern und sich zu bewegen, und lassen sich die molekularen Komponenten identifizieren, die das ermöglichen?
Eine hochmigratorische Lungenkrebs-Variante
Ärzte wissen schon länger, dass nur ein Teil der Lungenkrebserkrankungen die EML4-ALK-Fusion trägt, aber Patienten mit Tumoren, die die V3-Form exprimieren, haben tendenziell eine schlechtere Prognose als Patienten mit anderen Varianten. Unter dem Mikroskop sehen V3-exprimierende Zellen anders aus: Statt kompakt und pflastersteinartig sind sie langgestreckt und dünn mit ausgeprägten Ausläufern, ähnlich wie wandernde Zellen. Frühere Arbeiten zeigten, dass dieses Verhalten von zwei Enzymen abhängt, NEK9 und NEK7, die als molekulare Schalter in Zellen fungieren. Die entscheidenden downstream-Ziele dieser Schalter — also diejenigen, die das innere Gerüst der Zelle direkt umgestalten — waren jedoch nicht gut verstanden.
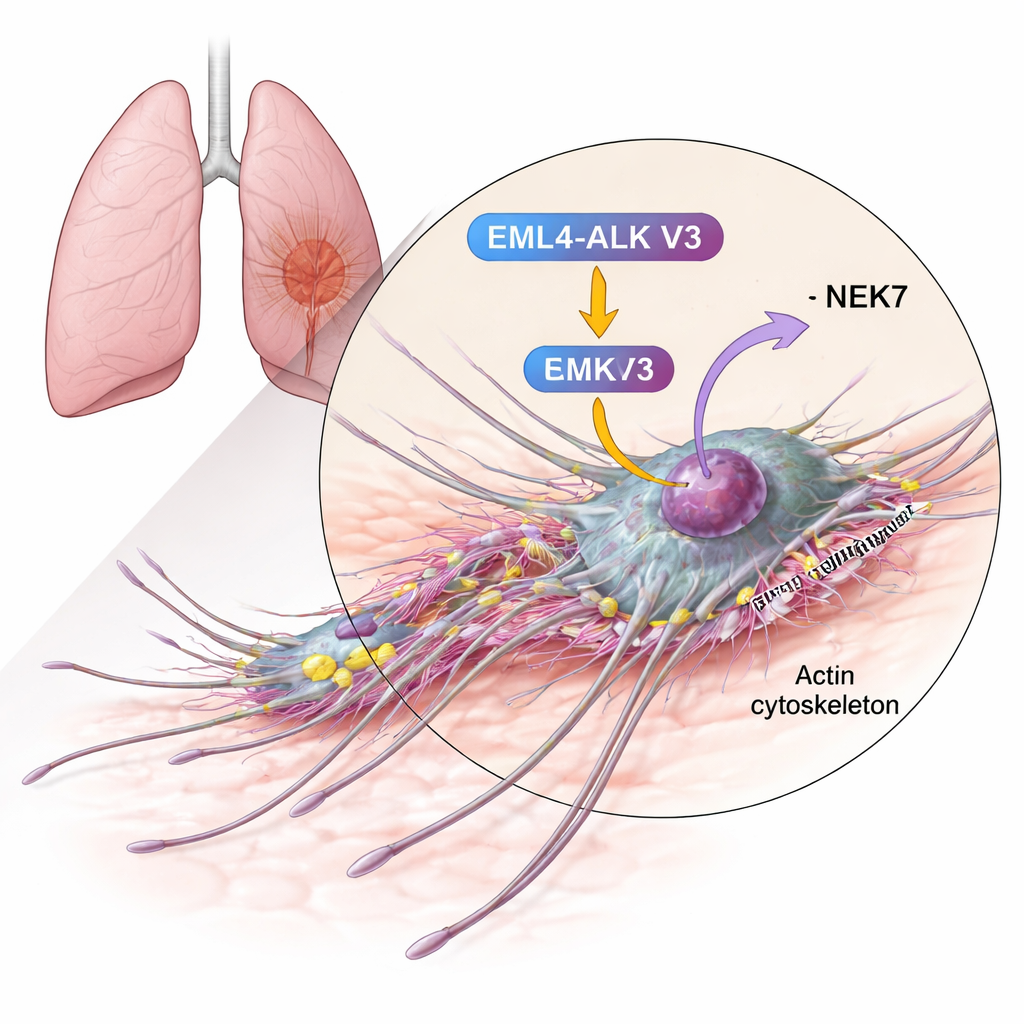
Verbindung eines Bewegungsproteins mit einer aggressiven Fusion
Die Autorinnen und Autoren konzentrierten sich auf Cortactin, ein Protein, das bereits dafür bekannt ist, in vielen invasiven Tumoren reichlich vorhanden zu sein und beim Aufbau der Aktinfilament-Netzwerke zu helfen, die die Zellmembran vorantreiben. Mit biochemischen Tests zeigten sie, dass Cortactin chemisch modifiziert (phosphoryliert) werden kann — durch NEK6 und noch stärker durch NEK7. Die Enzyme fügen Phosphatgruppen an spezifische Serinreste innerhalb der Aktinbindungsregion von Cortactin an — genau an der Stelle, die Aktinfasern greift und verzweigte Netzwerke stabilisiert. In Anwesenheit von NEK7 war Cortactin an mehr Stellen und stärker phosphoryliert als bei NEK6, was darauf hindeutet, dass NEK7 in diesem Kontext der Hauptregulator ist.
Cortactin ausschalten bremst die Krebszellmigration
Um zu prüfen, was Cortactin in lebenden Zellen tatsächlich bewirkt, entfernten die Forschenden das Protein mittels RNA-Interferenz in Zellen, die so konstruiert waren, dass NEK9 oder NEK7 aktiviert werden konnten, oder die EML4-ALK V3 selbst exprimierten. In allen drei Konstellationen brachen die auffälligen, langgestreckten, mesenchymal-ähnlichen Formen zusammen: Die Zellen wurden flacher und runder, verloren ihre langen Ausläufer und bildeten stattdessen dicke, gerade Aktin-„Stressfasern“, die die Zelle durchkreuzten. Mehrere Migrationsassays — vom Verschluss künstlicher „Wunden“ in einem Zellverband bis zur Verfolgung einzelner Zellen und der Messung der Bewegung zu einem chemischen Signal — zeigten, dass diese hoch mobilen Zellen ohne Cortactin deutlich langsamer wurden. Ähnliche Effekte zeigten etablierte Lungenkrebszelllinien, die natürlich EML4-ALK V3 tragen, was die klinische Relevanz dieses Signalwegs unterstreicht.
Feine Filamente und scharfe Spitzen an der Vorderkante
Hochauflösende Bildgebung in bronchialen Epithelzellen zeichnete ein noch detaillierteres Bild. EML4-ALK V3-exprimierende Zellen bildeten viele feine, manchmal verzweigte filopodienähnliche Fortsätze an ihren Ausläufern. An den Spitzen und Verzweigungspunkten dieser Strukturen sammelten sich Cortactin, EML4-ALK V3, NEK7 und eine phosphorylierte Form von Cortactin. Diese enge Kolisierung deutet auf eine fokussierte „Baustelle“ hin, an der NEK7 Cortactin modifiziert, um die feingliedrigen, verzweigten Aktinnetzwerke zu bauen und zu erhalten, die der Zelle die gerichtete Steuerung erlauben. Bei Entfernung von Cortactin verschwanden diese komplexen Fortsätze und das invasive Wachstum aus 3D-Tumorsphäroiden in ein umgebendes Gel wurde stark reduziert.
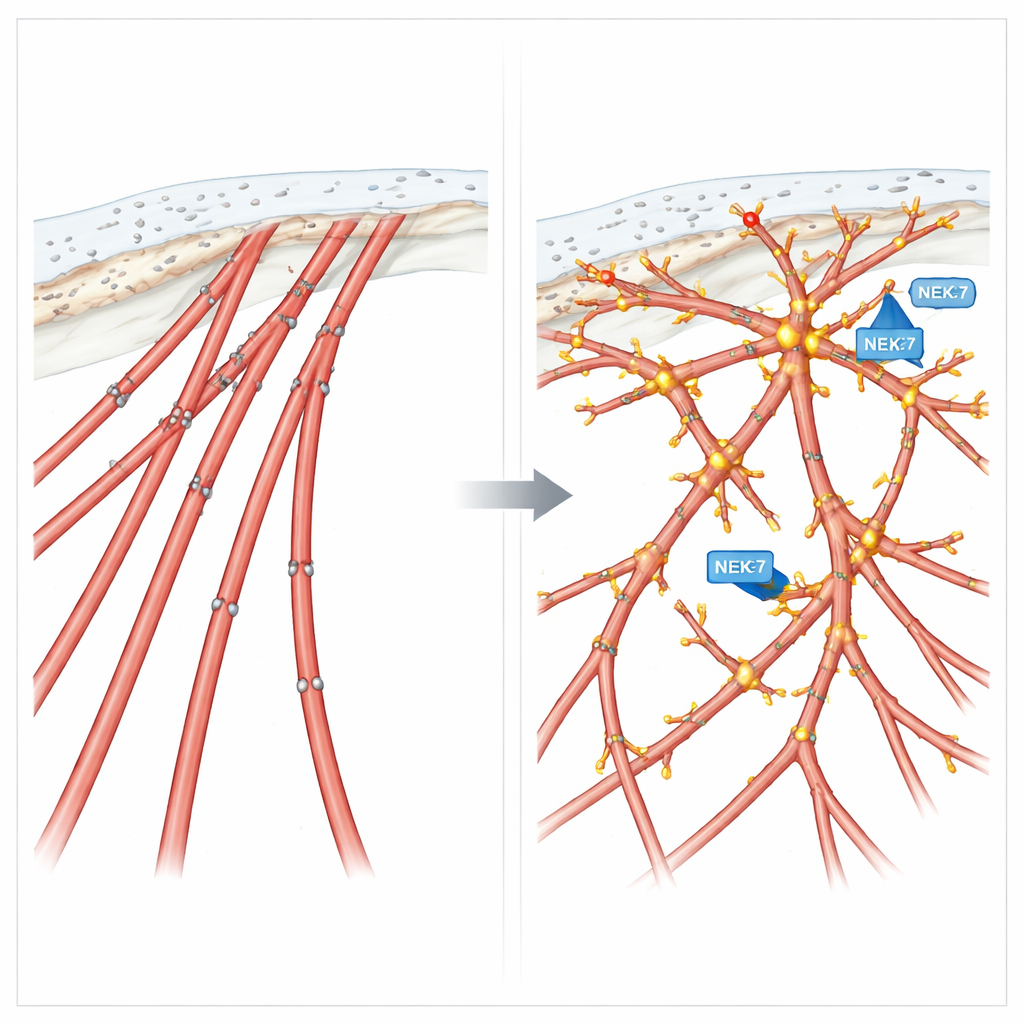
Phosphorylierung als Migrationsregler
Um zu testen, wie diese chemischen Markierungen auf Cortactin das Verhalten beeinflussen, erstellte das Team zwei Designer-Versionen des Proteins: eine Phospho‑Mimetikum‑Form, die eine konstante Phosphorylierung an vier Schlüsselstellen nachahmt, und eine Phospho‑Null‑Form, die dort nicht phosphoryliert werden kann. Zellen, die die mimetische Form exprimierten, entwickelten zahlreiche filopodienähnliche Ausläufer und zeigten verbesserte gerichtete Migration, ähnlich wie Zellen mit aktivem NEK7 oder EML4-ALK V3. Im Gegensatz dazu bildeten Zellen mit der nicht-phosphorylierbaren Form starre Stressfasern, verloren diese feinen Fortsätze und bewegten sich schnell, aber ziellos — gut beim Umherwandern, schlecht im Folgen eines Signals. In dreidimensionalen Kulturen trieb dieses phospho‑null Cortactin invasive Auswüchse voran, die unkoordiniert statt präzise gerichtet waren.
Was das für das Verständnis — und die Bekämpfung — der Ausbreitung bedeutet
Kurz gesagt zeigt die Studie, dass die aggressive EML4-ALK V3-Variante des Lungenkrebses ein normales formgebendes System der Zelle kapert. Durch Aktivierung von NEK7 bewirkt sie die Phosphorylierung von Cortactin an spezifischen Stellen innerhalb seiner Aktinbindungsregion. Diese Modifikation stellt Cortactin so ein, dass es fein verzweigte Aktinstrukturen und filopodienähnliche Ausläufer aufbauen kann, die schnelle, gerichtete Zellmigration und Invasion unterstützen. Die Störung von Cortactin oder seiner Phosphorylierung kehrt das System um: Zellen bewegen sich entweder kaum oder chaotisch ohne Richtung. Diese Erkenntnisse legen eine konkrete molekulare Kette offen — von einer krebsfördernden Fusion über NEK7 hin zu Cortactin und dem Aktin-Zytoskelett — die erklärt, warum manche Lungenkrebserkrankungen so effektiv metastasieren, und weisen auf neue Möglichkeiten hin, ihre Bewegung zu verlangsamen oder fehlzuleiten.
Zitation: Richardson, E.L., Knebel, A., Straatman, K.R. et al. NEK7 phosphorylation of cortactin modulates the migratory capacity of cells expressing EML4-ALK V3. Sci Rep 16, 6407 (2026). https://doi.org/10.1038/s41598-026-36484-4
Schlüsselwörter: nicht-kleinzelliges Lungenkarzinom, EML4-ALK V3, Zellmigration, Cortactin, Aktin-Zytoskelett