Clear Sky Science · de
Zusammenstellung des vollständigen Transkriptoms und Entwicklung von SSR-Markern für Spinibarbus hollandi mittels PacBio SMRT-Sequenzierung
Warum ein unscheinbarer Flussfisch wichtig ist
An den Flüssen Südchinas schwimmt Spinibarbus hollandi, ein karpfenähnlicher Fisch, der sowohl als Speisefisch als auch als Zierfisch geschätzt wird. Züchter möchten ihn effizienter halten, doch der Fisch wächst langsam, wird spät geschlechtsreif und produziert vergleichsweise wenige Eier. Die hier beschriebene Studie nutzt moderne DNA‑ und RNA‑Sequenzierungstechniken, um eine detaillierte genetische „Teileliste" für diese Art zu erstellen. Diese genetischen Informationen können langfristig Züchtern helfen, widerstandsfähigere, schneller wachsende Tiere auszuwählen und den Schutz wildlebender Bestände zu unterstützen.
Viele Gewebe zu einer genetischen Landkarte vereinen
Um möglichst viel genetische Information zu erfassen, entnahmen die Forschenden sechs verschiedene Gewebe — Herz, Kiemen, Gehirn, Flosse, Leber und Gonade — von jeweils sechs erwachsenen Männchen und Weibchen. Aus diesen Geweben gewannen sie RNA, das Molekül, das Kopien aktiver Gene innerhalb der Zellen trägt. Mit einer Technologie namens PacBio SMRT, die sehr lange RNA‑Kopien liest, stellten sie das erste vollständige Transkriptom von S. hollandi zusammen. Einfach ausgedrückt erstellten sie ein hochauflösendes Verzeichnis von 15.197 eindeutigen Genen und 23.403 Transkriptsequenzen, von denen die meisten deutlich länger und vollständiger sind als das, was ältere Kurzlese‑Methoden liefern konnten.
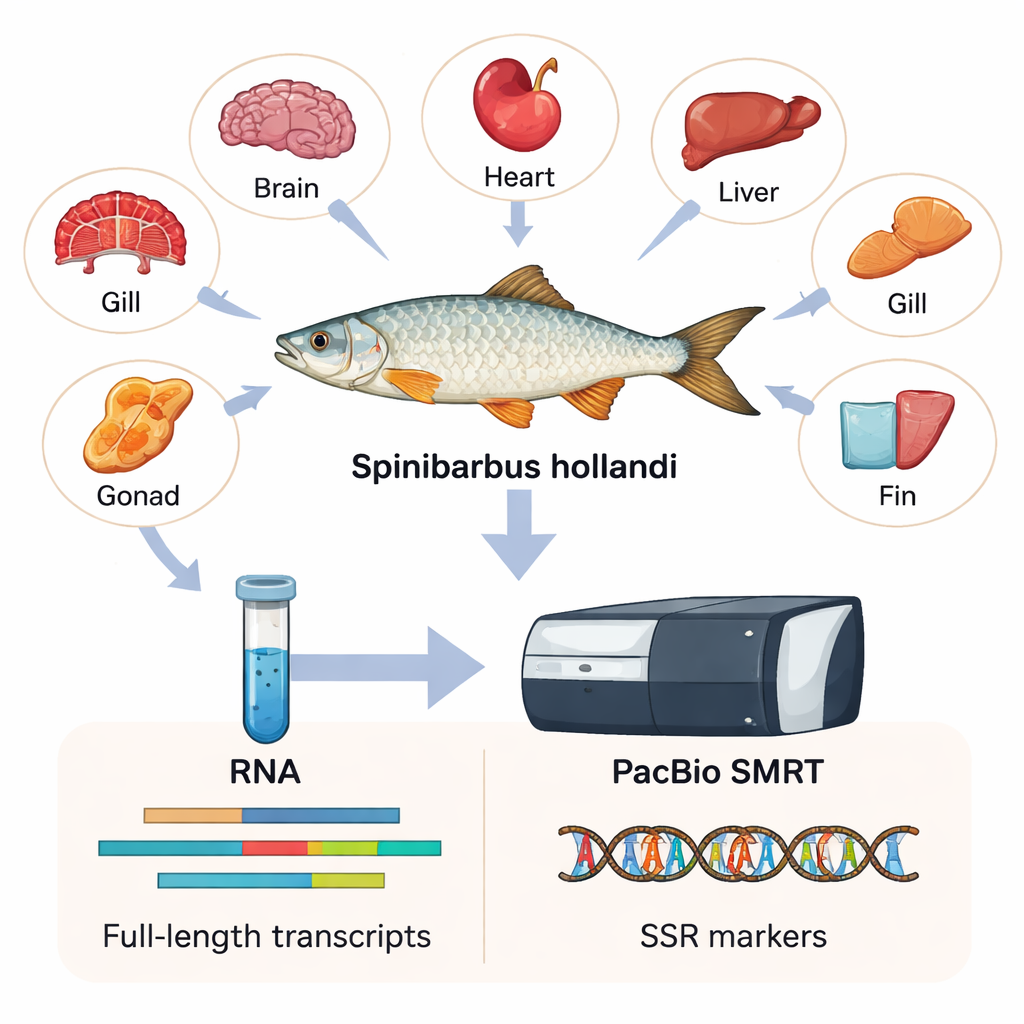
Was die Gene über den Fisch verraten
Im nächsten Schritt untersuchte das Team, welche Funktionen diese Gene haben. Sie verglichen jede Sequenz mit großen öffentlichen Datenbanken, die Gene nach Funktion gruppieren. Mehr als 95 % der Gene konnten bekannten Einträgen zugeordnet werden — eine sehr hohe Trefferquote, die auf eine gute Datenqualität hinweist. Viele Gene ordneten sich Kategorien zu, die mit grundlegenden zellulären Abläufen wie Stoffwechsel, Signalübertragung und Entwicklung zusammenhängen, und ähnelten am stärksten Genen anderer Karpfenverwandter. Das bestätigt, dass das neue Transkriptom biologisch stimmig ist und die Grundlage dafür bildet, Gene zu finden, die mit Merkmalen wie Wachstumsrate, Stressresistenz und Fortpflanzung bei S. hollandi verknüpft sind.
Verborgene Kontrollebenen in der RNA
Über die Identifizierung von Genen hinaus betrachteten die Wissenschaftler:innen auch deren Kontrollmechanismen. Sie fanden 373 Fälle alternativen Spleißens, bei dem dasselbe Gen unterschiedlich zusammengesetzt wird und so verschiedene RNA‑Botschaften entstehen. Das häufigste Muster behielt RNA‑Abschnitte bei, die in anderen Arten oft entfernt werden, was auf eine besondere Art der Feinabstimmung von Proteinen in diesem Fisch hindeutet. Außerdem entdeckten sie 2.397 lange nichtkodierende RNAs — RNA‑Moleküle, die keine Proteine produzieren, aber regulieren können, wann und wo andere Gene aktiviert werden. Zusammen zeigen diese Befunde, dass S. hollandi über ein reiches Set an RNA‑vermittelten Kontrollmechanismen verfügt, die Wachstum, Geschlechtsreife und Anpassung an lokale Lebensräume beeinflussen könnten.
DNA‑Marken für Zucht und Schutz erstellen
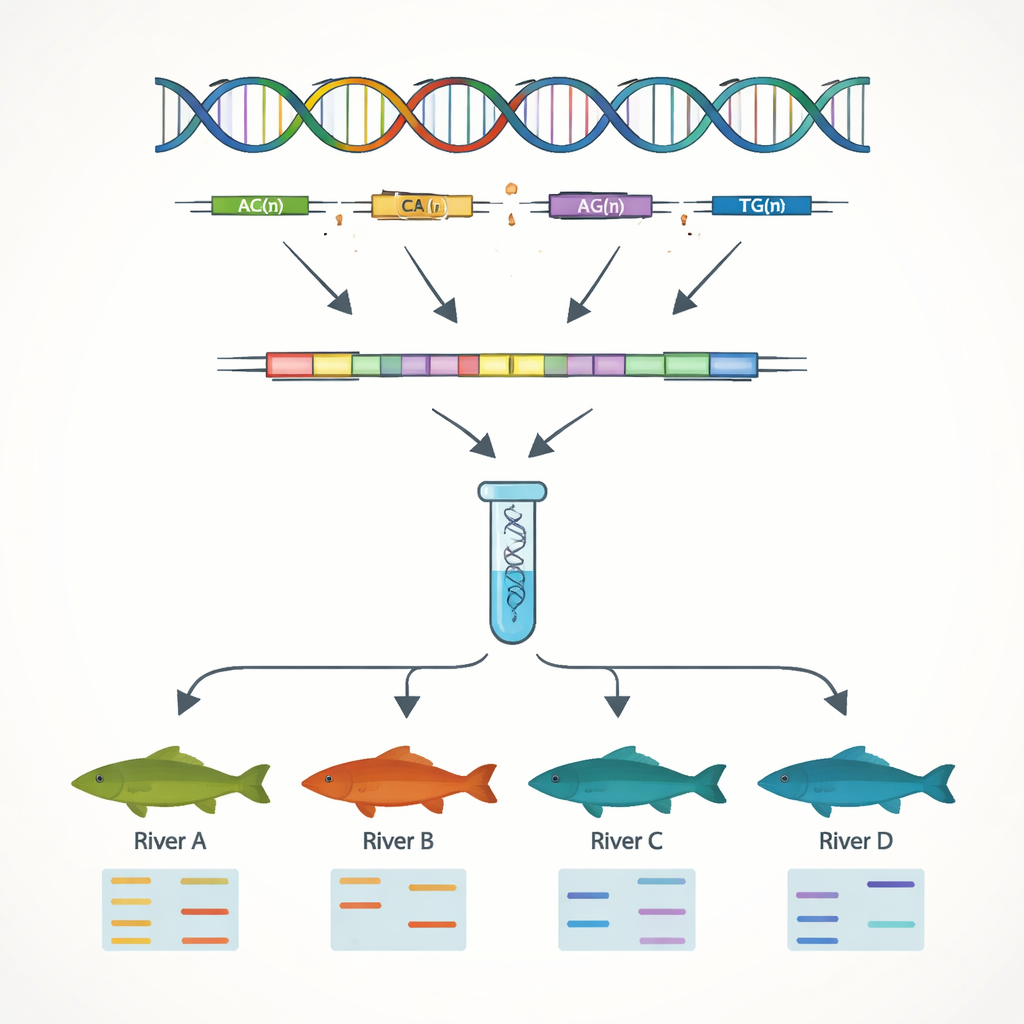
Ein zentrales Ziel der Arbeit war die Entwicklung einfacher DNA‑Marker, mit denen sich Individuen und Populationen unterscheiden lassen. Ausgehend von den Genfolgen suchten die Autor:innen nach einfachen Sequenzwiederholungen, sogenannten SSRs — kurzen DNA‑Motiven wie „AC“ oder „AAT“, die mehrfach hintereinander vorkommen. Diese Abschnitte variieren oft zwischen Individuen und eignen sich daher als genetische Barcodes. Sie identifizierten 7.449 solche SSR‑Stellen und entwarfen Dutzende kurzer DNA‑Primer, um sie im Labor zu amplifizieren. Dreizehn dieser Marker erwiesen sich bei Tests an 51 Fischen aus vier Flusssystemen als hochvariabel und zuverlässig. Mit nur diesen 13 Markern konnte das Team genetische Unterschiede zwischen Populationen des Jangtse und solchen des Perlflusses klar erkennen — ein Spiegelbild der Gebirgszüge, die den natürlichen Austausch zwischen den Einzugsgebieten begrenzen.
Was das für Züchter und Flussökosysteme bedeutet
Für Nicht‑Spezialisten ist die Kernaussage, dass die Autor:innen eine detaillierte, hochwertige genetische Referenz für S. hollandi und ein praktisches Set an DNA‑Markern geschaffen haben. Dieses Werkzeugset wird Forschenden helfen, Gene zu identifizieren, die für langsames Wachstum oder geringe Fruchtbarkeit verantwortlich sind, Züchtern ermöglichen, Brutfische mit erwünschten Eigenschaften auszuwählen, und Naturschützer:innen erlauben, die genetische Vielfalt in verschiedenen Flusssystemen zu überwachen. Zwar sind weitere Studien nötig, um einzelne Gene mit Leistungen in Teichen oder in der Wildnis zu verknüpfen, doch diese Arbeit legt das molekulare Fundament dafür, einen traditionellen Flussfisch in eine moderne, nachhaltig bewirtschaftete Aquakulturart zu überführen.
Zitation: Li, S., Lai, J., Wu, M. et al. Full-Length transcriptome assembly and SSR marker development for Spinibarbus hollandi using PacBio SMRT sequencing. Sci Rep 16, 5629 (2026). https://doi.org/10.1038/s41598-026-36468-4
Schlüsselwörter: Spinibarbus hollandi, Fisch-Transkriptom, PacBio-Sequenzierung, Mikrosatellitenmarker, Aquakulturgenetik