Clear Sky Science · de
Ein integrativer Ansatz zur Identifizierung neuartiger miRNA-mRNA-Interaktionsnetzwerke bei LMNA-Kardiomyopathie
Warum winzige Herzregulatoren wichtig sind
Die dilatative Kardiomyopathie ist eine schwere Erkrankung, bei der das Herz vergrößert und geschwächt wird und die häufig zu Herzinsuffizienz, gefährlichen Herzrhythmusstörungen und sogar plötzlichem Tod führt. Bei vielen Familien ist die Krankheit erblich, und Veränderungen in einem Gen namens LMNA sind ein häufiger Auslöser. Die Studie stellt eine scheinbar einfache, aber weitreichende Frage: Welche Gene werden in durch LMNA-Mutationen geschädigten Herzen ein- oder ausgeschaltet, und welche kleinen RNA-Moleküle betätigen diese Schalter? Indem diese molekularen Gespräche im Detail kartiert werden, weist die Arbeit auf neue Möglichkeiten hin, diese aggressive Form der Herzerkrankung besser vorherzusagen, zu überwachen und vielleicht eines Tages zu behandeln.
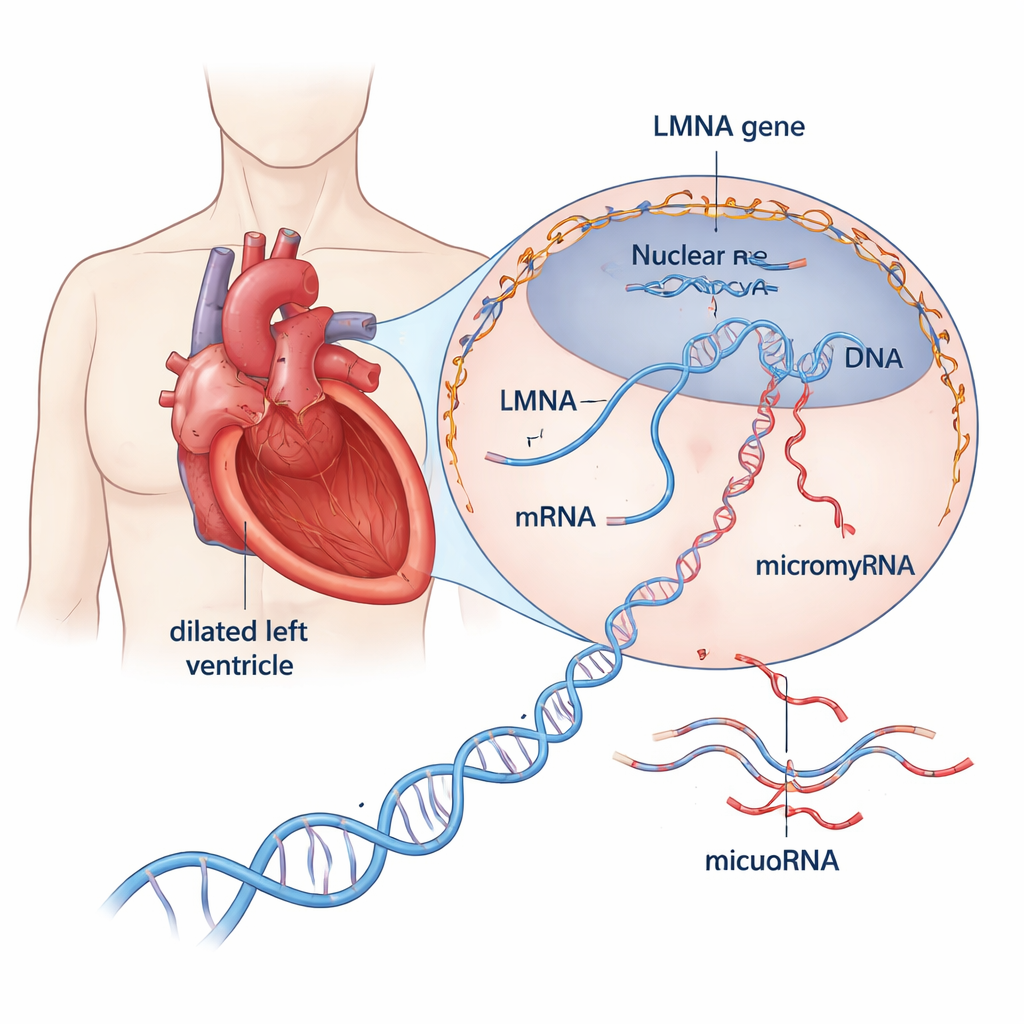
Ein genauerer Blick auf eine gefährliche Herzerkrankung
Die dilatative Kardiomyopathie dehnt und verdünnt die Hauptpumpe des Herzens und schwächt dadurch seine Fähigkeit, Blut durch den Körper zu pressen. Etwa ein Drittel bis die Hälfte der früher als „idiopathisch“ bezeichneten Fälle hat inzwischen eine genetische Ursache. Von den mehr als 30 beteiligten Genen sticht LMNA hervor: Schädliche Varianten in diesem Gen machen etwa 10 % der erblichen Fälle aus und sind mit raschem Krankheitsfortschritt, früh auftretenden Rhythmusstörungen und einem hohen Risiko für plötzlichen Herztod verbunden. LMNA kodiert für Strukturproteine, die ein Gerüst um die DNA der Zelle bilden, zur Aufrechterhaltung der Zellkernform beitragen und beeinflussen, welche Gene aktiv sind. Doch wie fehlerhafte LMNA-Proteine das Herz in Richtung Versagen treiben, blieb weitgehend unklar.
Den Botschaften in Mäuseherzen folgen
Um dies zu untersuchen, verwendeten die Forscher ein Maismodell mit einer bekannten LMNA-Mutation (R249W), das eine Form der dilatativen Kardiomyopathie entwickelt, die der menschlichen Erkrankung ähnelt. Im Alter von 50 Wochen—wenn die Mäuse vergrößerte Ventrikel, reduzierte Pumpfunktion und fibrotische Narbenbildung zeigen—entnahmen die Forscher Herzgewebe und untersuchten zwei Arten von RNA: messenger-RNA (mRNA), die Anweisungen zur Proteinherstellung trägt, und microRNA (miRNA), kurze nicht-kodierende Stränge, die die Genaktivität feinregulieren, indem sie bestimmte mRNAs blockieren oder abbauen. Mithilfe von Hochdurchsatz-Sequenzierung und strengen statistischen Filtern identifizierten sie 2.148 Gene, deren Aktivität in den mutierten Herzen verändert war, sowie 53 miRNAs, die im Vergleich zu gesunden Mäusen entweder erhöht oder vermindert waren.
Was sich in kranken Herz-Zellen verändert
Als die Forscher die veränderten Gene in biologische Signalwege gruppierten, zeigten sich mehrere zentrale Themen. Viele der veränderten Gene standen im Zusammenhang mit der Kontraktion von Herzmuskelzellen, ihrer Haftung untereinander und an die umgebende Stützmatrix, der Weiterleitung elektrischer Signale im Herzen sowie der Verarbeitung von Fetten zur Energiegewinnung. Diese Befunde passen gut zum klinischen Bild der LMNA-assoziierten Erkrankung: steifes, fibrotisches Gewebe; gestörte elektrische Leitung, die Arrhythmien begünstigt; und gestörter Energiehaushalt. Weganalysen mit etablierten Datenbanken bestätigten eine Anreicherung bei Umbau der extrazellulären Matrix, spannungsabhängigen Ionenkanälen, synapsenähnlicher Kommunikation im Herzen und dem Fettsäurestoffwechsel—was darauf hindeutet, dass die LMNA-Mutation mehrere miteinander verbundene Systeme stört und nicht nur einen einzelnen fehlerhaften Schritt.
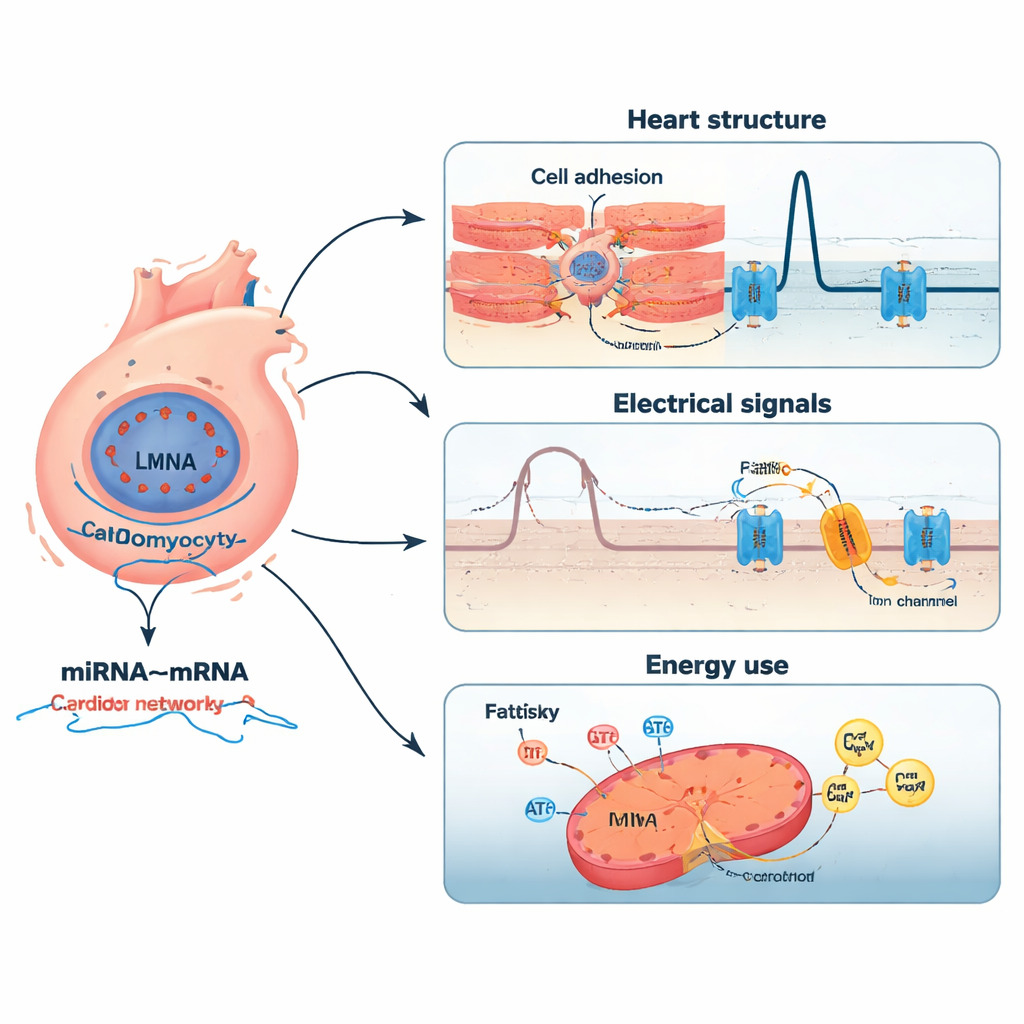
Netzwerke winziger Schalter und ihrer Ziele
Die Studie ging weiter und koppelte miRNAs mit ihren wahrscheinlichen mRNA-Zielsequenzen. Mithilfe von Korrelationsanalysen und Abgleich mit großen Datenbanken experimentell validierter Interaktionen stellten die Autoren ein Netzwerk mit hoher Zuverlässigkeit aus 2.197 miRNA–mRNA-Paaren zusammen, die 12 Schlüssel-miRNAs einbezogen. Einige miRNAs waren stärker aktiv und schienen Gene zu dämpfen, die für Herzentwicklung, Kalziumhandling und Reaktionen auf oxidativen Stress wichtig sind. Andere waren weniger aktiv und könnten Bremsen für Gene lösen, die an Zelladhäsion, Entzündung und Umbau des strukturellen Gerüsts des Herzens beteiligt sind. Zum Beispiel wurde eine miRNA (miR-183-5p) mit einem Rezeptor der Wnt-Signalgebung verknüpft, welche die Zell-zu-Zell-Kommunikation beeinflusst, während eine andere (miR-3473a) mit einem Kalziumfreisetzungskanal verbunden war, der zentral für den Herzrhythmus ist. Zusammen skizzieren diese Netzwerke, wie subtile Verschiebungen in winzigen RNA-Regulatoren die Auswirkungen einer LMNA-Mutation verstärken können.
Von molekularen Karten zu künftigen Therapien
Für Nicht-Spezialisten ist die Kernaussage, dass diese Studie eine detaillierte Karte liefert, wie eine LMNA-Mutation die interne Verdrahtung des Herzens auf Ebene der Genkontrolle umgestaltet. Statt eines einzelnen „schlechten Gens“ spiegelt die Erkrankung eine Kaskade veränderter Botschaften wider—viele orchestriert von miRNAs—die Herzstruktur, elektrische Stabilität und Energieverbrauch beeinflussen. Zwar wurden die Arbeiten an Mäusen durchgeführt und stützen sich stark auf rechnerische Analysen, dennoch hebt die Studie spezifische miRNA–Gen-Paare als vielversprechende Kandidaten für künftige blutbasierte Biomarker oder gezielte Therapien hervor. Langfristig könnte das Feintuning dieser winzigen RNA-Schalter Ärzten helfen, besser vorherzusagen, wer das höchste Risiko trägt, den Krankheitsverlauf präziser zu überwachen und individuellere Behandlungen für Familien mit LMNA-assoziierter Kardiomyopathie zu entwickeln.
Zitation: Córdoba-Caballero, J., Martínez, F.B., Campuzano, O. et al. An integrative approach to identify novel miRNA-mRNA interaction networks in LMNA-cardiomyopathy. Sci Rep 16, 6110 (2026). https://doi.org/10.1038/s41598-026-36439-9
Schlüsselwörter: dilatative Kardiomyopathie, LMNA-Gen, microRNA, Genregulation, Herzinsuffizienz