Clear Sky Science · de
Datenschutzorientierte Segmentierung der tiefen Venenthrombose mittels eines Multi‑Modell‑Federated‑Learning‑Rahmens mit dem Federated‑Averaging‑Algorithmus
Warum Blutgerinnsel und Datenschutz wichtig sind
Blutgerinnsel, die tief in den Venen der Beine entstehen und als tiefe Venenthrombose (TVT) bezeichnet werden, können still in die Lungen wandern und lebensbedrohliche Notfälle auslösen. CT‑Scans können diese Gerinnsel sichtbar machen, doch Tausende von Graustufenbildern in verlässliche automatische Erkennungen zu verwandeln, ist für Computer eine anspruchsvolle Aufgabe. Gleichzeitig sind Krankenhäuser zu Recht zurückhaltend beim Austausch sensibler Patientendaten. Diese Studie untersucht, wie mehrere Kliniken zusammenarbeiten können, um ein leistungsfähiges, Gerinnsel‑erkennendes System der künstlichen Intelligenz (KI) zu trainieren—ohne jemals ihre rohen Patientenscans zusammenzuführen oder offenzulegen.
Gehirne teilen, nicht Körper
Kernstück der Arbeit ist eine Technik namens federiertes Lernen, die mehreren Institutionen erlaubt, KI‑Modelle kollaborativ zu trainieren, während ihre Daten vor Ort bleiben. Anstatt CT‑Bilder an einen zentralen Server zu senden, trainiert jedes Krankenhaus sein eigenes lokales Modell an seinen eigenen Scans. Nur die gelernten Modellparameter—im Wesentlichen das, was das Modell über das Erkennen von Gerinnseln «herausgefunden» hat—werden an einen zentralen Server geschickt. Dort kombiniert ein Verfahren namens Federated Averaging diese unterschiedlichen Parametersätze zu einem einzigen, verbesserten globalen Modell, das anschließend an alle Kliniken zurückgesendet wird. Auf diese Weise profitiert jeder Standort von der kollektiven Erfahrung aller Teilnehmer, während kein Patientenbild jemals seine Heimatinstitution verlässt. 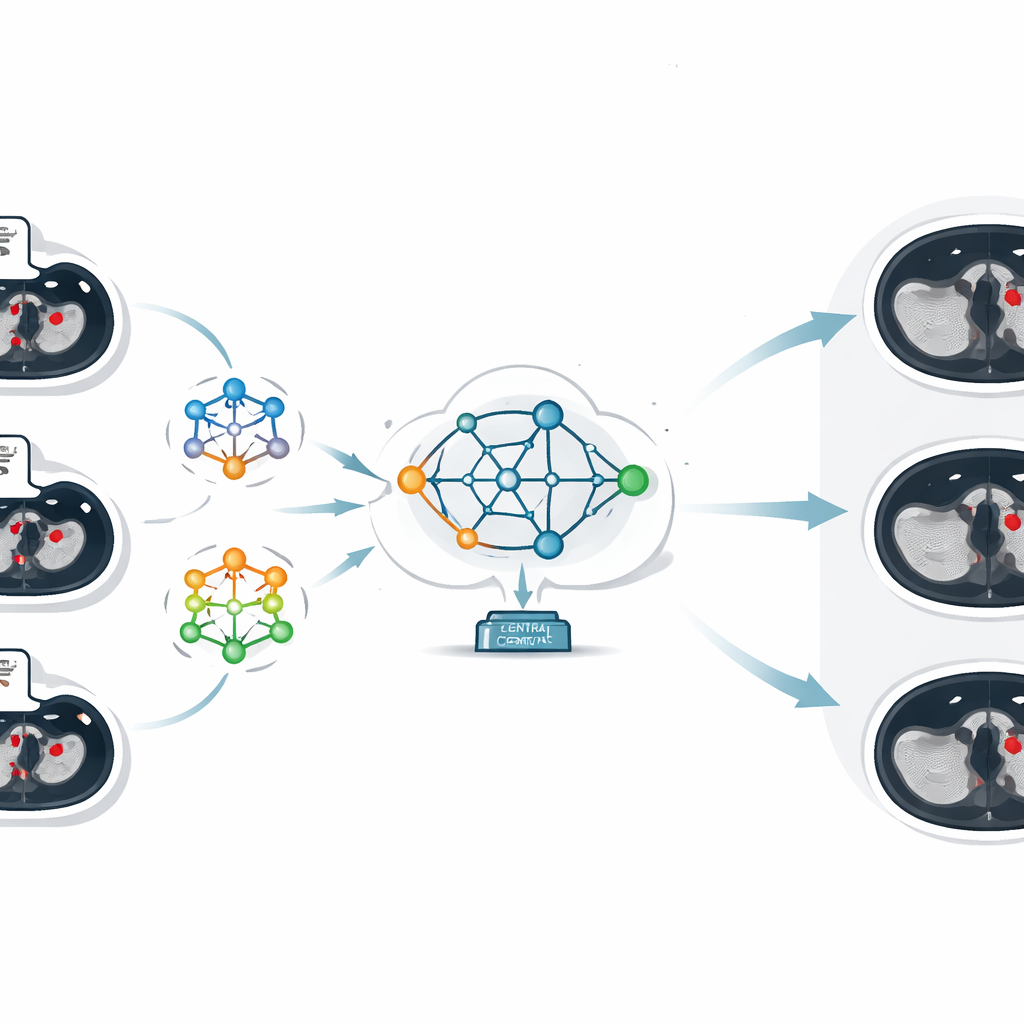
Viele KI‑Typen blicken auf dieselben Venen
Eine zentrale Neuerung dieser Studie ist, dass die Forschenden sich nicht auf nur einen Typ neuronaler Netze stützten. Sie setzten sieben verschiedene Modell‑Entwürfe ein, von denen jeder unterschiedliche Aspekte der CT‑Bilder besonders gut erfasst. Einfachere Modelle, wie grundlegende Faltungsnetzwerke und sequentielle Modelle, sind schneller und leichter auf begrenzter Hardware einsetzbar. Fortgeschrittenere Architekturen, darunter U‑Net, VGG‑19 und zwei angepasste Netze mit Residual‑, Inception‑, Attention‑ und Multi‑Scale‑Verarbeitungsblöcken, sind besser darin, feine Gefäßgrenzen nachzuzeichnen, kleine Gerinnsel zu entdecken und mit verrauschten Bildern umzugehen. Indem jedes Krankenhaus das Modell nutzen kann, das am besten zu seinen Daten und zur verfügbaren Rechenleistung passt, spiegelt das System die unordentliche Realität klinischer Umgebungen wider, anstatt anzunehmen, dass jeder Standort gleich ist.
Aus ungleichmäßigen und unvollkommenen Daten lernen
In der Medizin sieht ein Datensatz eines Krankenhauses selten genau so aus wie der eines anderen. Scanner, Bildgebungsprotokolle und Patientengruppen unterscheiden sich, daher arbeitete die Studie bewusst mit sogenannten „non‑IID“-Daten—Sammlungen, die ungleichmäßig und nicht identisch verteilt sind. Das führt gewöhnlich zu instabilerem Training. Die Autoren nahmen diese Vielfalt hier an und zeigten, dass das Zusammenführen von Wissen über mehrere unterschiedlich strukturierte Modelle die Generalisierungsfähigkeit des globalen Systems tatsächlich verbesserte. Sie führten drei Versuchsphasen durch: zunächst mit drei, dann fünf und schließlich sieben Clients und verwendeten Datensätze mit 1.000, 2.000 bzw. 3.000 CT‑Bildern. In jedem Schritt verfolgten sie nicht nur, wie häufig das globale Modell Gerinnsel korrekt segmentierte, sondern auch, wie viel Kommunikation nötig war, wie lange das Training dauerte, wie unterschiedlich die Daten der einzelnen Clients waren und wie gut die Datenschutzmaßnahmen funktionierten.
Bessere Gerinnsel‑Erkennung zu einem Rechenpreis
Über alle Phasen hinweg übertraf das kombinierte globale Modell konstant jedes einzelne lokale Modell. Mit wachsender Bildzahl und dem Beitritt leistungsfähigerer Modelle zur Föderation stieg die Segmentierungsgenauigkeit von etwa 91 % auf über 96 %, und eine ausgeglichene Qualitätskennzahl, der F1‑Score, kletterte von ungefähr 0,89 auf 0,95. Gleichzeitig sank eine fehlerfokussierte Verlustgröße um mehr als die Hälfte, was auf sauberere, verlässlichere Gerinnselkonturen hinweist. Diese Verbesserungen kamen nicht ohne Kosten: die Kommunikation zwischen Clients und Server wuchs von einigen Dutzend Megabyte auf mehrere Gigabyte, und die durchschnittliche Trainingszeit stieg von Sekunden auf viele Stunden, während die Architekturen komplexer wurden. Nichtsdestotrotz hielt das System eine starke formale Datenschutzgarantie aufrecht, die darauf hinweist, dass die geteilten Updates nur sehr wenige Informationen über einzelne Patienten preisgeben.
Was das für Patienten und Krankenhäuser bedeutet
Für Laien lautet die Quintessenz: Diese Arbeit zeigt, wie Krankenhäuser gemeinsam eine KI trainieren können, die gefährliche Blutgerinnsel genauer erkennt, ohne die Kontrolle über ihre sensiblen Daten aufzugeben. Durch die Kombination mehrerer komplementärer Modellentwürfe und das sorgfältige Aggregieren dessen, was jedes Modell lernt, bauen die Autoren ein Gerinnsel‑Segmentierungssystem, das sowohl leistungsfähig als auch datenschutzfreundlich ist. Obwohl der Ansatz erhebliche Rechenressourcen und Netzwerkkapazität erfordert, weist er auf eine Zukunft hin, in der medizinische Zentren routinemäßig bei der Entwicklung besserer Diagnosetools zusammenarbeiten—zur Verbesserung der Versorgung von Patienten mit TVT‑Risiko und verwandten Erkrankungen, während ihre persönlichen Scans sicher hinter institutionellen Schutzmauern bleiben.
Zitation: B, P.L., S, V. Privacy-aware deep vein thrombosis segmentation using a multi-model federated learning framework with the federated averaging algorithm. Sci Rep 16, 11333 (2026). https://doi.org/10.1038/s41598-026-36432-2
Schlüsselwörter: tiefe Venenthrombose, federiertes Lernen, Segmentierung medizinischer Bilder, datenschutzfreundliche KI, CT‑Bildgebung