Clear Sky Science · de
Antitumorale Aktivität von QAL333 und prädiktives Modellieren: Integrierte transkriptomisch-bioinformatische Analyse zeigt selektive Zytotoxizität und Sensitivitätsdeterminanten
Warum dieser neue Wirkstoffkandidat wichtig ist
Krebsmedikamente wirken bei manchen Patientinnen und Patienten gut, bei anderen hingegen nicht – größtenteils weil Tumoren in ihrer inneren Verschaltung unterschiedlich sind. Diese Studie stellt eine neu entworfene Verbindung vor, QAL333, die offenbar einige kolorektale Tumoren deutlich stärker trifft als andere, während viele normale Zellen verschont bleiben. Ebenso wichtig: Die Forschenden zeigen, wie Muster der Genaktivität in Tumorzellen helfen könnten vorherzusagen, wer am ehesten profitieren wird, und deuten damit auf präzisere, individualisierte Behandlungsstrategien hin.
Ein gezielter Schlag gegen bestimmte Tumortypen
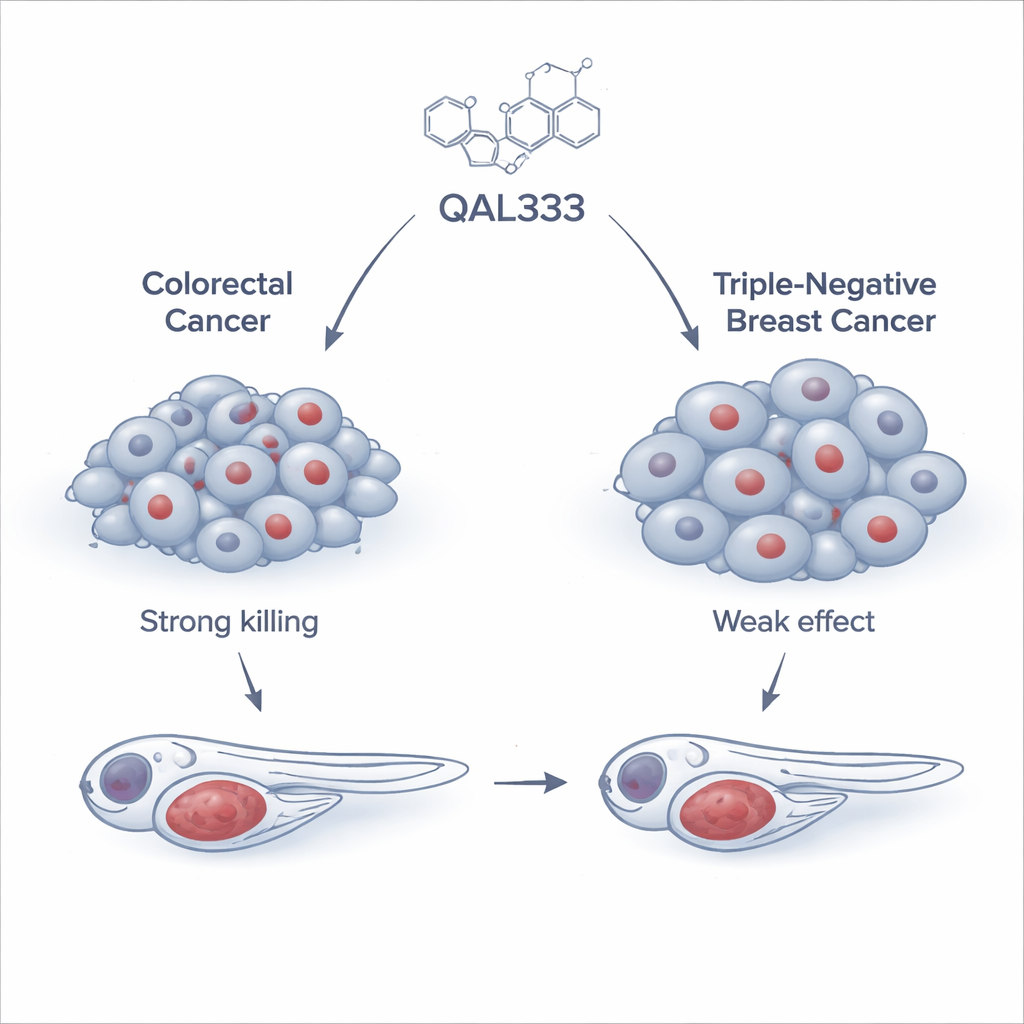
Das Team begann damit, QAL333 — ein synthetisches Molekül, verwandt mit einer Stoffklasse, die bereits dafür bekannt ist, Krebszellen zu schädigen — an einem breiten Panel von 15 menschlichen Krebszelllinien und drei nicht-kanzerösen Linien zu testen. Sie fanden, dass kolorektale Krebszellen, insbesondere eine Linie namens SW620, hochsensitiv waren; das Medikament tötete sie bei relativ niedrigen Dosen. Im Gegensatz dazu waren triple-negativen Brustkrebszellen weitaus resistenter und benötigten Dosen, die mehr als zehnmal höher lagen und schwer sicher zu erreichen wären. Interessanterweise reagierten nicht alle nicht-kanzerösen Zellen gleich: Einige waren empfindlich, andere, wie eine häufig verwendete Nierenzelllinie, zeigten überraschende Resistenz. Dieses Muster zeigte, dass die Wirkung von QAL333 stärker von der inneren Biologie einer Zelle abhängt als davon, ob sie als „Krebs“ oder „normal“ bezeichnet wird.
Test des Medikaments in lebenden Organismen
Um zu prüfen, ob die vielversprechenden Ergebnisse aus Zellkulturen sich auch in einem lebenden Organismus bestätigen, verwendeten die Forschenden Zebrafische, kleine transparente Fische, die häufig als Modell für menschliche Erkrankungen dienen. Sie setzten fluoreszenzmarkierte menschliche Krebszellen in Zebrafischembryonen und behandelten diese mit QAL333. Bei Fischen mit kolorektalen Krebszellen verlangsamte das Medikament deutlich das Tumorwachstum und kam dabei an die Wirkung einer klinisch verwendeten Standardchemotherapie heran. Im Gegensatz dazu sprachen Tumoren aus den triple-negativen Brustkrebszellen kaum an, obwohl ein übliches Brustkrebsmedikament, Paclitaxel, im selben Modell gut wirkte. Diese In-vivo-Tests untermauerten, dass die Stärke von QAL333 in einer Untergruppe von Tumoren liegt und nicht universell gegen alle Krebsarten wirkt.
Blick ins Zellinnere: Wie QAL333 wirkt
Um zu verstehen, warum manche Zellen absterben und andere resistent sind, ermittelten die Wissenschaftler, wie sich Tausende von Genen in ihrer Aktivität veränderten nach der QAL333-Behandlung. In sensitiven kolorektalen Krebszellen wurden Schlüssengene, die den Zellteilungszyklus und das Wachstum antreiben, herunterreguliert, und wichtige Überlebenswege wurden gedämpft. Signale, die mit oxidativem Stress und einer Form des Zelltods zusammenhängen, die sich von klassischem programmiertem Zelltod unterscheidet, waren ebenfalls verändert, was darauf hindeutet, dass QAL333 bereits fragile Systeme, die Schäden in diesen Zellen managen, überlastet. Resistente Brustkrebszellen dagegen schalteten Stress- und Entzündungsprogramme an, gesteuert von Faktoren wie NF-κB, die bekannt dafür sind, Zellen beim Umgang mit schädlichen Bedingungen zu helfen. Dieser direkte Vergleich zeichnete das Bild, dass QAL333 in einigen Zellen schwache Abwehrmechanismen überwältigt, während andere eine wirksame Gegenreaktion aufbauen.
Mit Genmustern vorhersagen, wer anspricht
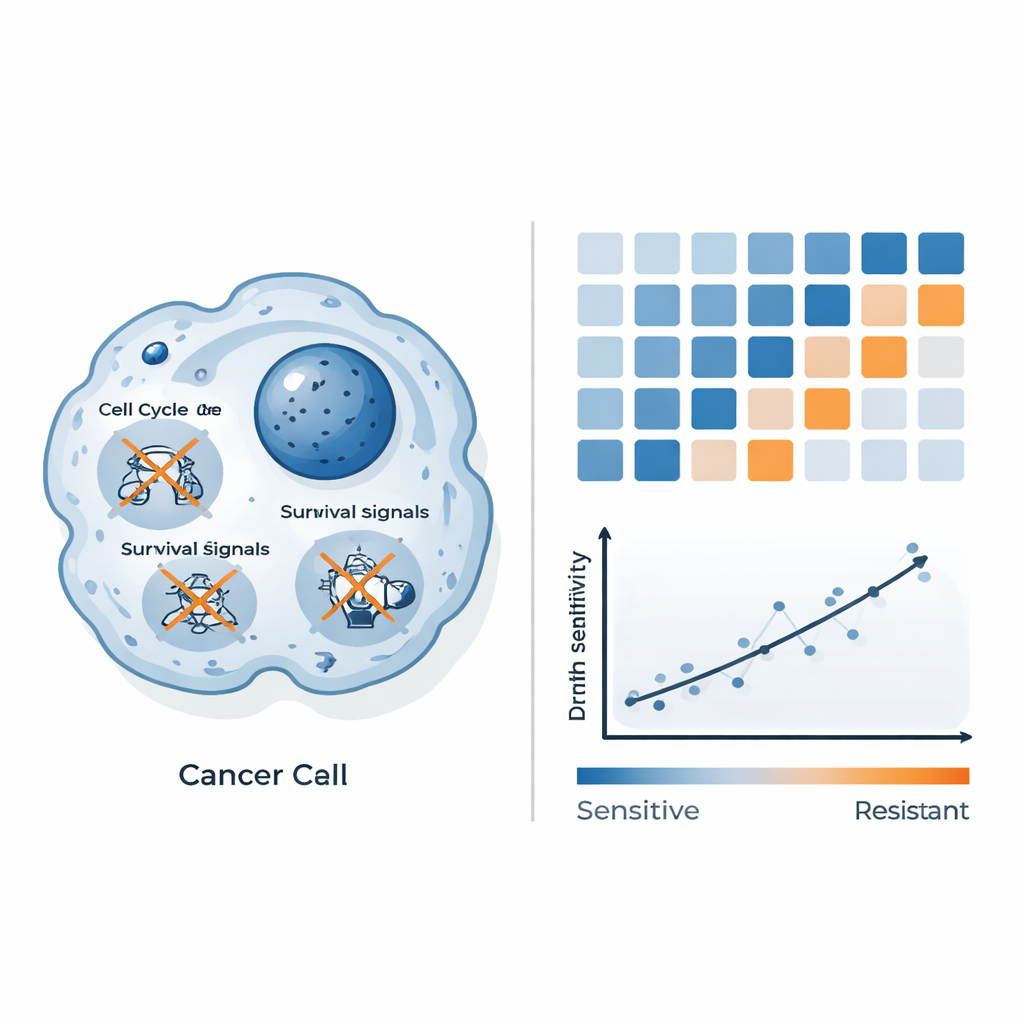
Über das reine Auflisten von Genveränderungen hinaus fragten die Forschenden, ob sich diese Muster in ein praktisches Vorhersagewerkzeug umsetzen lassen. Sie kombinierten Ausgangs-Gendaten des Zelllinienpanels mit den gemessenen Medikamentensensitivitäten und setzten maschinelles Lernen ein, um die aussagekräftigsten Signale zu finden. Statt sich auf einzelne Gene zu stützen, gruppierten sie Gene in biologische Signalwege und erstellten einen kombinierten „Pathway-Score“, aufgebaut aus drei Systemen: wie Zellen Energie und Stoffe verarbeiten (metabolische Wege), wie sie ihre Umgebung organisieren (Proteoglykane und verwandte Strukturen im Krebs) und wie ihr inneres Skelett angeordnet ist. Dieser zusammengesetzte Score korrelierte stark mit der benötigten Menge QAL333: Niedrigere Scores gingen mit höherer Sensitivität einher, höhere Scores mit Resistenz. Mit anderen Worten: Die Abstimmung dieser Netzwerke in einem Tumor kann vorhersagen, wie gut QAL333 wirken wird.
Unerwartete Hinweise auf breitere biologische Effekte
Während der Schwerpunkt auf Krebs lag, zeigte QAL333 auch die Fähigkeit, die sogenannte Quorum-Sensing-Kommunikation zu stören, ein System, das Bakterien nutzen, um Verhalten wie Biofilmbildung zu koordinieren. In sehr niedrigen Dosen reduzierte die Verbindung die Biofilmbildung durch einen Zahnfleischerkrankungs-Erreger und dämpfte bestimmte Entzündungssignale in Immunzellen. Die Autorinnen und Autoren werten dies als frühe, explorative Befunde, doch sie deuten an, dass QAL333 oder verwandte Moleküle eines Tages Anwendungen jenseits der Krebstherapie haben könnten, etwa bei Infektionen, in denen bakterielle Gemeinschaften schwer zu beseitigen sind.
Was das für künftige Patientinnen und Patienten bedeuten könnte
Insgesamt positioniert die Studie QAL333 als selektiven Wirkstoffkandidaten, der verwundbare kolorektale Tumoren trifft und viele andere Zelltypen verschont, und verbindet dies mit einer Roadmap zur Vorhersage, welche Tumoren am ehesten ansprechen. Wenn sich diese Ergebnisse in weiter fortgeschrittenen Tiermodellen und schließlich in klinischen Studien bestätigen, könnte ein einfacher Genexpressions-Test Ärzten helfen zu entscheiden, wann QAL333 eine passende Wahl ist – im Sinne des übergeordneten Ziels, Krebstherapien an die individuelle Tumorverschaltung anzupassen. Gleichzeitig unterstreicht die Arbeit, dass selbst vielversprechende Medikamente Grenzen haben: Brustkrebserkrankungen und andere resistente Tumoren könnten intelligente Kombinationen oder völlig andere Strategien erfordern.
Zitation: Kim, H.H., Im, S., Kim, J. et al. QAL333’s antitumor activity and predictive modeling: integrated transcriptomic-bioinformatic analysis reveals selective cytotoxicity and sensitivity determinants. Sci Rep 16, 5648 (2026). https://doi.org/10.1038/s41598-026-36430-4
Schlüsselwörter: kolorektales Karzinom, zielgerichtete Therapie, Genexpression, Modellierung der Arzneimittelempfindlichkeit, Zebrafisch-Xenograft