Clear Sky Science · de
Pseudolaricinsäure B fördert Ferroptose von Lungenkrebszellen abhängig von JNK/ERK-vermittelter Hochregulierung von Survivin
Pflanzenwirkstoff zielt auf Lungen-Tumoren
Lungenkrebs bleibt eine der tödlichsten Krebsarten weltweit, und viele Patientinnen und Patienten sprechen nicht auf moderne Arzneien an oder leiden an schweren Nebenwirkungen. Diese Studie untersucht einen natürlichen Stoff namens Pseudolaricinsäure B, der aus der Rinde eines traditionellen chinesischen Heilbaums gewonnen wird, um zu prüfen, ob er gezielt Lungenkrebszellen töten kann, während gesundes Lungengewebe verschont bleibt. Die Forschenden decken einen unerwarteten Mechanismus auf, mit dem diese Verbindung Tumorzellen zerstört: sie löst eine spezielle Form des Zelltods aus, die von Eisen und Lipid‑Schäden innerhalb der Zellen abhängt.
Warum ein Molekül aus Baumrinde wichtig ist
Ärztinnen und Ärzte brauchen dringend neue Therapien, die medikamentenresistente Tumoren besiegen, ohne normale Zellen zu schädigen. Pflanzenbasierte Arzneien haben bereits wichtige Krebsmedikamente wie Paclitaxel und Vincristin hervorgebracht. Pseudolaricinsäure B zeigte in mehreren Tumortypen antitumorale Effekte, doch ihre Wirkweise bei Lungenkrebs war bislang unklar und teilweise widersprüchlich. Hier testeten die Wissenschaftler Pseudolaricinsäure B an menschlichen Lungenkrebszellen und normalen Bronchialzellen im Labor und anschließend in Mäusen mit menschlichen Lungen-Tumoren, um genau nachzuzeichnen, wie dieser Naturstoff wirkt.
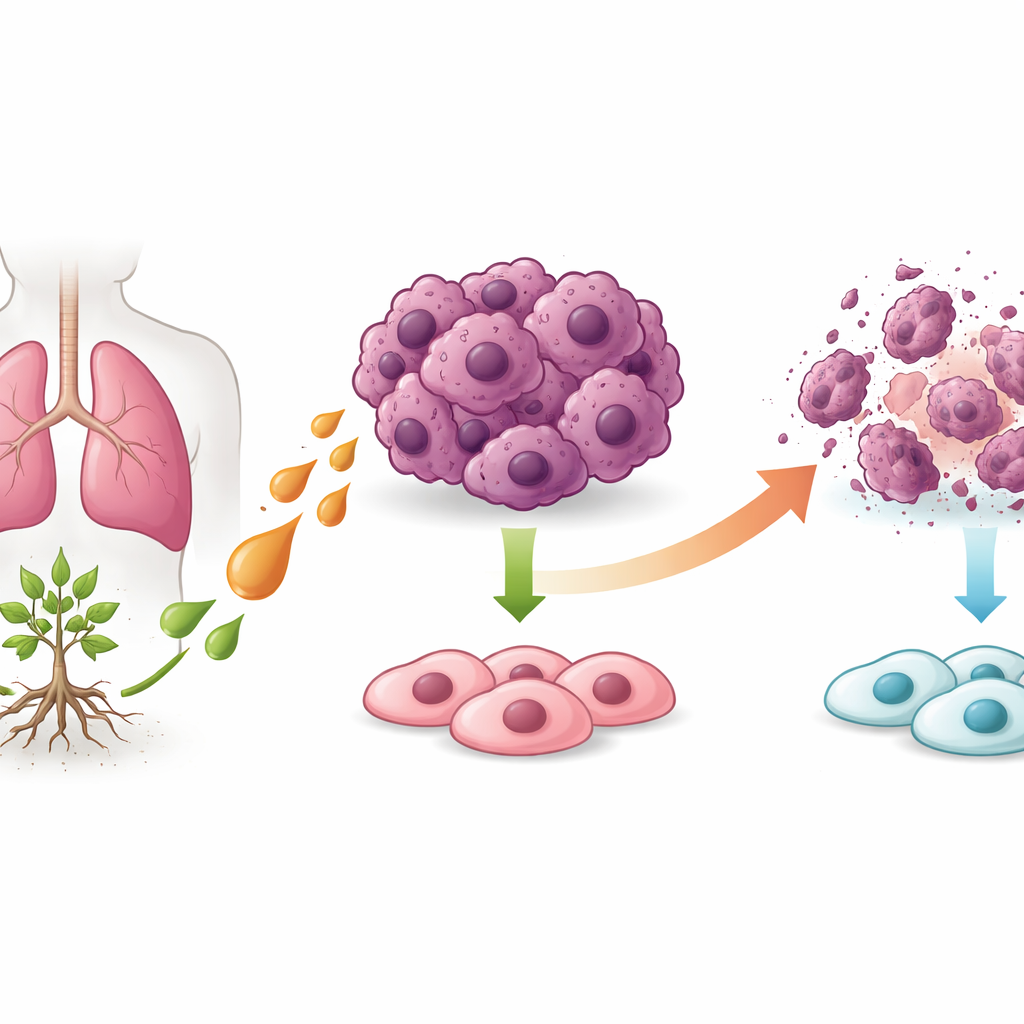
Selektiver Angriff auf Krebszellen
In Zellkulturen verlangsamte Pseudolaricinsäure B deutlich das Wachstum zweier verschiedener Lungenkrebszelllinien, hatte jedoch kaum Einfluss auf normale Bronchialzellen. Die behandelten Krebszellen hörten auf, sich zu vermehren, verloren ihre Fähigkeit, dichte Kolonien zu bilden, und zeigten eindeutige Schädigungszeichen. Interessanterweise spielte die klassische Form des Zelltods, die Apoptose, nur eine untergeordnete Rolle: Das Blockieren wichtiger Apoptose-Enzyme oder das Abschalten des Autophagie‑Recyclings rettete die Zellen nicht. Gleichzeitig waren Proteine, die als „Inhibitoren der Apoptose“ bekannt sind und Krebszellen normalerweise beim Überleben helfen, stark reduziert, was darauf hindeutet, dass das Mittel die Zellen in einen anderen Todesweg drängt.
Eisengetriebener Zelltod im Tumor
Durch die Analyse der Genaktivität über das gesamte Genom stellte das Team fest, dass viele der betroffenen Gene auf Ferroptose hinwiesen, eine regulierte Form des Zelltods, die durch Eisen und den Abbau von Membranlipiden angetrieben wird. Ein Blick in die Zellen offenbarte die typischen Merkmale der Ferroptose: geschrumpfte, geschädigte Mitochondrien; hohe Spiegel reaktiver Sauerstoffspezies; vermehrtes zweiwertiges Eisen; und stärker oxidierte Lipide in den Zellmembranen. Schützende Schlüsselproteine, die normalerweise gegen Ferroptose schützen, wie SLC7A11 und GPX4, waren sowohl auf Protein‑ als auch auf RNA‑Ebene reduziert. Als die Forschenden ein eisenbindendes Medikament zusetzten, das Ferroptose blockiert, wurden Zelltod, Eisenanreicherung und Lipid‑Schäden stark zurückgedreht, was bestätigt, dass Pseudolaricinsäure B Lungenkrebszellen hauptsächlich über Ferroptose tötet.
Eine unerwartete Hilfe: Survivin und Zellsignale
Überraschend war das Verhalten eines Proteins namens Survivin, das zur Familie der Inhibitoren der Apoptose gehört. Während die meisten dieser Überlebensproteine durch die Behandlung gesenkt wurden, stiegen die Survivin‑Spiegel auf Proteinebene deutlich an, obwohl sich seine RNA‑Menge nicht änderte. Als die Wissenschaftler Survivin mit einem kleinen Molekülinhibitor oder mittels Gen‑Silencing blockierten, verlor Pseudolaricinsäure B einen Großteil seiner Wirksamkeit: Lungenkrebszellen überlebten besser, Eisen‑ und Lipid‑Schäden nahmen ab, und die schützenden Ferroptose‑Proteine kehrten zurück. Weitere Signalwegsanalysen zeigten, dass zwei intrazelluläre Signalkaskaden, bekannt als JNK und ERK, nach der Behandlung stärker aktiv wurden. Die Hemmung dieser Signale reduzierte die Ferroptose, stellte die Überlebensproteine wieder her und senkte Survivin‑Level, was zeigt, dass Pseudolaricinsäure B Ferroptose über eine JNK/ERK–Survivin‑Achse auslöst.
Von der Schale in lebende Tumoren
Um zu prüfen, ob diese Effekte auch in einem lebenden Organismus gelten, setzten die Forschenden menschliche Lungenkrebszellen in Mäuse ein, um kleine Tumoren wachsen zu lassen. Eine tägliche Behandlung mit Pseudolaricinsäure B verlangsamte das Tumorwachstum signifikant, ohne offensichtlichen Gewichtsverlust oder andere Anzeichen von Toxizität. Tumorproben aus behandelten Tieren zeigten hohe Werte eines Lipidschadensmarkers, vermehrtes Survivin und weniger teilende Zellen — alles im Einklang mit andauernder Ferroptose und verminderter Tumorvitalität. Diese in vivo‑Befunde stimmten mit den Laborergebnissen überein und stützten die Idee, dass der Pflanzenstoff Tumorwachstum durch das Fördern eisenabhängigen Zelltods eindämmen kann.
Was das für künftige Therapien bedeutet
Insgesamt zeigt die Studie, dass Pseudolaricinsäure B Lungenkrebszellen selektiv töten kann, indem sie diese in die Ferroptose treibt — eine durch Eisen und Membranschäden angetriebene Form des Zelltods — anstatt vorwiegend auf klassische Apoptose zu setzen. Dieser Effekt hängt von einer Signalkette mit JNK‑ und ERK‑Proteinen und einem unerwarteten Anstieg des Überlebensproteins Survivin ab, das in diesem Kontext entscheidend für das Fortschreiten der Ferroptose wird. Zwar ist noch viel Arbeit nötig, bevor dieser Stoff am Menschen erprobt werden kann, doch deuten die Befunde darauf hin, dass das gezielte Nutzen von Ferroptose, möglicherweise mit pflanzlichen Wirkstoffen, neue Wege zur Behandlung hartnäckiger Lungenkrebserkrankungen eröffnen könnte.
Zitation: Li, Y., Yu, C., Yang, S. et al. Pseudolaric acid B promotes lung cancer cells ferroptosis depending on JNK/ERK-mediated upregulation of survivin. Sci Rep 16, 8294 (2026). https://doi.org/10.1038/s41598-026-36423-3
Schlüsselwörter: Lungenkrebs, Pseudolaricinsäure B, Ferroptose, Survivin, MAPK-Signalisierung