Clear Sky Science · de
Von in-silico-QSAR-Modellierung bis in-vitro-MTT-Assay: experimentelle Validierung neuartiger uPAR-Kandidaten für triple-negativen Brustkrebs (TNBC) und Hautkrebs
Warum diese Forschung wichtig ist
Krebsarten wie der triple‑negative Brustkrebs und bestimmte Hautkrebse sind besonders schwer zu behandeln, weil sie sich schnell ausbreiten und häufig gegen Standardtherapien resistent sind. In dieser Studie wird ein vielversprechendes neues Zielmolekül an der Zelloberfläche von Krebszellen untersucht – uPAR – und gezeigt, wie die Kombination aus computerbasiertem Wirkstoffdesign und Laborversuchen neue Wirkstoffkandidaten aufspüren kann, die das Wachstum oder die Ausbreitung dieser aggressiven Tumoren verlangsamen oder stoppen könnten.
Eine Tür, die dem Krebs beim Streuen hilft
Damit ein Tumor lebensgefährlich wird, müssen seine Zellen sich vom Ursprungsort lösen, das umliegende Gewebe durchdringen, in den Blutkreislauf gelangen und entfernte Organe besiedeln. uPAR spielt in diesem Prozess eine zentrale Rolle. Es sitzt auf der Zelloberfläche von Krebszellen und arbeitet mit Partnerproteinen zusammen, um Enzyme zu aktivieren, die die stützende Umgebung auflösen, sodass Zellen sich leichter bewegen und eindringen können. uPAR kommt insbesondere in Zellen des triple‑negativen Brustkrebses und in bestimmten Hautkrebszellen in hohen Mengen vor; seine Häufigkeit korreliert mit schnellerem Wachstum, höherer Invasivität und ungünstigerer Prognose. Deshalb ist uPAR ein attraktives – wenn auch bislang wenig genutztes – Ziel für Krebsmedikamente.
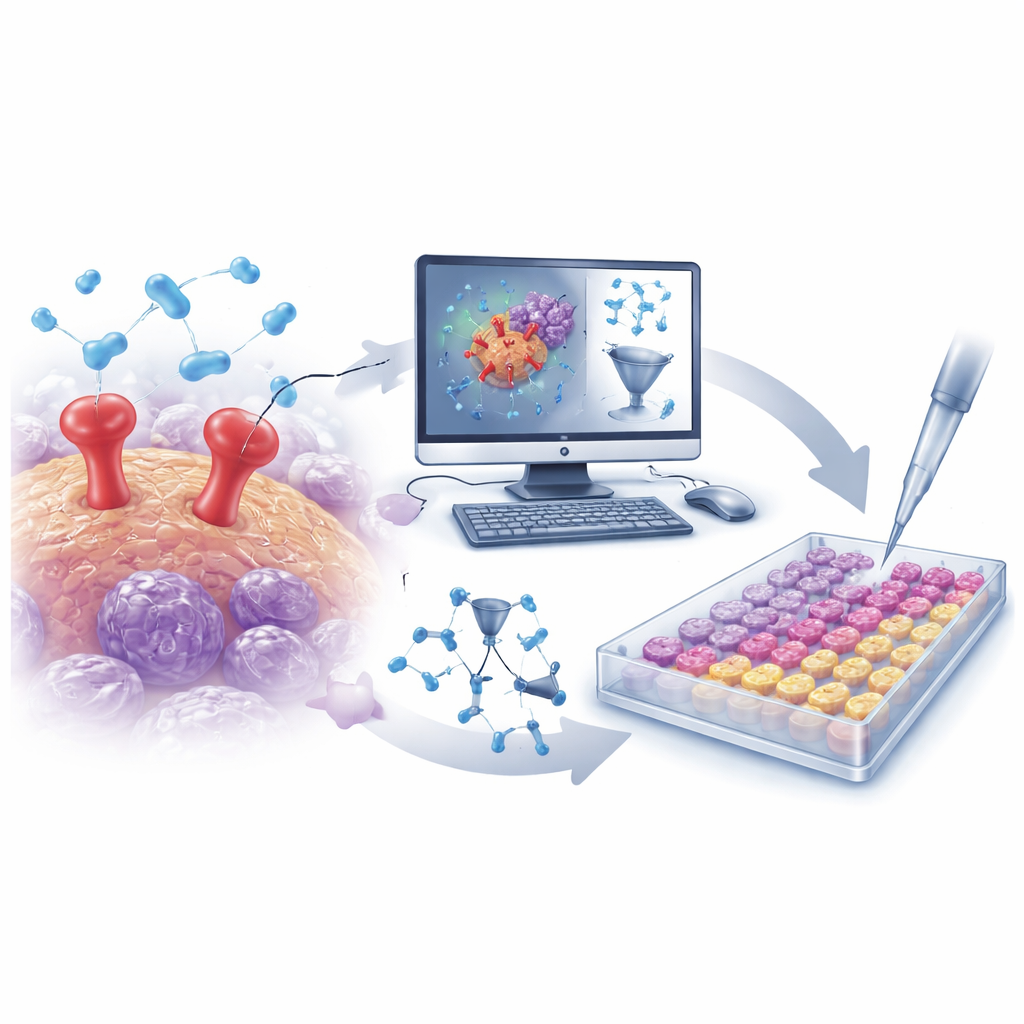
Große chemische Datensätze mit schlauen Algorithmen auswerten
Die Forscher begannen damit, eine umfangreiche Sammlung von mehr als 500 bekannten uPAR-blockierenden Molekülen aus einer öffentlichen Datenbank zusammenzustellen. Die Struktur jedes Moleküls wurde in tausende numerische Deskriptoren übersetzt, die Merkmale wie Größe, Form, Ladungsverteilung und Flexibilität erfassen. Mit diesen Daten baute das Team ein QSAR-Modell (quantitative Struktur‑Aktivitäts‑Beziehung) – ein mathematisches Werkzeug, das lernt, welche strukturellen Eigenschaften ein Molekül zu einem stärkeren uPAR‑Inhibitor machen. Nach sorgfältiger Validierung, um Overfitting zu vermeiden, zeigte das Modell eine hohe Vorhersagekraft für unbekannte Verbindungen und hob mehrere Schlüsselfaktoren hervor, die uPAR‑Hemmung verstärken oder abschwächen. Diese Erkenntnisse lenkten die Suche nach neuen, besser gestalteten Molekülen.
Von virtuellen Screens zu echten Reagenzgläsern
Mit dem trainierten QSAR‑Modell durchsuchte das Team virtuell eine fokussierte Bibliothek von etwa 30.000 protease‑gerichteten Molekülen. Das Modell schränkte diesen großen Pool schnell auf eine kleine Gruppe wahrscheinlicher uPAR‑Inhibitoren ein. Parallel dazu wurden Docking‑Simulationen genutzt, um zu beurteilen, wie gut jeder Kandidat in die uPAR‑Bindetasche passen könnte, und Molekulardynamik‑Simulationen prüften, ob diese gedockten Komplexe über die Zeit stabil blieben. Aus dieser kombinierten in‑silico‑Kampagne gingen zwei herausragende Moleküle hervor: D685‑0061, vom QSAR‑Modell als sehr wirksam eingestuft, und C878‑1660, durch Docking und Simulation als besonders stabil in der Interaktion mit uPAR hervorgehoben.
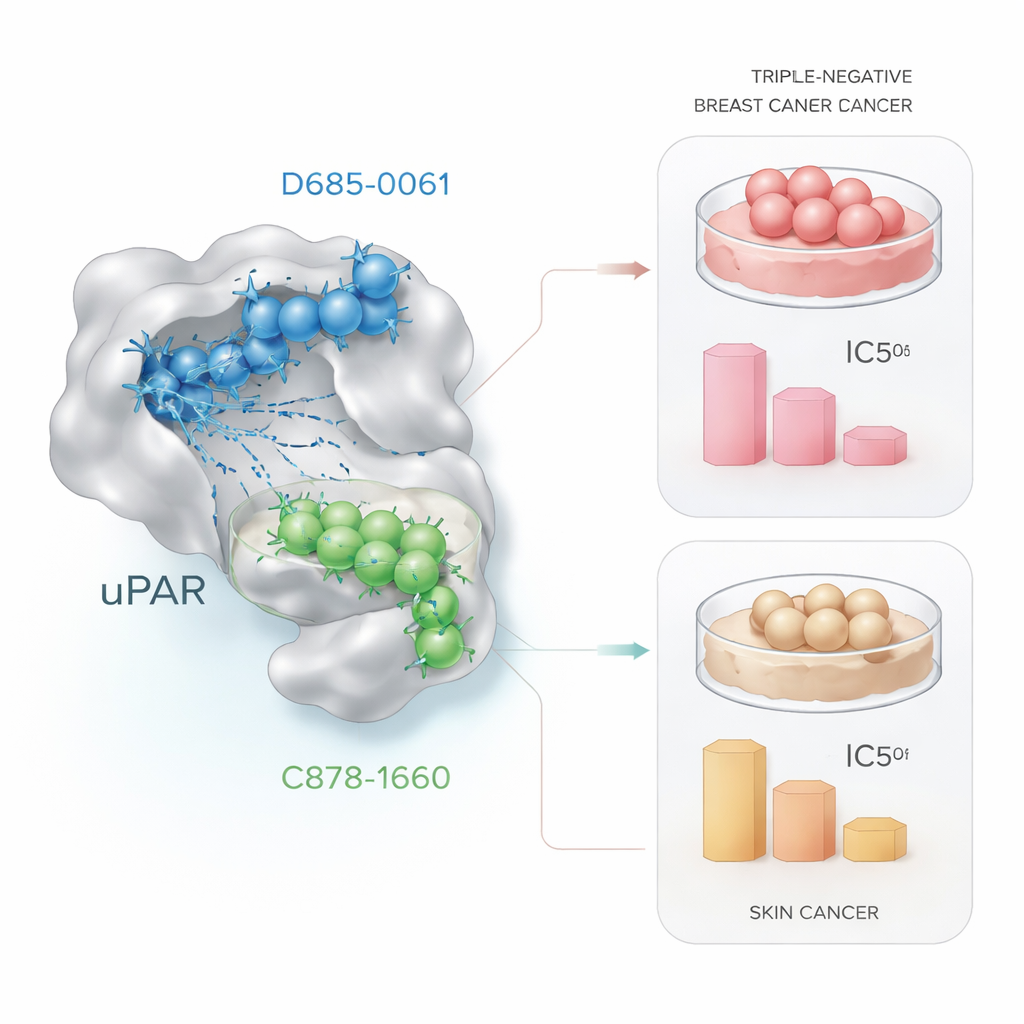
Die Kandidaten in Krebszellen testen
Computergestützte Vorhersagen sind nur dann relevant, wenn sie sich biologisch bestätigen. Um das zu prüfen, setzten die Forscher lebende Krebszellen steigenden Dosen der beiden Leitmoleküle aus und bestimmten die Zellüberlebensrate mit einem standardisierten Labormethode, dem MTT‑Assay. In triple‑negativen Brustkrebszellen (MDA‑MB‑231) tötete D685‑0061 Zellen effizienter und halbierte die Lebensfähigkeit bei etwa 21 Mikromolar, während C878‑1660 etwa die vierfache Menge benötigte. Unter dem Mikroskop zeigten Zellen, die mit D685‑0061 behandelt wurden, deutliche Zeichen programmierter Zellsterblichkeit, wie das Abkugeln, Ablösen von der Oberfläche und Fragmentieren. Im Gegensatz dazu war in Hautkrebszellen (A431) C878‑1660 der stärkere Wirkstoff und erreichte 50 % Zelltod bei etwa 19 Mikromolar gegenüber etwa 28 Mikromolar für D685‑0061, wiederum mit sichtbaren dosisabhängigen Schäden.
Was das für zukünftige Krebsbehandlungen bedeutet
Diese Arbeit liefert kein sofort einsatzfähiges neues Medikament, wohl aber zwei vielversprechende Ausgangspunkte und genauso wichtig eine kraftvolle Blaupause zur Entdeckung weiterer Kandidaten. Durch die Verbindung von Big‑Data‑Modellierung, 3D‑Simulationen und sorgfältigen zellbasierten Experimenten zeigt die Studie, dass uPAR selektiv mit kleinen Molekülen angegriffen werden kann, die aggressive Brust‑ und Hautkrebszellen schädigen. D685‑0061 und C878‑1660 dienen nun als Leitverbindungen, die Chemiker verfeinern können, um Wirksamkeit zu steigern, Sicherheit zu verbessern und pharmakokinetische Eigenschaften zu optimieren. Langfristig könnten auf diesem Ansatz basierende Wirkstoffe dazu beitragen, die Ausbreitung uPAR‑getriebener Krebserkrankungen zu blockieren und einige der heute gefährlichsten Tumoren besser beherrschbar zu machen.
Zitation: Badukle, H., Jawarkar, R.D., Shah, U. et al. From in-silico QSAR modeling to in-vitro MTT assay: experimental validation of novel uPAR leads for triple-negative breast cancer (TNBC) and skin cancer. Sci Rep 16, 5786 (2026). https://doi.org/10.1038/s41598-026-36406-4
Schlüsselwörter: uPAR-Inhibitoren, triple-negativer Brustkrebs, Hautkrebs, computerunterstütztes Wirkstoffdesign, MTT-Zellviabilitätsassay