Clear Sky Science · de
Eine Dichtefunktionaltheorie-Studie zur Adsorption von Cyclophosphamid und Purinethol auf einem kovalenten Triazinrahmen (CTF-2) für Anwendungen in der Arzneimittelabgabe
Warum intelligentere Chemotherapie wichtig ist
Chemotherapeutika retten Leben, wirken aber oft wie ein Flutlicht statt wie ein Scheinwerfer – sie greifen gesunde Zellen neben den Krebszellen an. Das kann zu schweren Nebenwirkungen führen, von Müdigkeit und Infektionen bis hin zu Organschäden. Die hier beschriebene Studie untersucht ein ultradünnes, hochporöses Material namens kovalenter Triazinrahmen (CTF-2) als eine Art „intelligenten Schwamm“, der zwei seit Langem eingesetzte Krebsmedikamente – Cyclophosphamid und Purinethol – sicherer und effizienter dorthin transportieren kann, wo sie gebraucht werden, und sie unter tumornahen Bedingungen wieder freigibt.
Eine neue Art molekularer Schwamm
CTF-2 ist ein künstlich hergestelltes Material, aufgebaut aus Ringen von Kohlenstoff und Stickstoff, verknüpft zu einem flachen, blattartigen Netzwerk mit einer großen zentralen Hohlkammer und viel offenem Raum. Da es dünn, stabil und porös ist, bietet es eine enorme innere Oberfläche zum Einfangen von Wirkstoffmolekülen. Die Autoren konzentrierten sich auf zwei wichtige Krebsmedikamente: Cyclophosphamid, das häufig bei Blutkrebsen und soliden Tumoren eingesetzt wird, und Purinethol (auch Mercaptopurin genannt), das gegen Leukämien und einige entzündliche Darmerkrankungen verwendet wird. Die Idee ist, diese Medikamente sanft auf der Oberfläche von CTF-2 zu ‚andocken‘, sodass sie durch den Blutkreislauf transportiert und selektiver freigesetzt werden können, wodurch Schäden an gesundem Gewebe verringert werden.
Das Unsichtbare mit Computerexperimenten erkunden
Anstatt im Nasslabor zu arbeiten, verwendete das Team fortgeschrittene Quantenrechnungen (Dichtefunktionaltheorie und verwandte Methoden), um zu untersuchen, wie stark jedes Medikament an CTF-2 haften würde und was die Komplexe zusammenhält. Sie optimierten die Geometrien von CTF-2 plus jeweils einem Medikament, maßen die Abstände zwischen berührenden Atomen und berechneten, wie viel Energie frei wird, wenn ein Wirkstoff am Rahmen haftet. Für Cyclophosphamid lag die berechnete Adsorptionsenergie bei etwa −1,04 Elektronenvolt, etwas stärker als die −0,82 Elektronenvolt für Purinethol. Diese Werte, die auch nach Korrekturen für technische Artefakte und unter Einbeziehung von Wasser als Lösungsmittel deutlich günstig bleiben, zeigen, dass beide Wirkstoffe fest genug binden, um geladen zu werden, aber nicht so stark, dass sie später nicht wieder freigegeben werden können.
Sanfte Kräfte leisten wichtige Arbeit
Die Studie zeigt, dass der ‚Klebstoff‘ zwischen den Medikamenten und CTF-2 keine harte chemische Bindung ist, sondern ein Geflecht aus sanften, nicht-kovalenten Kräften. Mithilfe spezialisierter Analysen der Elektronendichte – im Wesentlichen Karten, wo die gemeinsamen Elektronen lokalisiert sind – fanden die Forscher heraus, dass van-der-Waals-Anziehungen (die gleichen schwachen Kräfte, die es Geckos ermöglichen, an Wänden zu haften) und milde elektrostatische Wechselwirkungen dominieren. Diese Interaktionen treten in kurzen, aber nicht-bindenden Abständen zwischen Wasserstoff-, Stickstoff-, Sauerstoff-, Schwefel- und Kohlenstoffatomen der Wirkstoffe und des Rahmens auf. Zusätzliche Rechnungen, die die Gesamtanziehung in verschiedene Komponenten aufschlüsselten, bestätigten, dass elektrostatische und Dispersions- (van-der-Waals-) Kräfte den größten Teil der stabilisierenden Anziehung liefern, während abstoßende Kräfte verhindern, dass das Medikament zu tief einsinkt oder irreversibel bindet.
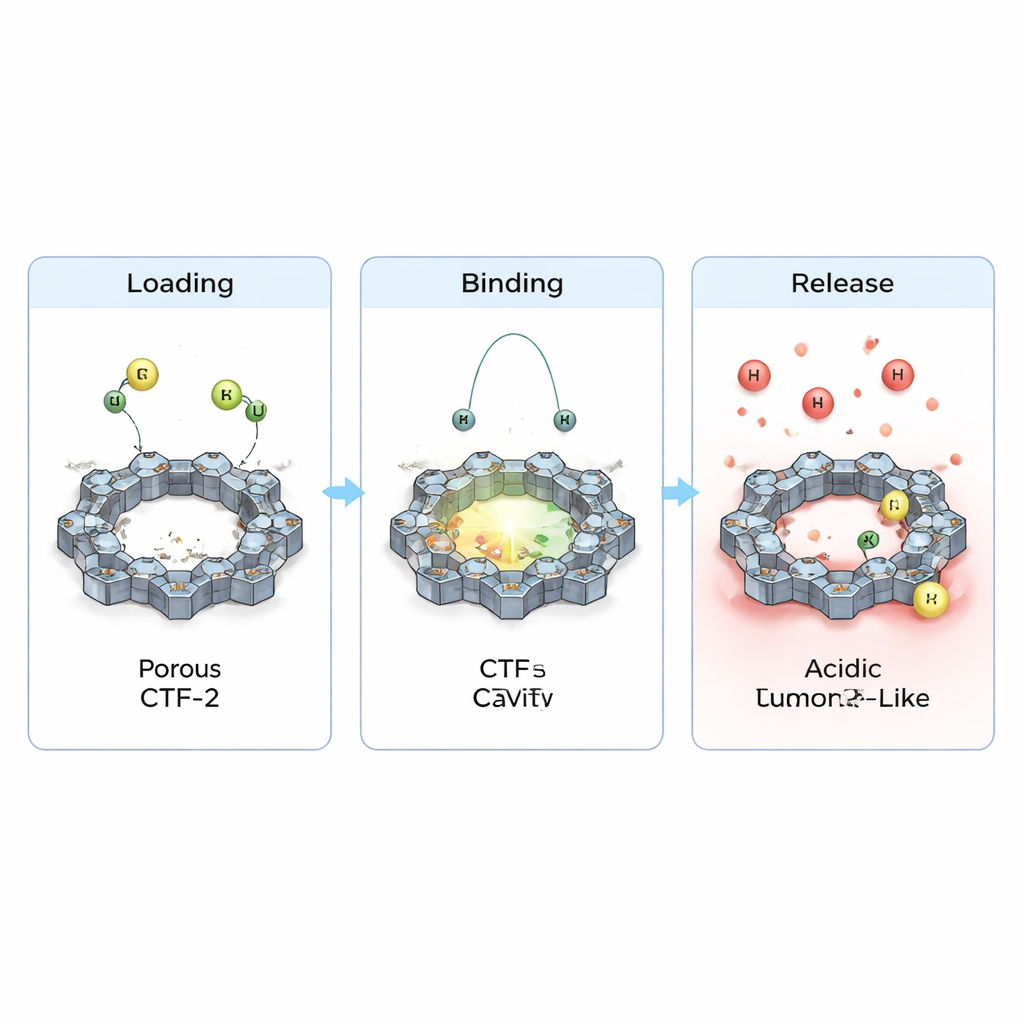
Hinweise auf stabile Beladung und steuerbare Freisetzung
Das Team untersuchte außerdem, wie sich Elektronen verschieben, wenn die Wirkstoffe auf CTF-2 sitzen, und wie sich dadurch grundlegende elektrische Eigenschaften ändern. Sie beobachteten kleine, aber klare Ladungsüberträge zwischen jedem Medikament und dem Rahmen sowie eine leichte Verringerung der Energielücke zwischen besetzten und unbesetzten elektronischen Zuständen. Das deutet darauf hin, dass Reaktivität und Leitfähigkeit des Materials bei Beladung subtil verändert werden, eine nützliche Eigenschaft für künftige Sensor- oder Theranostik-Anwendungen. Entscheidend ist, dass bei Simulation eines säureren Umfelds, wie es in Tumornähe vorkommt (durch Zugabe zusätzlicher Protonen), die berechnete Bindung schwächer wurde und die Kontaktabstände zunahmen. Einfach ausgedrückt legen die Simulationen nahe, dass CTF-2 die Wirkstoffe unter normalen, blutähnlichen Bedingungen halten kann, sie aber in tumornahen, sauren Umgebungen eher freigibt – genau das gewünschte Verhalten für eine gezielte Abgabe.
Was das für künftige Krebstherapien bedeutet
Insgesamt zeichnen diese Berechnungen CTF-2 als vielversprechenden Träger für Cyclophosphamid und Purinethol: Es kann sie stabil auf seiner porösen Oberfläche aufnehmen, sie während der Zirkulation schützen und bei Änderung der lokalen Chemie nahe einem Tumor wieder freisetzen. Obwohl die Arbeit theoretisch ist und experimentell bestätigt werden muss, deutet sie darauf hin, dass fein gestaltete, stickstoffreiche Rahmen wie CTF-2 dazu beitragen könnten, bewährte, aber einfache Chemotherapeutika in intelligentere Medikamente zu verwandeln – indem sie starke Dosen genau dorthin liefern, wo sie am meisten gebraucht werden, und gleichzeitig die Kollateralschäden an gesundem Gewebe verringern.
Zitation: Tariq, T., Yar, M., Bayach, I. et al. A density functional theory study of cyclophosphamide and purinethol adsorption on a covalent triazine framework (CTF-2) for drug delivery applications. Sci Rep 16, 6125 (2026). https://doi.org/10.1038/s41598-026-36405-5
Schlüsselwörter: Nanoträger, Arzneimittelabgabe, Krebschemotherapie, kovalenter Triazinrahmen, computergestützte Modellierung