Clear Sky Science · de
Ein interaktives, kaskadiertes Deep‑Learning‑Framework mit fachlicher Feinabstimmung für präzise Segmentierung von Striatum‑Unterregionen
Warum die Kartierung winziger Hirnregionen wichtig ist
Das Striatum, eine kleine, tief im Gehirn liegende Struktur, spielt eine zentrale Rolle für Bewegung und Motivation und ist bei Erkrankungen wie der Parkinson‑Krankheit stark betroffen. Ärztinnen und Ärzte nutzen häufig PET‑ und MRI‑Aufnahmen, um chemische Veränderungen in diesem Bereich zu messen, doch das Striatum ist in viele winzige Unterregionen unterteilt, die schwer zu sehen und exakt abzugrenzen sind. Diese Arbeit stellt eine neue computerunterstützte Methode vor, genannt StriaSeg‑iARM, die Spezialisten hilft, diese Grenzen genauer und effizienter zu zeichnen — selbst bei Menschen, deren Gehirne durch Alterung oder Krankheit verändert sind.
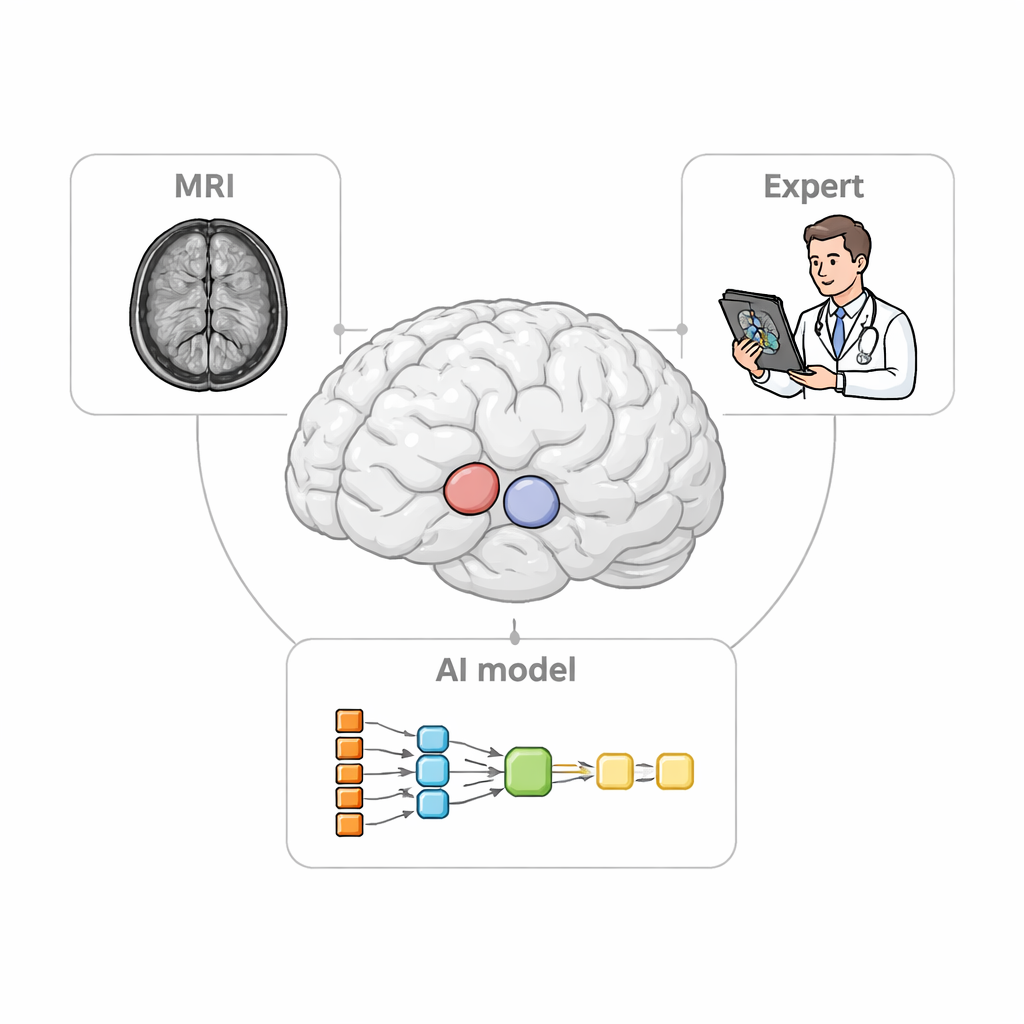
Das klinische Problem in klarem Blick
Wenn Neurologinnen und Neurologen Zustände wie die Parkinson‑Krankheit beurteilen, verlassen sie sich auf PET‑Scans, um zu verfolgen, wie dopaminbezogene Signale in verschiedenen Teilen des Striatums variieren. Damit dies korrekt gelingt, müssen sie zuerst kleine dreidimensionale „Regions of Interest“ im MRI definieren, die als Messgefäße für die PET‑Daten dienen. Das manuelle Nachzeichnen dieser Regionen ist langsame, mühsame Arbeit und kann zwischen Expertinnen und Experten variieren. Bestehende Software erkennt meist nur die größeren Strukturen automatisch und hat oft Schwierigkeiten bei Patientinnen und Patienten mit geschrumpftem oder verzerrtem Gehirn — ein häufiges Bild in fortgeschrittenen neurodegenerativen Erkrankungen. Diese Schwächen können das wahre Schadensmuster verwischen und die Aussagekraft der Bildgebung als diagnostisches Instrument schwächen.
Ein schlauer Assistent in zwei Schritten
Die Forschenden entwickelten StriaSeg‑iARM als zweistufiges Deep‑Learning‑System, das direkt im individuellen Gehirnraum der Person arbeitet, anstatt den Scan in eine Standardvorlage zu zwingen. In der ersten Stufe findet das Programm das gesamte Striatum auf einem dreidimensionalen MRI. In der zweiten Stufe teilt es diese Struktur in 12 anatomisch definierte Unterregionen auf beiden Gehirnhälften ein. Zwischen diesen beiden Stufen liegt die entscheidende Innovation: ein interaktiver Schritt, in dem ein Experte die grobe Umrisszeichnung der ersten Stufe schnell prüfen und bei Bedarf korrigieren kann, bevor die feinere Unterteilung ausgeführt wird. Dieser Ansatz verbindet die Geschwindigkeit der Automatisierung mit dem Urteilsvermögen einer geschulten Fachperson.
Training und Tests in realen Gehirnen
Um dem System beizubringen, worauf es achten soll, sammelte das Team Hunderte von MRI‑Scans aus mehreren Krankenhäusern und von verschiedenen Scanner‑Typen und erstellte sorgfältige manuelle Umrisse der 12 striatalen Unterregionen. Anschließend testeten sie das Modell an zwei externen Datensätzen, die sowohl MRI‑ als auch dopaminbezogene PET‑Scans enthielten: einer aus relativ frühen Parkinson‑Patientinnen und ‑patienten sowie gesunden Freiwilligen, und ein anderer aus einer älteren, stärker betroffenen klinischen Gruppe mit ausgeprägtem Hirnschwund und gemischten Diagnosen. In diesen herausfordernden Fällen erzielte StriaSeg‑iARM durchweg bessere Übereinstimmungen mit manuellen Expertenzeichnungen als traditionelle atlasbasierte Methoden und ein einfacheres einstufiges Deep‑Learning‑Modell, mit höherer Überlappung, genaueren Begrenzungen und stabilen Volumenmessungen.
Schärfere Messungen für chemische Hirnscans
Da das Endziel die Quantifizierung von PET‑Signalen ist, untersuchten die Autorinnen und Autoren auch, wie sich verschiedene Segmentierungsmethoden auf die PET‑Ausgaben auswirken. Mithilfe eines Standardmaßes für Tracer‑Bindung in jeder Unterregion verglichen sie automatische Ergebnisse mit jenen auf Basis manueller Umrisse. Die Atlas‑Methode neigte dazu, die Bindung zu unterschätzen, besonders bei Patientinnen und Patienten mit stärkeren Veränderungen, während das einfache Deep‑Learning‑Modell in einigen Regionen weiterhin spürbare Verzerrungen zeigte. Im Gegensatz dazu lieferten die kaskadierten Modelle — insbesondere wenn der interaktive Korrekturschritt genutzt wurde — PET‑Werte, die eng der Expertenreferenz folgten, mit minimaler Verzerrung und Streuung. Das Team zeigte außerdem, dass ein einfacher Unsicherheitswert aus der ersten Stufe etwa ein Viertel der schwierigsten Fälle markieren kann, in denen fachliche Feinabstimmung wirklich nötig ist, während der Rest vollständig automatisch bleibt.
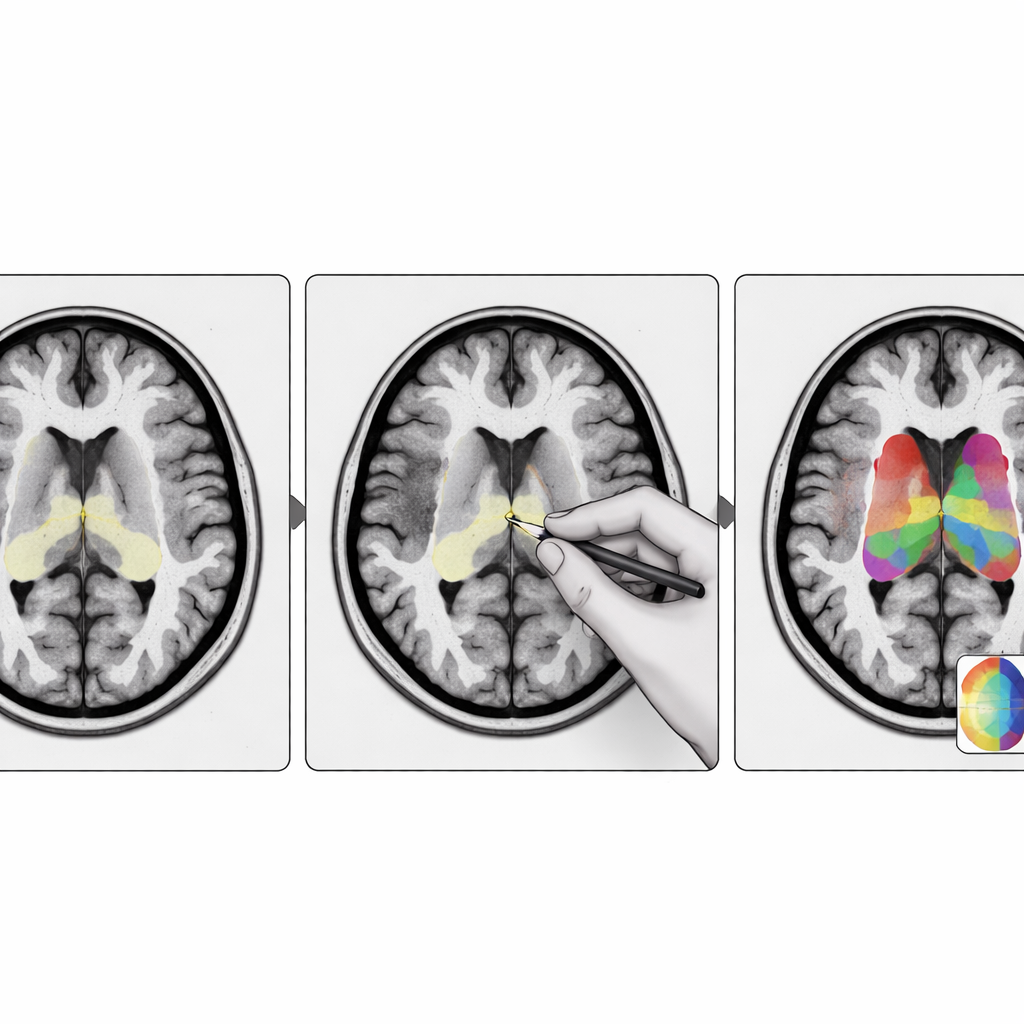
Was das für Patientinnen, Patienten und Kliniker bedeutet
Für Nicht‑Spezialisten lautet die Quintessenz: bessere digitale Karten kleiner Hirnregionen können chemische Hirnscans vertrauenswürdiger machen. StriaSeg‑iARM bietet ein flexibles Framework, in dem ein Deep‑Learning‑Modell den Großteil der Arbeit übernimmt, aber Spezialistinnen und Spezialisten bei kniffligen Fällen ohne erneutes Training des Systems eingreifen können. Diese Kombination aus Automatisierung und fachlicher Aufsicht verbessert die Präzision der Messungen, die zur Diagnose und Verlaufskontrolle von Erkrankungen wie der Parkinson‑Krankheit verwendet werden, und könnte auf andere Organe und Erkrankungen übertragen werden, in denen kleine, schwer sichtbare Strukturen wichtige Hinweise liefern.
Zitation: Kim, J., Kim, D., Kim, S. et al. An interactive cascaded deep learning framework with expert refinement for accurate striatal subregion segmentation. Sci Rep 16, 6550 (2026). https://doi.org/10.1038/s41598-026-36399-0
Schlüsselwörter: Bildgebung bei Parkinson‑Krankheit, Striatum‑Segmentierung, Deep Learning in der Radiologie, Hirn‑PET MRI, biomarker neurodegenerativer Erkrankungen