Clear Sky Science · de
Staphylococcus capitis-Stamm, der zwei Bakteriocine produziert, Capidermicin und Micrococcin P1, zeigt breites antimikrobielles Spektrum
Warum winzige Hautbakterien für Superkeim-Bedrohungen wichtig sind
Antibiotikaresistente Infektionen nehmen weltweit zu, und Ärzten gehen zunehmend verlässliche Wirkstoffe aus. Eine vielversprechende Idee ist, unsere eigenen „guten" Mikroben zur Bekämpfung der schädlichen Keime zu nutzen. Diese Studie konzentriert sich auf ein häufiges Hautbakterium, Staphylococcus capitis, und zeigt, dass ein bestimmter Stamm, HBC3 genannt, von Natur aus zwei potente keimtötende Moleküle herstellt. Zusammen können diese Moleküle gefährliche Krankenhauskeime wie methicillinresistenten Staphylococcus aureus (MRSA) eindämmen, was nahelegt, dass freundliche Hautbakterien selbst zu künftigen Werkzeugen gegen Infektionen werden könnten.
Ein Hautbewohner mit versteckter Schlagkraft
S. capitis lebt normalerweise unauffällig auf unserer Haut, besonders auf der Kopfhaut, und ist meist harmlos. Die Forscher untersuchten 18 S.-capitis-Stämme, die aus Nasenproben von Menschen stammten, um herauszufinden, ob einer von ihnen MRSA hemmen kann. Ein Stamm, HBC3, stach hervor. In Labortests unterdrückte er eine breite Palette grampositiver Bakterien stark, darunter MRSA, vancomycinresistente Enterokokken (VRE), Streptococcus pyogenes, Listeria monocytogenes sowie Bacillus- und Clostridium-Arten, die schwere Erkrankungen verursachen können. Auffällig war, dass er auf mehrere häufige gramnegative Bakterien wie Escherichia coli und Klebsiella pneumoniae keine Wirkung zeigte, was auf eine gezielte, aber starke Wirkung statt auf wahlloses Töten hindeutet. 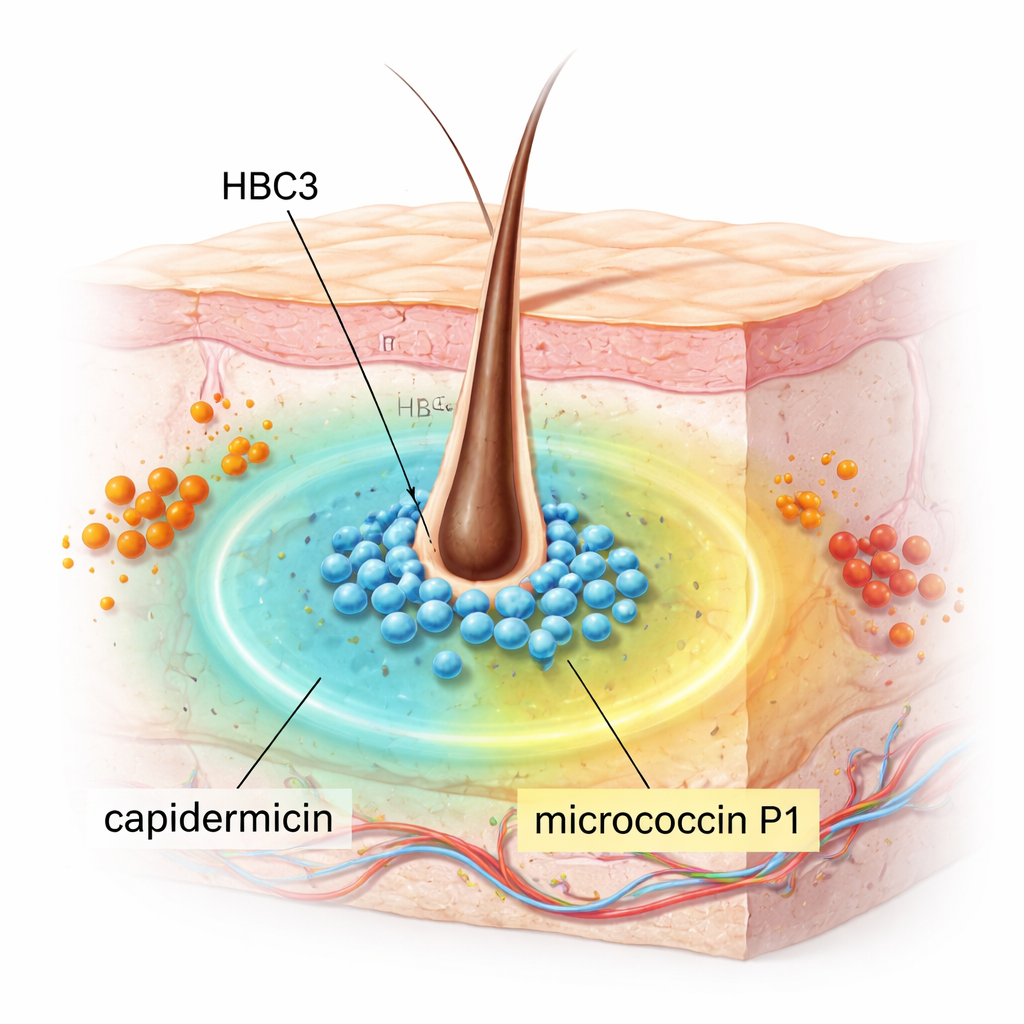
Zwei natürliche Antibiotika auf einem einzigen genetischen „Mini-Chromosom"
Um zu klären, wie HBC3 diese breite antimikrobielle Wirkung erzielt, entschlüsselten die Forscher sein gesamtes Genom. Sie identifizierten ein kleines zirkuläres DNA-Element, ein Plasmid namens pHBC3_1, das die vollständigen Anweisungen zur Herstellung von zwei verschiedenen Bakteriocinen trägt – natürlichen, antibiotikaähnlichen Peptiden, die von Bakterien produziert werden. Eines ist Capidermicin, ein kleines positiv geladenes Peptid, das bereits in anderen S.-capitis-Stämmen beschrieben wurde. Das andere ist Micrococcin P1 (MP1), ein Thiopeptid, das die Proteinproduktion in Zielbakterien blockiert und zuvor nicht in S. capitis berichtet worden war. Wurde dieses Plasmid aus HBC3 entfernt, verlor der Stamm vollständig seine antibakterielle Aktivität, was bestätigt, dass diese Gene für seine Abwehrfähigkeit entscheidend sind.
Verschiedene Ziele, gemeinsames Ziel
Durch die separate Reinigung der einzelnen Bakteriocine testeten die Wissenschaftler deren Wirksamkeit gegen verschiedene Mikroben. MP1 zeigte bei niedrigen Konzentrationen ein breites und starkes Wirkspektrum gegen viele grampositive Kokken, darunter MRSA und Enterokokken. Capidermicin hingegen war am effektivsten gegen stäbchenförmige grampositive Bakterien wie Bacillus coagulans und Listeria, zeigte unter den hier verwendeten Bedingungen aber nur geringe oder keine Wirkung gegen Staphylokokken. Als das Team beide Peptide gegen B. coagulans kombinierte, beobachteten sie einen additiven Effekt: Niedrigere Dosen zusammen erreichten stärkere Wachstumshemmung als jedes Peptid allein. Diese komplementäre Zielausrichtung ermöglicht es HBC3, durch den Einsatz zweier unterschiedlicher molekularer Waffen, die auf verschiedene Bakterienformen und Zelloberflächen abgestimmt sind, eine breitere Palette von Konkurrenten zu unterdrücken. 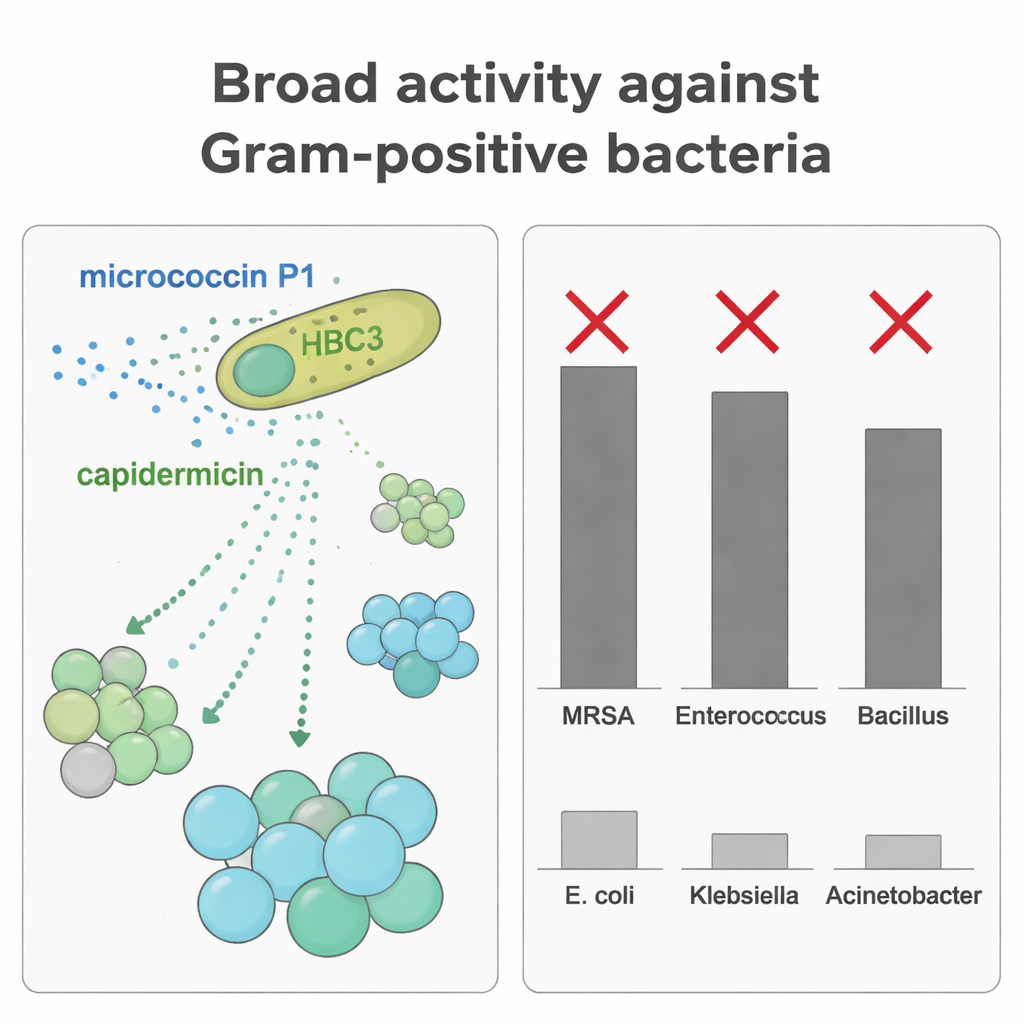
Platz gewinnen in überfüllten mikrobiellen Nachbarschaften
Um reale Konkurrenzsituationen nachzuahmen, kultivierten die Forscher HBC3 gemeinsam mit MRSA, VRE und B. coagulans auf denselben Platten. Der normale HBC3-Stamm eliminierte diese Pathogene in den Mischkulturen nahezu vollständig, während eine Variante ohne das Plasmid ihnen das Wachstum erlaubte. Genetische Vergleiche deuten darauf hin, dass das Dual-Bakteriocin-Plasmid wahrscheinlich durch frühere Fusion und Umgestaltung separater Plasmide entstand, begünstigt durch mobile DNA-Elemente, die Gencluster zwischen Bakterien bewegen können. Dieses zusammengesetzte Plasmid verschafft HBC3 einen klaren Vorteil in überfüllten Umgebungen wie Haut oder Schleimhäuten, wo viele Mikroben um Nährstoffe und Raum konkurrieren.
Vom Hautverbündeten zum möglichen Probiotikum?
Die Studie kommt zu dem Schluss, dass S. capitis HBC3 mit einer seltenen Kombination aus zwei unterschiedlichen Bakteriocinen auf einem Plasmid ausgestattet ist, die es ihm ermöglicht, mehrere klinisch bedeutsame grampositive Erreger, einschließlich antibiotikaresistenter Stämme, stark zu hemmen. Da HBC3 selbst keiner bekannten Hochrisikolinie angehört und keine nachweisbaren Resistenzgene gegen Arzneimittel trägt, könnte es ein Kandidat für die Entwicklung als gezieltes Probiotikum oder Dekolonisationsmittel sein – etwa, um selektiv S. aureus auf der Haut oder in der Nase zu reduzieren und gleichzeitig harmlosere Nachbarn zu schonen. Bevor solche Anwendungen Realität werden, sind jedoch Sicherheitsprüfungen, Wirksamkeitsnachweise in Tieren und Menschen sowie Untersuchungen zu langfristigen Auswirkungen auf das normale Mikrobiom erforderlich. Die Arbeit unterstreicht jedoch, wie unsere eigenen Mikroben dazu beitragen könnten, der anhaltenden Superkeimkrise entgegenzuwirken.
Zitation: Ohdan, K., Suzuki, Y., Kawada-Matsuo, M. et al. Staphylococcus capitis strain producing dual bacteriocins, capidermicin and micrococcin P1, shows broad-spectrum antimicrobial activity. Sci Rep 16, 6835 (2026). https://doi.org/10.1038/s41598-026-36393-6
Schlüsselwörter: Bakteriocine, Staphylococcus capitis, Micrococcin P1, Capidermicin, Antibiotikaresistenz