Clear Sky Science · de
Einsatz des High-Throughput-Virtual-Screening-(HTVS)-Ansatzes zur Identifizierung neuer Lactatdehydrogenase-(LDH)-Hemmer mit antitumoralen Eigenschaften
Warum diese Forschung für die Krebsbehandlung wichtig ist
Krebszellen verändern häufig ihre Energiegewinnung, und diese Verschiebung kann genutzt werden, um gezieltere, selektivere Wirkstoffe zu entwickeln. In dieser Studie untersuchen die Forschenden ein zentrales Stoffwechselenzym, die Lactatdehydrogenase (LDH), das Tumoren hilft, unter widrigen Bedingungen zu gedeihen und Behandlungen zu widerstehen. Mithilfe fortschrittlicher rechnergestützter Screening-Verfahren und Labortests identifizierten sie zwei neue kleine Moleküle, die LDH blockieren und in Prostatakrebszelllinien vielversprechende antitumorale Effekte zeigen.
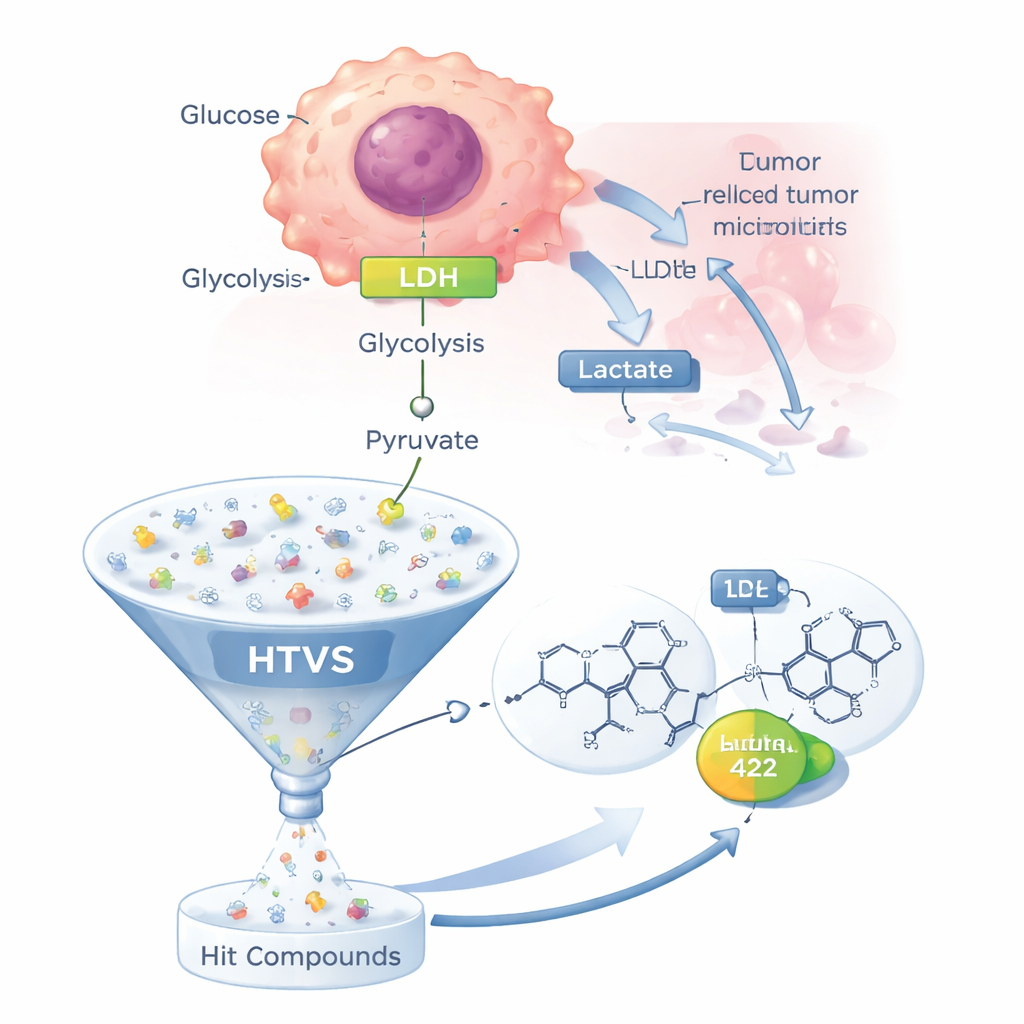
Der ungewöhnliche Stoffwechsel von Krebszellen
Die meisten gesunden Zellen nutzen Sauerstoff effizient in ihren Mitochondrien zur Energieerzeugung. Viele Krebszellen verlassen sich jedoch stark auf einen weniger effizienten Weg, die Glykolyse, selbst wenn ausreichend Sauerstoff vorhanden ist — ein Phänomen, das als Warburg-Effekt bekannt ist. Auf diesem Abkürzungsweg wird Glukose zu Pyruvat abgebaut, das dann von LDH zu Laktat umgewandelt wird, statt in die Mitochondrien eingespeist zu werden. Das Laktat wird aus der Zelle exportiert, wodurch die Umgebung des Tumors ansäuert; das hilft Krebszellen, dem Zelltod zu entgehen, die Immunantwort abzuschwächen und die Wirkung vieler Chemotherapeutika zu dämpfen. Da LDH im Zentrum dieses veränderten Stoffwechsels steht und noch kein LDH‑gerichtetes Medikament zugelassen ist, ist es ein vorrangiges Ziel für die Entwicklung neuer Krebstherapien.
Mithilfe von Computern eine halbe Million Moleküle durchforsten
Anstatt potenzielle Wirkstoffe einzeln im Labor zu testen, nutzte das Team eine High-Throughput-Virtual-Screening-(HTVS)-Strategie. Sie begannen mit 28 in der Literatur beschriebenen LDH‑hemmenden Molekülen und leiteten daraus ein „Pharmakophor“ ab — ein abstraktes 3D-Muster von Merkmalen, das ein guter LDH‑Inhibitor wahrscheinlich teilt. Dieses Modell wandten sie dann auf eine kommerzielle Bibliothek von etwa 500.000 wirkstoffähnlichen Molekülen an und prüften, welche Kandidaten die wesentlichen Merkmale erfüllten. Etwa 110.000 Moleküle bestanden dieses erste Filter, und eine weitere Auswahl anhand gängiger Regeln zur „Drug‑Likeness“ reduzierte die Liste auf 2.337 realistischere Kandidaten für das Docking an das LDH‑Enzym.
Auf die besten Binder fokussieren
Im nächsten Schritt schätzten die Forschenden, wie fest diese Kandidaten in die aktive Stelle von LDH passen könnten. Mithilfe mehrerer Stufen rechnerischen Dockings berechneten sie, wie jedes Molekül mit bestimmten Aminosäuren innerhalb der Enzymtasche interagieren könnte. Dieser mehrstufige Prozess verengte den Pool schrittweise von Tausenden Kandidaten auf lediglich 59 vielversprechende Moleküle und schließlich auf fünf klare Treffer mit besonders starker vorhergesagter Bindung. Zwei davon, bezeichnet als Verbindungen 15 und 422, stachen hervor, weil molekulardynamische Simulationen auf dem Computer darauf hindeuteten, dass sie über die Zeit ungewöhnlich stabile Komplexe mit LDH bilden, zentrale Kontakte zu kritischen Resten in der aktiven Stelle aufrechterhalten und gleichzeitig die Gesamtstruktur des Proteins vernünftig bewahren.
Vom Screening zu echten Krebszellen
Um zu prüfen, ob diese Treffer in lebenden Systemen relevant sind, kauften die Wissenschaftler die Verbindungen 15 und 422 und testeten sie in den Prostatakrebszelllinien DU‑145 und PC‑3. Beide Moleküle hemmten die LDH‑Aktivität in Zellen bereits im Nanomolarbereich und verlangsamt en auch direkt die Aktivität eines gereinigten LDH‑Enzyms, obwohl sie etwas weniger potent waren als ein bekannter experimenteller Inhibitor namens GNE‑140. In Proliferationsassays reduzierten die Verbindungen das Überleben der Krebszellen in niedrigen Mikromolarbereichen und kamen damit erneut an die Leistung von GNE‑140 heran. Weitere Experimente zeigten, dass die Behandlungen oxidativen Stress leicht erhöhten, das mitochondriale Membranpotenzial störten — ein Zeichen geschwächter Energiefabriken — und in DU‑145‑Zellen programmierte Zellsterblichkeit (Apoptose) auslösten, wobei Verbindung 15 die aktivere der beiden war.
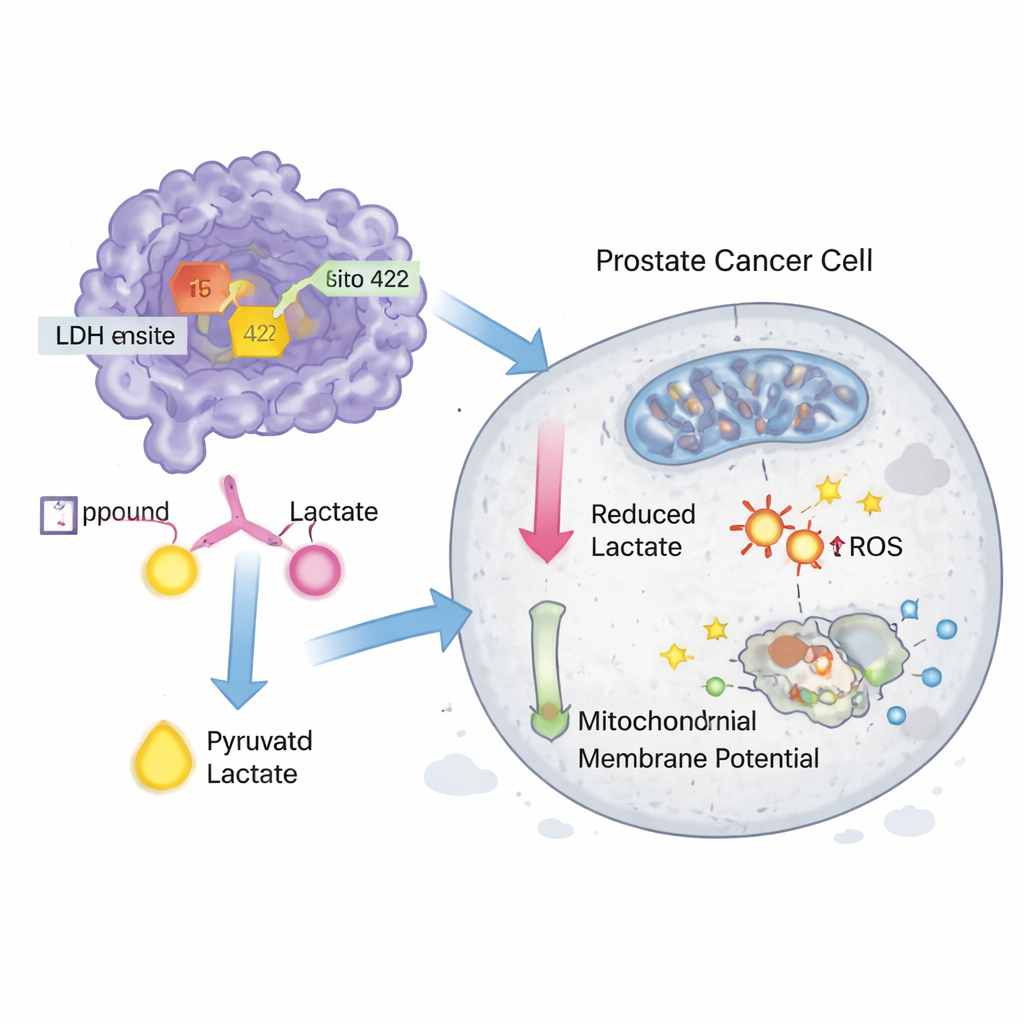
Was das für künftige Krebsmedikamente bedeuten könnte
Obwohl diese Moleküle keine fertigen Medikamente sind, bieten sie wertvolle Ausgangspunkte für die Wirkstoffentwicklung. Sowohl Verbindung 15 als auch 422 weisen chemische Eigenschaften auf, die bessere Löslichkeit, Permeabilität und allgemein höhere „Drug‑Likeness“ andeuten als einige bestehende LDH‑Inhibitoren, was sie zu attraktiven Leads für weitere Optimierung macht. Die Studie zeigt, wie groß angelegtes rechnergestütztes Screening, geleitet von bekannten Strukturmerkmalen, neue LDH‑Hemmer zutage fördern kann, die Krebszellen schwächen, indem sie deren veränderte Energieversorgung austrocknen. Mit weiterer Arbeit zur Verfeinerung ihrer Strukturen, rigoroserem Test direkter Bindung und Untersuchungen im Tiermodell könnten diese Verbindungen zu einer neuen Klasse antitumoraler Wirkstoffe beitragen, die Tumoren über ihre spezifischen metabolischen Verwundbarkeiten angreifen.
Zitation: Huang, Y., Benni, S., Yadav, U.P. et al. Deploying the high-throughput virtual screening (HTVS) approach for the identification of new lactate dehydrogenase (LDH) inhibitors with anticancer assets. Sci Rep 16, 5921 (2026). https://doi.org/10.1038/s41598-026-36385-6
Schlüsselwörter: Lactatdehydrogenase-Hemmer, Krebsstoffwechsel, virtuelles Screening, Prostatakrebs, Entdeckung antitumoraler Wirkstoffe