Clear Sky Science · de
Hochregulierung von MGMT vermittelt Temozolomid‑Resistenz durch USP5‑Abhängigkeit
Warum einige Hirntumoren auf ein Schlüsselmedikament nicht mehr ansprechen
Bei Menschen mit dem aggressiven Hirnkrebs Glioblastom ist eines der wichtigsten Medikamente, auf das Ärztinnen und Ärzte setzen, Temozolomid. Zunächst kann dieses Chemotherapeutikum das Fortschreiten verlangsamen, doch Tumoren lernen oft, sich dagegen zu wappnen. Diese Studie stellt eine praktische Frage mit lebenswichtigen Folgen: Was genau erlaubt diesen Krebszellen, dem Medikament zu entkommen, und lassen sich neue Schwachstellen finden, damit die Behandlung wieder wirkt?
Ein Medikament, das zuerst hilft und dann an Wirkung verliert
Temozolomid wirkt, indem es die DNA schnell teilender Tumorzellen schädigt und so ihren Tod erzwingt. Viele Glioblastome produzieren jedoch ein Reparaturprotein namens MGMT, das diese Schäden rückgängig machen kann. Patientinnen und Patienten, deren Tumoren MGMT einschalten, haben tendenziell schlechtere Verläufe, weil die Wirkung des Medikaments aufgehoben wird. Ärztinnen und Ärzte können die Ansprechrate teilweise vorhersagen, indem sie untersuchen, ob das MGMT‑Gen chemisch ausgeschaltet (methylisiert) oder eingeschaltet (unmethylisiert) ist, aber das erklärt nicht vollständig, wie Resistenz entsteht oder wie MGMT‑Spiegel in Tumorzellen über die Zeit hoch bleiben.
Verborgene Helfer, die das Reparaturprotein schützen
Die Autorinnen und Autoren untersuchten eine weitere Kontrollebene: die molekularen „Aufräumteams“, die entscheiden, welche Proteine abgebaut und welche verschont werden. Normalerweise markieren Zellen abgenutzte Proteine zur Zerstörung, während eine Gruppe von Enzymen, die deubiquitinierenden Enzyme (DUBs), Proteine vor diesem Schicksal bewahren kann. Durch Auswertung großer öffentlicher Krebsdatenbanken und Untersuchung von im Labor gezüchteten, medikamentenresistenten Glioblastom‑Zelllinien konzentrierte sich das Team auf zwei solcher Enzyme, USP5 und USP8. In Tumorproben von Hunderten Patientinnen und Patienten traten höhere USP5‑Werte häufig zusammen mit erhöhten MGMT‑Werten auf, und Patientinnen und Patienten, deren Tumoren beide Gene stark hochreguliert zeigten, starben im Allgemeinen früher.
Resistenz im Labor aufbauen
Um das nachzubilden, was bei Patientinnen und Patienten passiert, setzten die Forschenden zwei gängige Glioblastom‑Zelllinien langsam steigenden Temozolomid‑Dosen aus, bis die Zellen resistent wurden. In diesen „gehärteten“ Zellen stiegen mehrere DUBs an, besonders stark jedoch USP5, USP8, USP10 und das Reparaturprotein MGMT. Wenn das Team kleine RNA‑Moleküle einsetzte, um USP5 oder USP8 stummzuschalten, wurden die resistenten Zellen plötzlich verwundbar: Sie aktivierten Selbstzerstörungsprogramme, darunter Apoptose und eine Form stressbedingter Selbstverdauung, bekannt als Autophagie. Gleichzeitig fielen die MGMT‑Spiegel stark ab, und ein weiteres mit Resistenz assoziiertes Protein, USP10, wurde ebenfalls reduziert, was darauf hindeutet, dass diese Enzyme nahe der Spitze eines Überlebensnetzwerks sitzen.
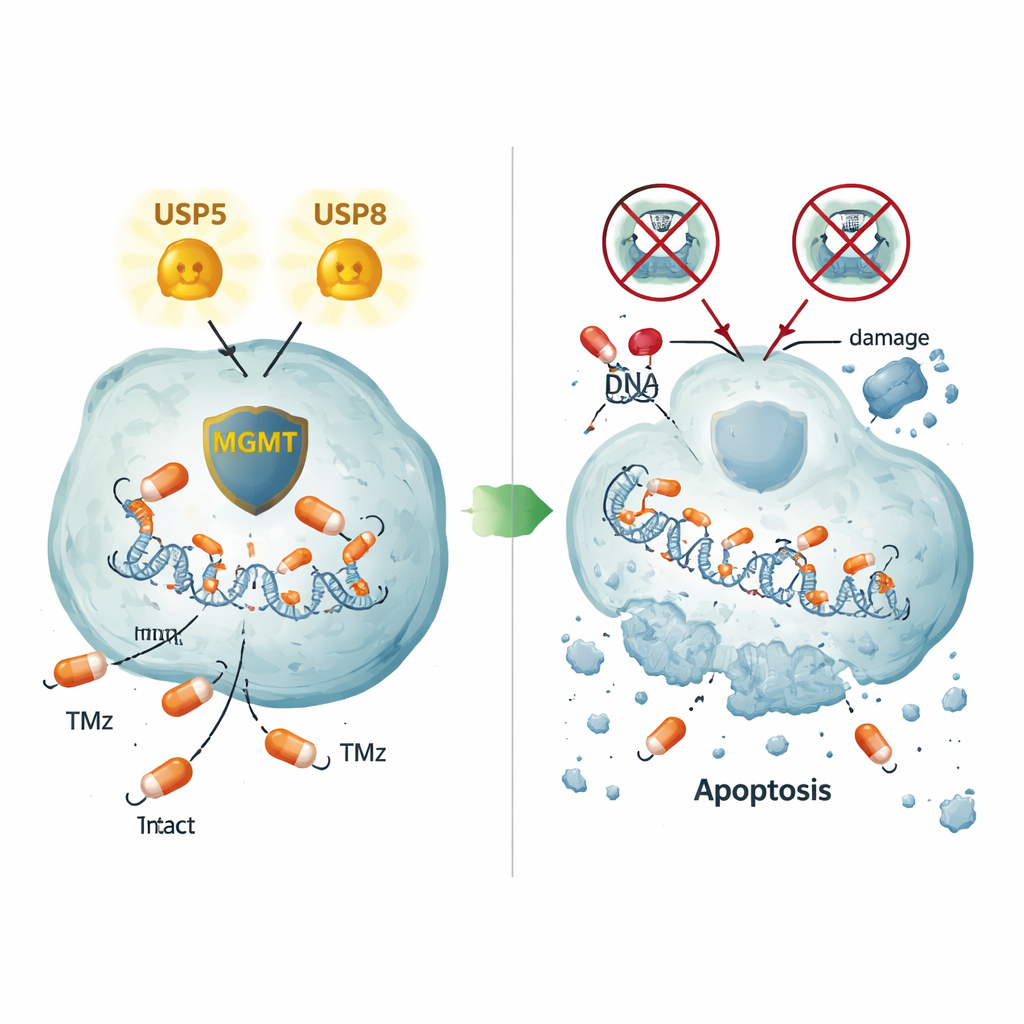
Zwei unterschiedliche Wege, MGMT am Leben zu erhalten
Sorgfältige Bildgebung von Tumorzellen und menschlichem Tumorgewebe zeigte, dass USP5 und MGMT oft im selben Zellbereich vorkommen, besonders im Zytoplasma. Die Blockade von USP5 senkte nicht nur MGMT, sondern führte auch dazu, dass MGMT vom zellulären Protein‑Schredderapparat abgebaut wurde — ein Prozess, der sich durch das Medikament Bortezomib, das das Proteasom hemmt, rückgängig machen ließ. Die Überexpression von USP5 in ansonsten MGMT‑negativen Zellen reichte aus, um MGMT‑Proteinspiegel anzuheben, sogar in einer Nicht‑Hirnzelllinie, was einen direkten stabilisierenden Effekt bestätigt. USP8 erwies sich als anders arbeitend: Dessen Herunterregulieren reduzierte ebenfalls MGMT, ohne USP5 zu verändern, und zeigt damit eine zweite, USP5‑unabhängige Route, die MGMT erhält. Selbst in einer resistenten Zelllinie, die überhaupt kein MGMT produzierte, löschte das Abschalten von USP5 oder USP8 weiterhin umfangreichen Zelltod aus, was auf zusätzliche Resistenzwege hindeutet, die von diesen Enzymen kontrolliert werden.
Verbindungen zum Immunsystem und neue Therapieideen
Über die Medikamentenresistenz hinaus verknüpft die Studie USP5 mit der Wechselwirkung des Glioblastoms mit dem Immunsystem. Die Analyse genomischer Daten deutete darauf hin, dass Veränderungen in USP5‑Spiegeln und in der Genkopienzahl das Gleichgewicht verschiedener Immunzellen rund um den Tumor verschieben, darunter cytotoxische T‑Zellen und regulatorische T‑Zellen. Frühere Arbeiten zeigten außerdem, dass USP5 PD‑L1 stabilisieren kann, ein Protein, das Tumoren nutzen, um angreifende T‑Zellen auszuschalten. Zusammen genommen deuten die Befunde darauf hin, dass USP5 Tumoren sowohl beim Überleben unter Chemotherapie als auch bei der Umgehung der Immunantwort helfen kann, was es zu einem besonders attraktiven Angriffspunkt für neue Medikamente macht.
Was das für die zukünftige Therapie von Hirnkrebs bedeutet
Kurz gesagt identifiziert diese Arbeit USP5 und USP8 als wichtige Leibwächter, die das Reparaturprotein MGMT schützen und Glioblastomzellen helfen, Temozolomid zu widerstehen. Durch das Ausschalten dieser Leibwächter konnten die Autorinnen und Autoren medikamentenresistente Zellen im Labor abtöten und MGMT‑Spiegel senken, selbst in Fällen, in denen MGMT‑basierte Resistenz nicht das einzige Problem war. Das weckt die Hoffnung, dass zukünftige Wirkstoffe gegen USP5 oder USP8, möglicherweise in Kombination mit bestehender Chemotherapie und immunbasierten Medikamenten, hartnäckige Hirntumoren wieder empfindlich machen und Patientinnen und Patienten mehr Lebenszeit verschaffen könnten.
Zitation: Bhardwaj, S., Sanjay, Sharma, D. et al. MGMT upregulation mediates Temozolomide resistance conferred USP5 dependency. Sci Rep 16, 6118 (2026). https://doi.org/10.1038/s41598-026-36379-4
Schlüsselwörter: Glioblastom, Temozolomid‑Resistenz, MGMT, USP5, Deubiquitinierende Enzyme