Clear Sky Science · de
Reziproke kooperative Gating‑Fusion von SqueezeNet und ShuffleNetV2 zur Brustkrebsdetektion in Histopathologie‑Bildern
Intelligentere Unterstützung bei der Brustkrebsdiagnose
Wenn ein Knoten in der Brust entdeckt wird, verlassen sich Ärzte oft auf hauchdünne Gewebeschnitte, die gefärbt und unter dem Mikroskop betrachtet werden, um zu entscheiden, ob die Zellen harmlos oder bösartig sind. Diese sorgfältige Begutachtung ist der diagnostische Goldstandard, doch sie ist langsam, arbeitsintensiv und kann von Facharzt zu Facharzt variieren. Die hier beschriebene Studie stellt ein Computerwerkzeug vor, das diese Mikroskopbilder mit künstlicher Intelligenz analysiert und darauf abzielt, Pathologen schnelle, konsistente und sehr genaue Zweitmeinungen zu liefern, während die Rechenkosten niedrig genug bleiben, um im klinischen Alltag einsetzbar zu sein.
Die Herausforderung beim Lesen von Gewebebildern
Brustkrebs ist eine der weltweit häufigsten Krebsarten und verursacht Hunderttausende Todesfälle pro Jahr. Der Schlüssel zu besseren Ergebnissen liegt in der frühen Erkennung und Charakterisierung von Tumoren, was nach wie vor größtenteils auf Histopathologie beruht: der Untersuchung gefärbter Gewebeschnitte im Mikroskop. Viele Gewebemuster sehen jedoch täuschend ähnlich aus. Normale und gutartige (nicht gefährliche) Proben können ähnliche Strukturen aufweisen, während frühe und invasive Stadien ineinander übergehen können. Hinzu kommen Unterschiede bei Färbungen, Beleuchtung und Bildkontrast zwischen Laboren, die dieselbe Erkrankung sehr unterschiedlich erscheinen lassen. Traditionelle Computerprogramme tun sich mit diesen Nuancen schwer, und viele moderne Deep‑Learning‑Systeme, die besser damit umgehen, sind so groß und energiehungrig, dass sie außerhalb führender Forschungszentren schwer einzusetzen sind.
Zwei kompakte Netzwerke im Team
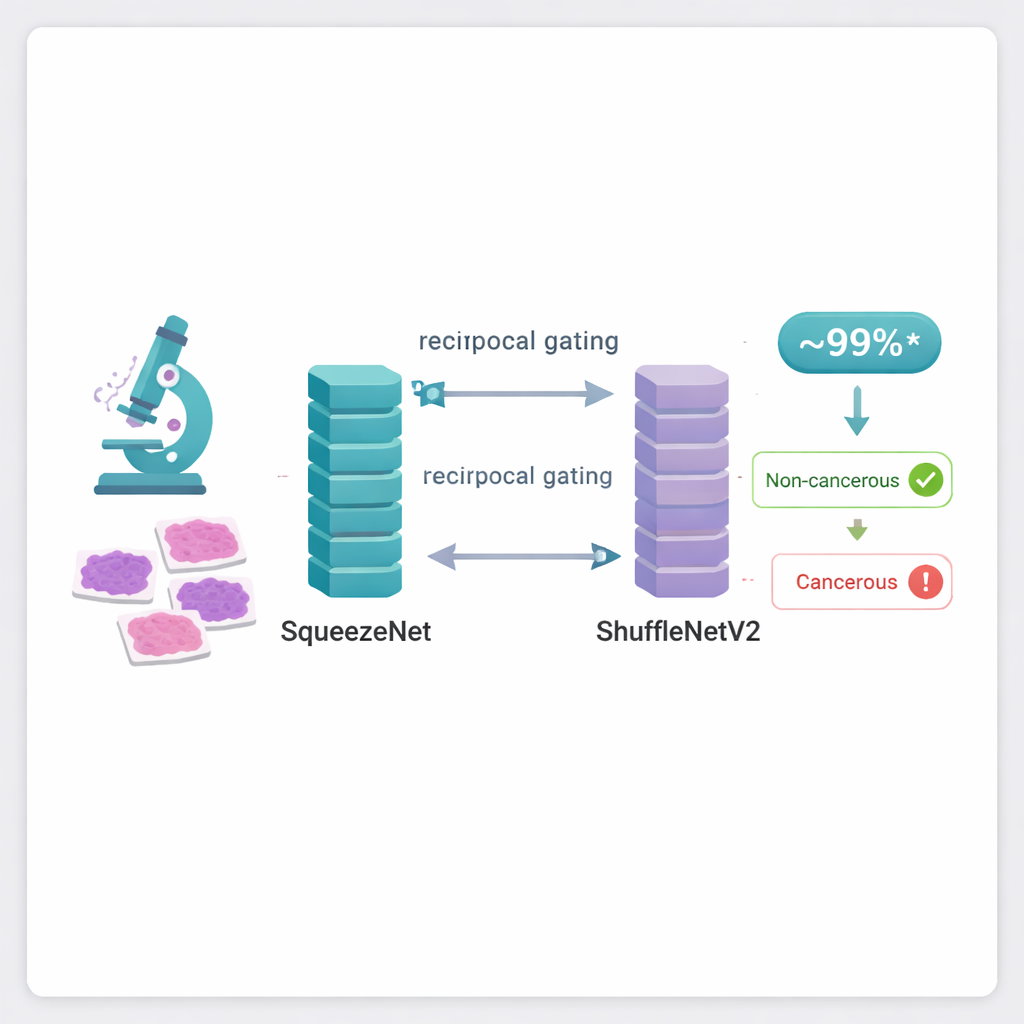
Um dieses Problem anzugehen, kombinieren die Autorinnen und Autoren zwei bestehende kompakte neuronale Netze, bekannt als SqueezeNet und ShuffleNetV2. Diese Modelle wurden ursprünglich dafür entwickelt, Alltagsobjekte in Fotos zu erkennen und dabei deutlich weniger Rechenaufwand zu benötigen als schwere Systeme wie Transformer oder sehr tiefe Netze. In dieser Arbeit werden sie daraufhin trainiert, Muster in Brustgewebebildern zu erkennen. Jedes Netzwerk betrachtet dasselbe Mikroskopbild und lernt, unterschiedliche visuelle Hinweise zu identifizieren—feine Variationen in Zellformen, Gewebetexturen und Farbanordnungen. Für sich genommen liefern beide Modelle gute Ergebnisse, doch die eigentliche Innovation liegt in der Art und Weise, wie ihre Stärken zusammengeführt werden.
Ein Gating‑Mechanismus, der Rauschen filtert
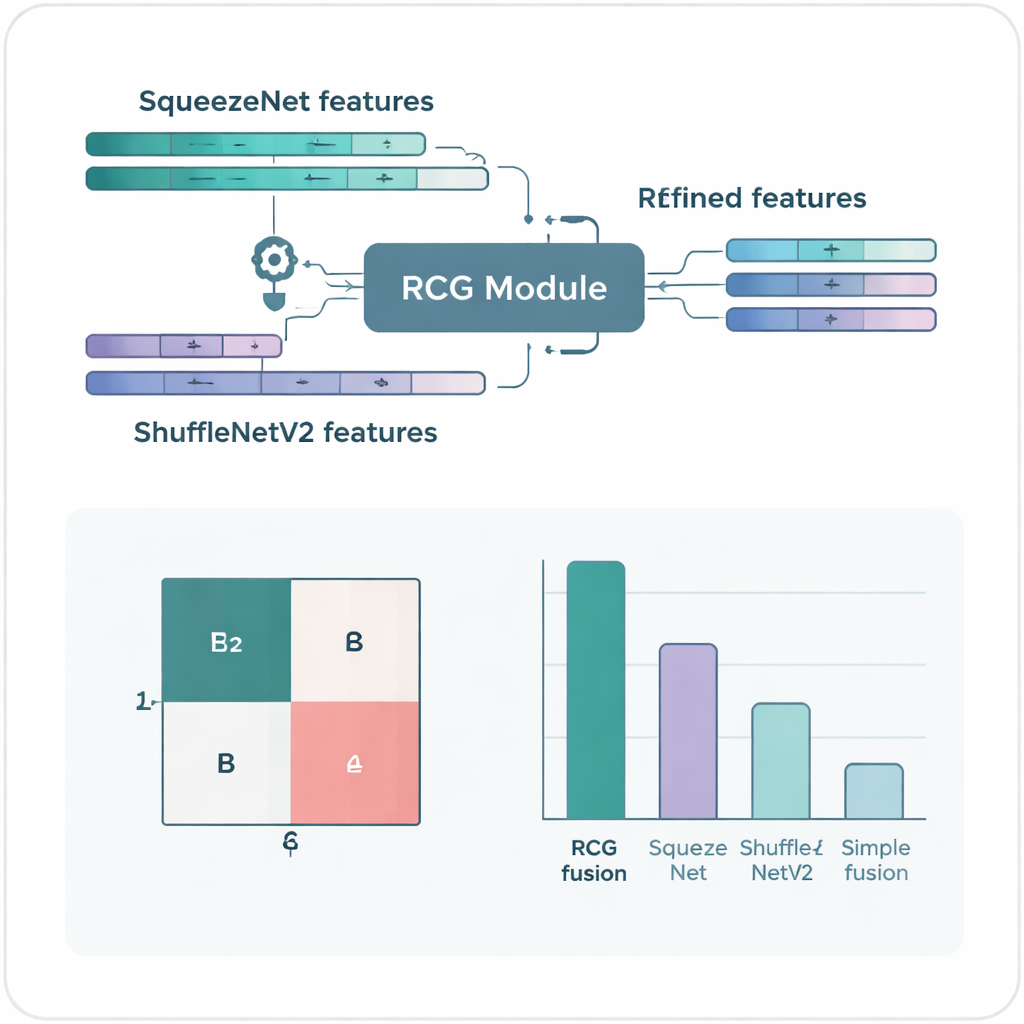
Die Kernidee der Studie ist ein neues „reziprokes kooperatives Gating“‑Modul, das den beiden Netzen erlaubt, miteinander zu kommunizieren und zu entscheiden, welche Teile ihrer internen Signale wirklich nützlich sind. Anstatt ihre Ausgaben einfach zu stapeln oder zu mitteln, misst das Gating‑System, wie viel Information jeder Kanal trägt und wie redundant sie zu dem ist, was das Partnernetz bereits gesehen hat. Kanäle, die neue, hilfreiche Details beitragen, werden verstärkt, während solche, die wiederholen oder Rauschen hinzufügen, abgeschwächt werden. Diese wechselseitige Anpassung erfolgt in beide Richtungen, sodass SqueezeNet die Merkmale von ShuffleNetV2 schärft und umgekehrt. Das Ergebnis ist eine einzige, fusionierte Repräsentation jedes Bildes, die reicher, sauberer und stärker auf die feinen Unterschiede fokussiert ist, die eine Diagnose von der anderen trennen.
Hohe Genauigkeit bei geringem Rechenaufwand
Bei Tests mit zwei weit verbreiteten Brustkrebs‑Bilddatenbanken, ICIAR‑2018 und BreakHis, zeigt das fusionierte System beeindruckende Leistungen. Bei der Vier‑Klassen‑Aufgabe—Unterscheidung von normalem Gewebe, gutartigen Veränderungen, frühem in situ Krebs und invasivem Krebs—klassifiziert es 97 Prozent der Bilder korrekt. Bei der vereinfachten Aufgabe, krebsartiges von nicht‑krebsartigem Gewebe zu trennen, steigt die Genauigkeit auf 99 Prozent bei ICIAR‑2018 und etwa 99,7 Prozent bei BreakHis. Diese Werte liegen über vielen komplexeren Methoden in der Literatur, obwohl das neue Modell relativ wenige Parameter und moderaten Rechenaufwand verwendet, was sich in schnelleren Vorhersagen und geringeren Hardware‑Anforderungen niederschlägt.
Was das für Patientinnen und Kliniken bedeutet
Vereinfacht gesagt haben die Autorinnen und Autoren einen schlanken, aber leistungsfähigen Assistenten entwickelt, der Mikroskopbilder von Brustgewebe durchsuchen und mit nahezu fachärztlicher Zuverlässigkeit kennzeichnen kann. Da das Design effizient ist, eignet es sich besser für reale Einsatzorte wie regionale Krankenhäuser oder Screening‑Zentren, die möglicherweise nicht über Hochleistungsserver verfügen. Das System ersetzt zwar nicht die Pathologinnen und Pathologen, kann jedoch verdächtige Bereiche hervorheben, konsistente Zweitmeinungen liefern und potenziell die Diagnostik beschleunigen. Die Arbeit weist auch auf einen breiteren Trend hin: Durch die clevere Kombination kleinerer KI‑Modelle und ihre kooperative Abstimmung statt Konkurrenz ist es möglich, Spitzengenauigkeit zu erreichen, ohne die hohen Kosten und die Komplexität, die praktische medizinische KI oft behindern, in Kauf nehmen zu müssen.
Zitation: Khati, B., Mukherjee, S., Sinitca, A. et al. Reciprocal cooperative gating fusion of SqueezeNet and ShuffleNetV2 for breast cancer detection in histopathology images. Sci Rep 16, 5904 (2026). https://doi.org/10.1038/s41598-026-36375-8
Schlüsselwörter: Brustkrebs, Histopathologie, medizinische Bildgebung KI, leichtgewichtiges CNN, computerassistierte Diagnose