Clear Sky Science · de
Die Genese von COPD entschlüsseln: ein Multi-Omics-Ansatz zur Identifizierung von Metaboliten und genetischen Verknüpfungen
Warum Lungenerkrankung und Körperchemie zusammenhängen
Die chronisch obstruktive Lungenerkrankung (COPD) ist vor allem als Raucherlunge bekannt, doch diese Studie zeigt, dass das, was in unserer Blutchimie geschieht, genauso wichtig sein kann wie das, was wir einatmen. Durch die Kombination großer genetischer Datensätze, detaillierter Messungen kleiner Moleküle im Blut und Laborversuchen an menschlichen Atemwegszellen enthüllen die Forschenden, wie gestörte Fettverarbeitung im Körper COPD antreiben könnte — und wie ein vertrautes Inhalationspräparat, Salbutamol, auf überraschende Weise helfen könnte.
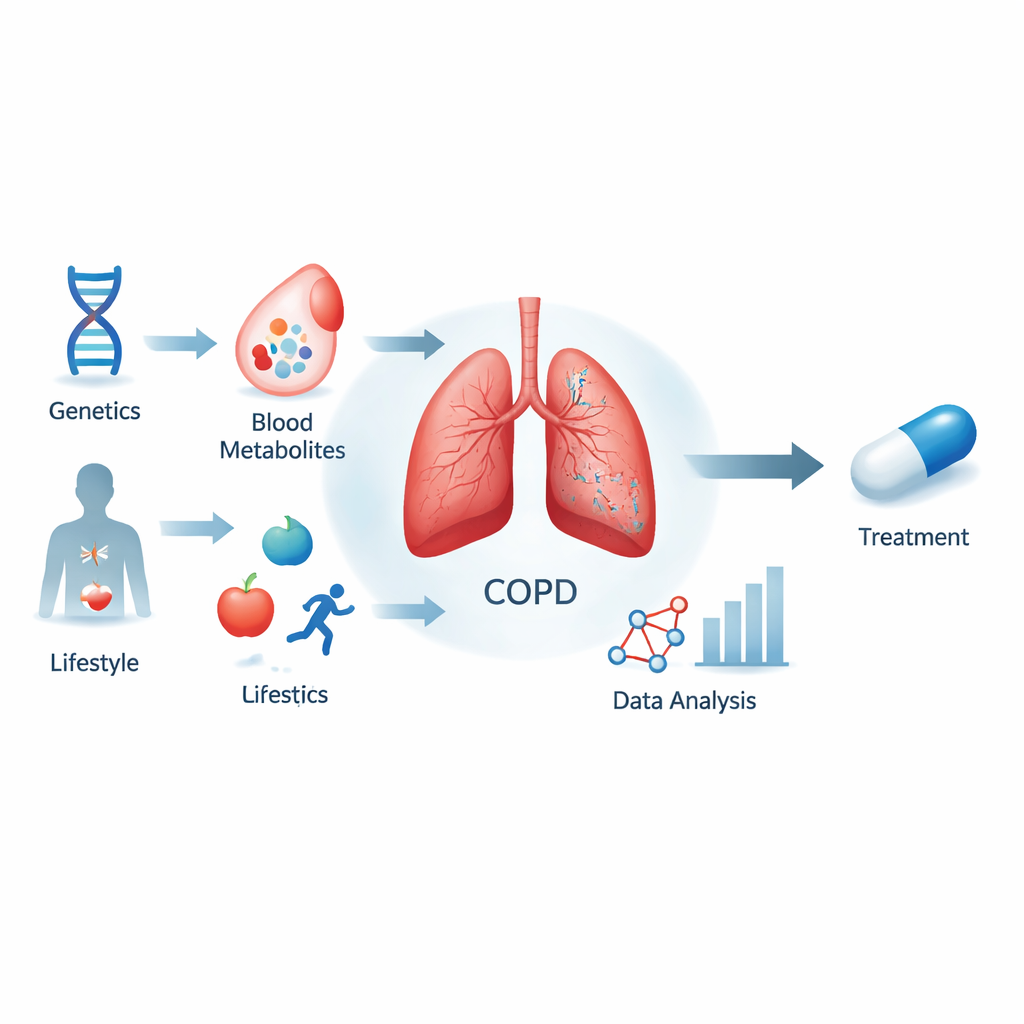
In die COPD hineinschauen: mehr als Rauchen
COPD betrifft weltweit Hunderte Millionen Menschen und wird voraussichtlich zur dritthäufigsten Todesursache. Obwohl Rauchen und Luftverschmutzung Hauptverursacher sind, erklären sie nicht vollständig, wer COPD entwickelt oder wie schnell sie voranschreitet. Das Team hinter dieser Arbeit fragte, ob bestimmte Blutmoleküle, sogenannte Metaboliten, nicht nur Schadensmarker sind, sondern aktive Mitspieler der Krankheit. Sie konzentrierten sich auf mehr als 1.400 in großen europäischen Studien gemessene Metaboliten und verbanden diese mit dem COPD-Risiko, wobei sie genetische Unterschiede von Menschen als eine Art natürliches Experiment nutzten.
Gene nutzen, um Ursache und Wirkung zu prüfen
Um über einfache Korrelationen hinauszukommen, nutzten die Forschenden eine Methode namens Mendelsche Randomisierung. Einfach gesagt verfolgten sie, ob Menschen, die mit Genvarianten geboren wurden, die bestimmte Metaboliten erhöhen oder senken, auch höhere oder niedrigere Chancen haben, COPD zu entwickeln. Dieser Ansatz hilft, echte Ursachen von Lebensstilfaktoren zu trennen, die das Bild verwässern können, etwa Kaffeekonsum oder Rauchen. Von 1.400 Metaboliten hoben sich sechs zunächst als mit COPD-Risiko assoziiert hervor. Ein zweiter, strengerer genetischer Test zeigte jedoch, dass nur zwei — Carnitin C14 und 3‑Hydroxyoleoylcarnitin — dasselbe zugrunde liegende genetische Signal wie COPD teilen. Beide stehen im Zusammenhang damit, wie der Körper langkettige Fettsäuren verarbeitet, was darauf hindeutet, dass Fettstoffwechsel, nicht nur Entzündung und Luftstrom, im Zentrum von COPD stehen könnte.
Von Molekülen zu zentralen Steuerungs-Schaltern
Sobald die zwei verlässlichen Metaboliten identifiziert waren, verfolgten die Forschenden die Stoffwechsel"straßen", auf denen sie unterwegs sind. Diese Wege liefen im Fettstoffwechsel zusammen und hoben eine Reihe von Enzymen hervor, die wie Ampeln wirken und steuern, wie viel Fett aufgebaut oder abgebaut wird — insbesondere die Enzyme ACACA und ACACB. Durch die Auswertung vorhandener Datenbanken zu Medikamenten und Proteininteraktionen entdeckte das Team, dass diese Enzyme im selben Netzwerk wie ADRB2 liegen, das Protein-Ziel von Salbutamol, einem gebräuchlichen Notfallinhalator bei COPD. Analysen von Lungengewebe von Patientinnen und Patienten zeigten, dass ACACA und ACACB hochreguliert waren, während ADRB2 herunterreguliert war, konsistent mit einem Zustand von Fettsäureüberladung in erkrankten Lungen.
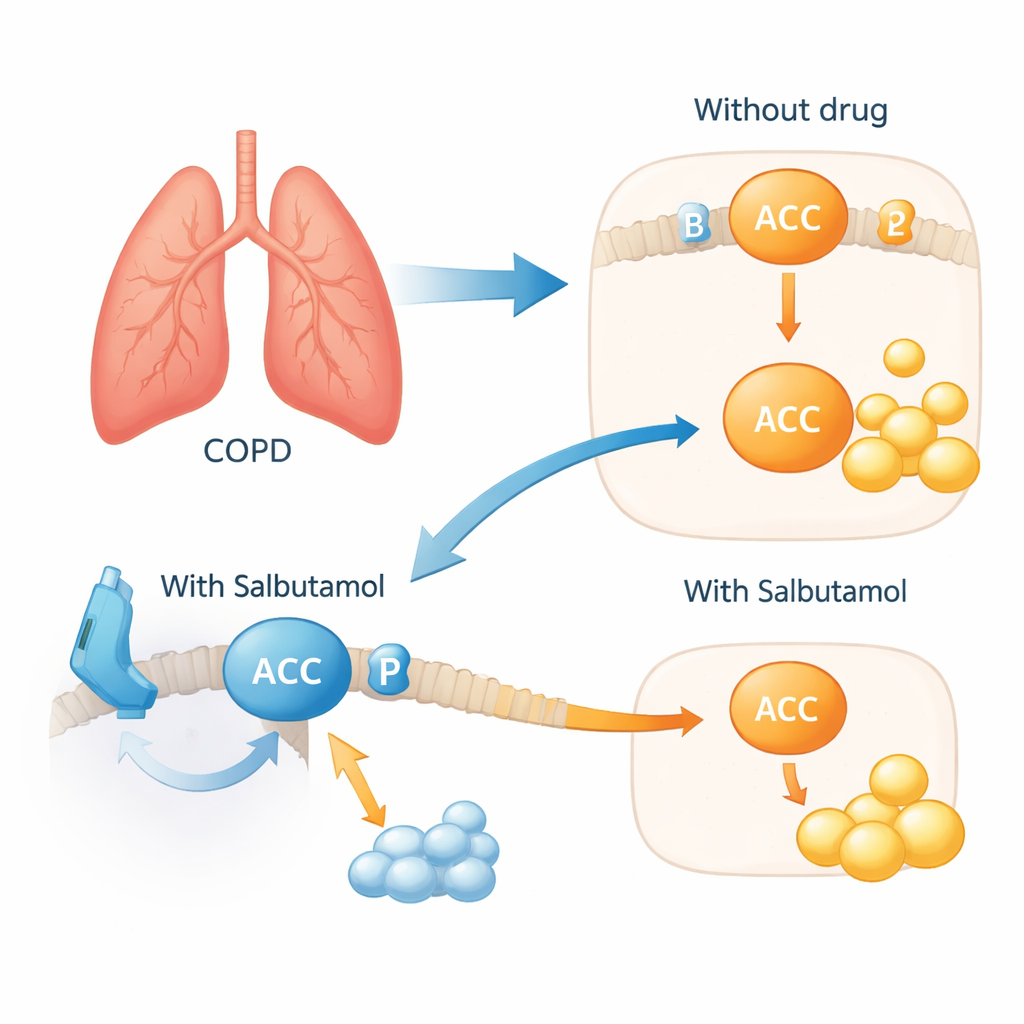
Ein Inhalator, der auch überbordendes Fett dämpft
Um zu prüfen, ob dieses Netzwerk in lebenden Zellen relevant ist, setzten die Wissenschaftler menschliche Bronchialzellen Zigarettenrauchextrakt aus, um COPD‑ähnlichen Stress zu simulieren. Die Zellen reagierten mit einer Hochregulierung von ACACA und ACACB und mit einer Reduktion einer schützenden chemischen Markierung auf ACACA, die normalerweise die Fettproduktion bremst. Wurde Salbutamol zugegeben, kehrte dieses schädliche Muster um: Die schützende Markierung auf ACACA wurde wiederhergestellt und Anzeichen übermäßiger Fettsynthese nahmen ab. Einfach ausgedrückt schien das Medikament die Fettaufbau-Maschinerie innerhalb der Atemwegszellen zu bremsen, vermittelt über den ADRB2‑"Schalter" an der Zelloberfläche. Genetische Analysen mit Blick auf Lebensstilfaktoren stützten zusätzlich die Idee, dass die beiden Schlüsselmoleküle mit zugrundeliegender Biologie verknüpft sind und nicht nur mit Gewohnheiten wie Kaffeekonsum, die mehrere andere Kandidaten erklärten.
Was das für Patienten und künftige Therapien bedeutet
Die Kernbotschaft für Nicht‑Fachleute lautet, dass COPD teilweise durch einen metabolischen Stau in der Fettverarbeitung von Lungenzellen angetrieben sein könnte und dass ein weit verbreiteter Bronchodilatator auch stillschweigend dazu beitragen kann, diesen Stau zu beseitigen. Carnitin C14 und 3‑Hydroxyoleoylcarnitin treten als starke Blutmarker hervor, die eines Tages helfen könnten, Menschen mit erhöhtem Risiko zu identifizieren oder den Krankheitsverlauf zu überwachen. Die Enzyme ACACA und ACACB, die an Schlüsselknoten im Fettstoffwechsel sitzen und mit dem Salbutamol‑Ziel ADRB2 verknüpft sind, bieten neue Ansatzpunkte für die Medikamentenentwicklung. Obwohl weitere Arbeiten in diversen Populationen und vertiefende metabolische Studien nötig sind, eröffnet dieser Multi‑Omics‑Ansatz einen Weg zu COPD‑Behandlungen, die mehr tun als nur die Atemwege zu weiten — sie könnten auch die Nutzung von Brennstoffen in der Lunge wieder gesünder gestalten.
Zitation: Zeng, M., Liu, J., Cao, X. et al. Unraveling COPD pathogenesis: a multi-omics approach to identify metabolites and genetic links. Sci Rep 16, 6013 (2026). https://doi.org/10.1038/s41598-026-36368-7
Schlüsselwörter: COPD, Fettstoffwechsel, Salbutamol, Carnitin-Biomarker, Multi-Omics