Clear Sky Science · de
Die Rolle von MNX1-vermittelten Histonmodifikationen und der PBX-Genfamilie bei MNX1-induzierter Leukämogenese
Warum ein winziger genetischer Fehler für kranke Kinder so wichtig ist
Die meisten kindlichen Leukämien sind heute behandelbar, doch eine seltene Form, die Säuglingsakute myeloische Leukämie (AML), bleibt besonders tödlich. Viele dieser Säuglinge teilen denselben genetischen Unfall: Zwei Chromosomen tauschen Stücke aus, wodurch ein ruhiges Entwicklungsgen namens MNX1 zu einem überaktiven Treiber wird. Diese Studie stellt eine einfache, aber entscheidende Frage: Wenn MNX1 hochreguliert ist, was bewirkt es in jungen Blutzellen, um sie in Richtung Krebs zu treiben — und lässt sich dieser Prozess unterbrechen?
Von normalen Babyblutzellen zum unkontrollierten Wachstum
Leukämie entsteht, wenn unreife Blutzellen aufhören zu reifen und sich stattdessen unkontrolliert vermehren. Bei Säuglingen mit der t(7;12)-Chromosomenumsortierung wird MNX1 in sehr frühen blutbildenden Zellen des fetalen Leber- und Knochenmarkstils ungewöhnlich aktiv. Die Forschenden entwickelten ein Mausmodell, das diese Situation nachahmt: Sie schalteten humanes MNX1 in fetalen Blutstammzellen an, transplantierten diese in Mäuse und beobachteten, wie die Tiere von einem präleukämischen Zustand zur voll entwickelten Leukämie übergingen. Durch den Vergleich der Zellen in diesen verschiedenen Stadien mit gesunden Kontrollen konnten sie nachvollziehen, wie MNX1 im Lauf der Zeit die internen Kontrollsysteme der Zelle umprogrammiert.
Wie MNX1 das Betriebsbuch der Zelle umschreibt
MNX1 ist ein Transkriptionsfaktor, ein Protein, das auf DNA sitzt und steuert, welche Gene an- oder abgeschaltet werden. Das Team kombinierte mehrere leistungsfähige Methoden — Massenspektrometrie, RNA-Sequenzierung und Chromatinprofilierung — um zu sehen, mit welchen Partnern MNX1 zusammenarbeitet und welche Gene es verändert. Sie stellten fest, dass MNX1 mit Enzymen kooperiert, die chemische Markierungen an Histonproteinen anbringen, den spulenähnlichen Strukturen, um die DNA gewickelt ist. Insbesondere verstärkt MNX1 ein "AN"-Mark namens H3K4me3 und verringert ein "AUS"-Mark namens H3K27me3 an bestimmten Stellen im Genom. Diese Veränderungen lockern die lokale DNA-Struktur und erleichtern es wichtigen wachstumsbezogenen Genen, aktiviert zu werden.
Ein kurzer, anschubsender Eingriff an einem kritischen Kontrollgen
Unter den vielen betroffenen Genen stach eines heraus: Pbx1, Teil der PBX-Familie von DNA-bindenden Proteinen, die seit langem mit Leukämie in Verbindung gebracht werden. Die Studie zeigt, dass MNX1 direkt an die Kontrollregion des Pbx1-Gens bindet, das AN-Mark dort erhöht und das AUS-Mark entfernt. Dies startet die Pbx1-Expression sehr früh, als die Zellen noch präleukämisch sind. Überraschenderweise ist MNX1 später — sobald die Leukämie etabliert ist — an dieser Stelle nicht mehr stark gebunden, doch das Pbx1-Gen bleibt weiter eingeschaltet und seine Histonmarkierungen verbleiben in der wachstumsfördernden Konfiguration. Das deutet auf einen "Hit-and-Run"-Mechanismus hin: MNX1 besucht kurz wichtige Chromatinregionen, hinterlässt dauerhafte epigenetische Markierungen und kann dann verschwinden, während der veränderte Zustand die Krankheit weiter antreibt.
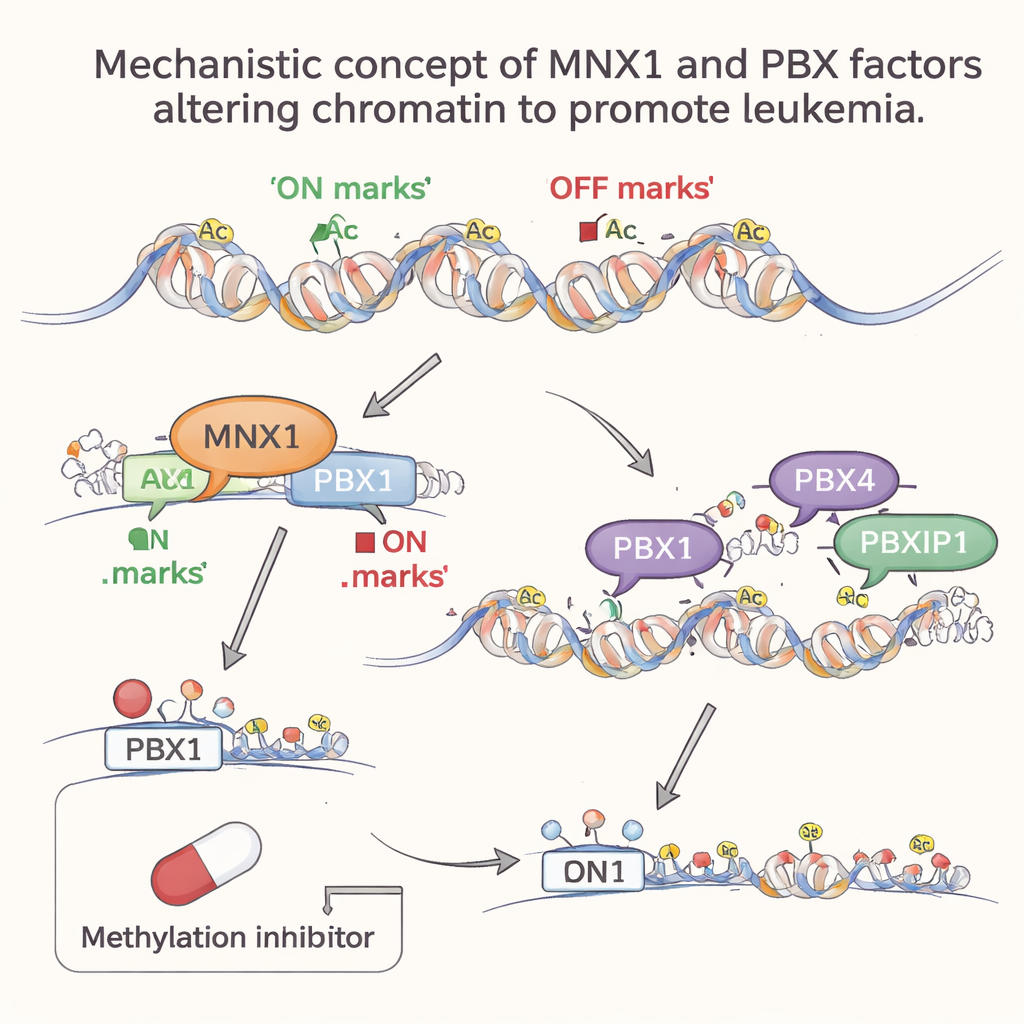
Spätere Helfer treten hinzu, um den Krebszustand zu verfestigen
Mit dem Fortschreiten der Leukämie werden andere PBX-Familienmitglieder, PBX4 und PBXIP1, aktiver, jedoch erst in diesem späteren Stadium. Genomweite Analysen zeigten, dass ihre bevorzugten DNA-Motive stark in Regionen offenen, aktiven Chromatins angereichert sind, die infolge der MNX1-Aktivität umgestaltet wurden. Anders gesagt: MNX1 formt zuerst die Chromatinlandschaft um und schaltet Pbx1 an; anschließend besetzen PBX4 und PBXIP1 diese neu zugänglichen Regionen, um abnorme Genprogramme zu verstärken, die Zellteilung fördern, die normale Blutentwicklung blockieren und die DNA-Reparatur beeinträchtigen. Diese schrittweise Beteiligung deutet auf eine Arbeitsteilung hin: PBX1 wirkt als frühe, MNX1-abhängige Schaltstelle, während PBX4 und PBXIP1 helfen, das leukämische Programm aufrechtzuerhalten.
Die chemischen Markierungen, die Leukämie antreiben, blockieren
Da MNX1 über Enzyme wirkt, die Methylgruppen an Histone anbringen, testete das Team, ob ein breiter Methyltransferase-Inhibitor, Sinefungin, diese Kette von Ereignissen stören kann. In präleukämischen fetalen Blutzellen, die MNX1 exprimieren, reduzierte Sinefungin die Pbx1-Spiegel stark, was mit einer Blockade der promoter-spezifischen Methylierung übereinstimmt, auf die MNX1 angewiesen ist. Im Gegensatz dazu änderten sich PBX4- und PBXIP1-Spiegel kaum, was zu ihrer späteren, indirekten Aktivierung im Krankheitsverlauf passt. Zusammengenommen liefern diese Ergebnisse ein überzeugendes Argument dafür, dass die Säuglings-AML mit t(7;12) nicht nur von einem defekten Gen getrieben wird, sondern von einer Kaskade dauerhafter epigenetischer Veränderungen, die MNX1 in Gang setzt.
Was das für zukünftige Therapien bedeutet
Für Nichtfachleute lautet die Kernbotschaft: Diese Studie kartiert eine Kettenreaktion — ein überaktives MNX1-Gen verändert die chemischen Markierungen an DNA-verpackenden Proteinen, schaltet PBX1 früh an und ebnet den Weg für PBX4 und PBXIP1, Zellen in einen leukämischen Zustand zu verriegeln. Weil diese Schritte von spezifischen Histonmethylierungsmustern abhängen, bieten sie klare, testbare Ziele für Medikamente, die in diese Markierungen eingreifen. Langfristig könnten Therapien, die auf die MNX1–PBX-Achse oder auf die Enzyme abzielen, die diese epigenetischen Tags anbringen, dazu beitragen, die fehlerhaften Anweisungen, die diese aggressive Leukämie bei Säuglingen antreiben, auszuschalten und die Chancen auf dauerhafte Heilungen zu verbessern.
Zitation: Malmhäll-Bah, E., Östlund, A., Nilsson, T. et al. Role of MNX1-mediated histone modifications and PBX gene family in MNX1-induced leukemogenesis. Sci Rep 16, 2593 (2026). https://doi.org/10.1038/s41598-026-36367-8
Schlüsselwörter: Säuglingsakute myeloische Leukämie, MNX1, PBX1 PBX4 PBXIP1, epigenetische Histonmethylierung, t(7;12)-Chromosomentranslokation