Clear Sky Science · de
Translationale Bewertung von BUB1B als Biomarker für Präzisionsmedizin beim hepatozellulären Karzinom
Warum ein Gen der Zellteilung für Leberkrebs wichtig ist
Die meisten Menschen denken bei Krebs an sichtbare Tumoren in Bildern, doch tief in diesen Wucherungen arbeiten mikroskopische Steuermechanismen, die entscheiden, wie und wann Zellen sich teilen. Diese Studie konzentriert sich auf einen solchen Schalter, ein Gen namens BUB1B, und zeigt, wie es Ärzten helfen könnte vorherzusagen, welche Leberkrebspatienten eine schlechtere Prognose haben, wer auf bestimmte Medikamente reagieren könnte und warum manche Tumoren das Immunsystem überlisten. Indem ein grundlegender Zellzyklusregler zu einem „Armaturenbrett“ für das Verhalten von Leberkrebs gemacht wird, weist die Arbeit auf möglichere Wege zu präziseren und individualisierten Behandlungen hin.
Eine häufige Leberkrebserkrankung braucht bessere Wegweiser
Das hepatozelluläre Karzinom, die häufigste Form des primären Leberkrebses, wird oft erst spät entdeckt, wenn Symptome auftreten und die Behandlungsmöglichkeiten begrenzt sind. Bestehende Blut- und Gewebsmarker, wie Alpha-Fetoprotein oder Ki-67, sind unvollkommen: Sie erfassen Erkrankungen nicht zuverlässig im Frühstadium und leiten keine maßgeschneiderten Therapien. Die Autoren suchten daher nach einem anderen Markertyp — einem, der die innere Verdrahtung der Krebszellen widerspiegelt und nicht nur deren bloße Anwesenheit. Sie interessierten sich für BUB1B, ein Protein, das dafür sorgt, dass Chromosomen bei der Zellteilung korrekt verteilt werden. Fällt dieses System aus, häufen sich genetische Fehler an, die aggressive Tumoren antreiben können.
BUB1B in verschiedenen Krebsarten und bei realen Patienten verfolgen
Mithilfe großer öffentlicher Krebsdatenbanken, einschließlich The Cancer Genome Atlas, untersuchten die Forschenden zunächst die Aktivität von BUB1B in vielen Tumortypen. Sie fanden, dass es in 19 verschiedenen Krebsarten stärker hochreguliert war, mit besonders ausgeprägter Überaktivität in Lebertumoren im Vergleich zum umgebenden gesunden Gewebe. Patientinnen und Patienten, deren Leberkrebserkrankungen höhere BUB1B-Werte aufwiesen, lebten tendenziell kürzer, selbst nach Berücksichtigung des Erkrankungsstadiums — sodass BUB1B ein unabhängiges Warnsignal darstellt. Eine eingehende Auswertung von 50 Leberkrebspatienten aus dem eigenen Krankenhaus bestätigte dieses Muster: Die Tumoren zeigten unter dem Mikroskop intensive BUB1B-Färbung, vor allem im Zellplasma, und hohe Werte korrelierten mit größeren Tumoren, fortgeschrittenerem Stadium und schlechterem Überleben.
Genetisches Chaos, Medikamentenansprechen und ein verwirrtes Immunsystem
Hohe BUB1B-Werte signalisierten nicht nur Gefährlichkeit; sie standen auch im Zusammenhang mit tiefergehender Instabilität in der DNA des Tumors. Tumoren mit verstärktem BUB1B zeigten mehr Hinweise auf defekte DNA-Reparatur und subtile Formen von Mikrosatelliteninstabilität — Kennzeichen genomischer Unordnung, die einerseits eine schnelle Evolution fördern und andererseits beeinflussen können, wie Tumore auf Therapien reagieren. Computermodelle, die Genmuster mit Medikamententests verknüpfen, deuteten darauf hin, dass BUB1B-auffällige Leberkarzinome empfindlicher gegenüber bestimmten Wirkstoffen sein könnten, darunter das zielgerichtete Medikament Sorafenib und klassische Chemotherapeutika wie Paclitaxel und Doxorubicin, während sie vergleichsweise resistent gegenüber Medikamenten waren, die den EGFR-Signalweg anvisieren. Gleichzeitig enthielten diese Tumoren viele Immunzellen, insbesondere T-Zellen, erzielten aber hohe Werte bei Messungen von Immunfunktionsstörung und -ausschluss — das heißt, das Immunsystem war zwar präsent, aber effektiv ausgesperrt und weniger wahrscheinlich auf übliche Immuntherapien zu reagieren, die PD-1 oder PD-L1 blockieren.
Wie BUB1B Wachstumsignale innerhalb der Krebszellen antreibt
Um über statistische Zusammenhänge hinauszugehen, testete das Team, was geschieht, wenn BUB1B chemisch in Leberkrebszellen im Labor blockiert wird. Die Hemmung dieses Gens dämpfte eine ganze Kaskade von Wachstumsignalen, die häufig unter dem Begriff MAPK-Wege zusammengefasst werden. Schlüsselakteure auf mehreren Ebenen — darunter RAS, bestimmte RAF-Familienmitglieder, ERK sowie mehrere p38- und verwandte Kinasen — wurden deutlich reduziert. Da diese Signalwege wie eine Staffel fungieren, die den Krebszellen sagt, weiter zu teilen und Stress zu widerstehen, deutet ihre Abschwächung darauf hin, dass BUB1B nicht nur ein passiver Marker ist, sondern aktiv zur Aufrechterhaltung der inneren Verdrahtung des Tumors beiträgt. Einige Komponenten zeigten unerwartete Rückkopplungsreaktionen, was auf eingebaute Feedback-Schleifen hindeutet, doch insgesamt war die Wirkung eine breite Abschwächung pro‑wachstumsfördernder Signale.
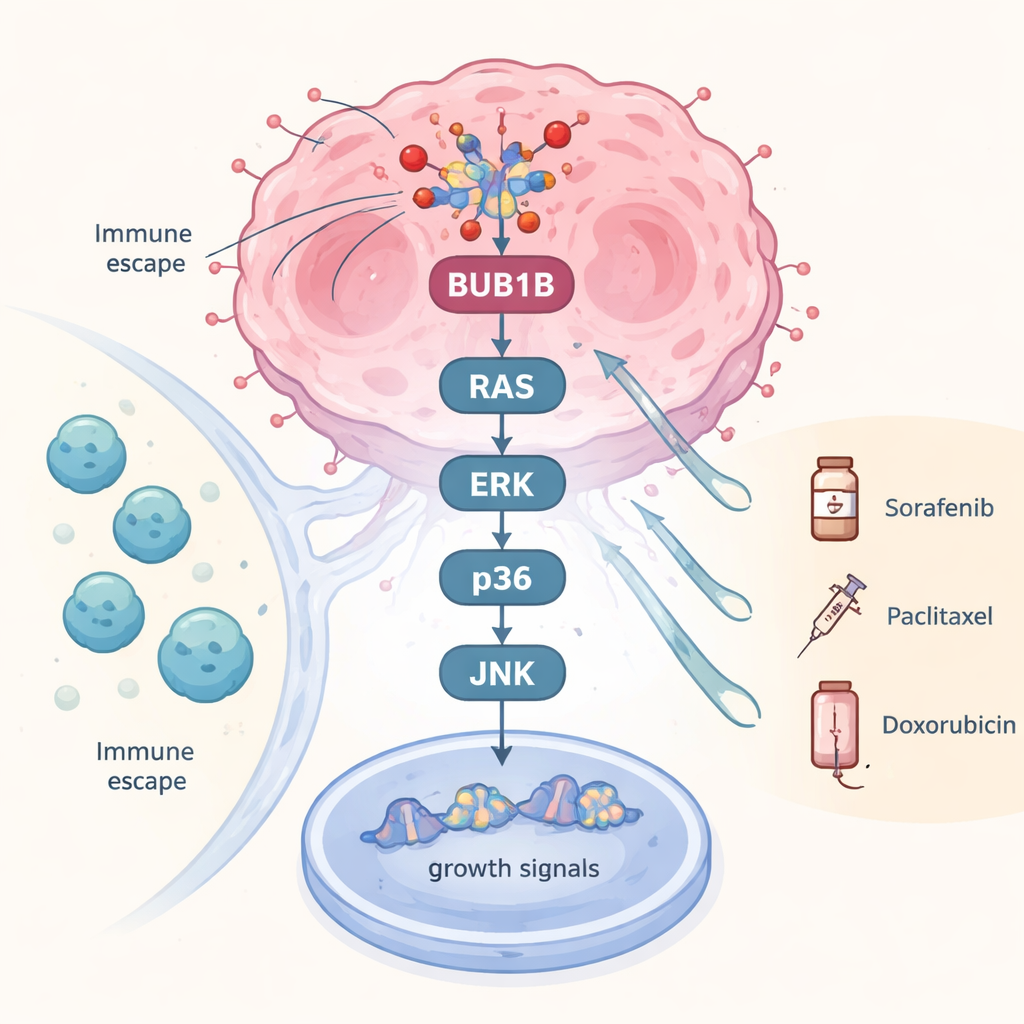
Was das für Patienten und die künftige Versorgung bedeutet
Für Nicht-Spezialisten lautet die Quintessenz: Ein einzelnes Zellteilungsgen, BUB1B, scheint an der Schnittstelle dreier entscheidender Merkmale von Leberkrebs zu stehen — wie instabil die Tumor-DNA ist, wie der Tumor mit dem Immunsystem kommuniziert und wie er auf mehrere wichtige Medikamente reagiert. Die Messung von BUB1B in Tumorproben könnte Ärzten helfen, Patienten in Risikogruppen einzuteilen, das Überleben besser abzuschätzen und Behandlungen auszuwählen, die die Schwächen des Tumors ausnutzen — zugleich aber erkennen, wann eine Standard-Immuntherapie voraussichtlich nicht wirkt. Da Lebertumoren auf BUB1B angewiesen zu sein scheinen, um ihre Wachstums- und Stressantwortsignale aufrechtzuerhalten, könnten Wirkstoffe, die dieses Protein gezielt angreifen, allein oder in Kombination mit bestehenden Therapien, neue Wege zu präziseren und wirksameren Behandlungen des hepatozellulären Karzinoms eröffnen.
Zitation: Sun, Cy., Yu, X., Deng, Lq. et al. Translational evaluation of BUB1B as a precision medicine biomarker for hepatocellular carcinoma. Sci Rep 16, 5301 (2026). https://doi.org/10.1038/s41598-026-36364-x
Schlüsselwörter: hepatozelluläres Karzinom, BUB1B, Biomarker, MAPK-Signalübertragung, Präzisionsonkologie