Clear Sky Science · de
Kompromiss zwischen kanonischen und ungewöhnlichen Rekombinationsstellen fördert Vielfalt und Stabilität von Genkassettensystemen mobiler Integrone
Wie Bakterien ihre Abwehr umsortieren
Bakterien in Krankenhäusern sind ständig einer Flut von Antibiotika ausgesetzt, doch viele überleben und verbreiten sich. Ein wesentlicher Grund dafür ist ein genetisches Gerät namens Integron, das Bakterien ermöglicht, Resistenzgene schnell zu sammeln und neu anzuordnen. Diese Arbeit untersucht eine ungewöhnliche Funktionsweise dieser Systeme und zeigt, wie Bakterien zwei Bedürfnisse zugleich ausbalancieren: ihre Resistenzgene stabil genug zu halten, um sich auf sie verlassen zu können, und zugleich flexibel genug, um sich an neue Wirkstoffe anzupassen.
Ein genetisches Werkzeug auf Abruf
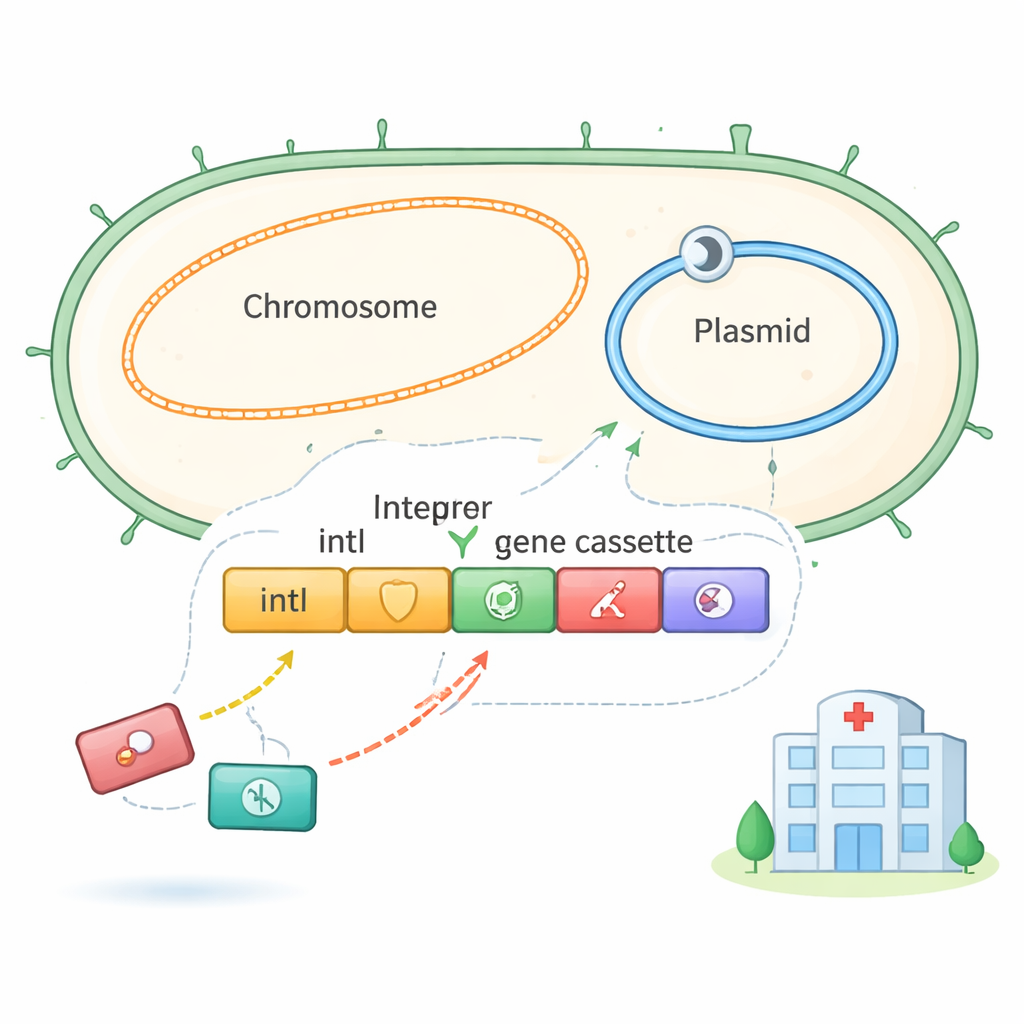
Viele gramnegative Bakterien tragen Integrone, kleine genetische Plattformen, die wie Dockingstationen für „Genkassetten“ funktionieren. Jede Kassette enthält typischerweise ein einzelnes Gen, oft für Antibiotikaresistenz, zusammen mit einem kurzen DNA-Tag, der dem Integron-Enzym IntI sagt, wo geschnitten und eingefügt werden soll. Zwei Haupttag-Typen sind bekannt: attI, meist am Anfang des Integrons, und attC, das Standardkassetten markiert. Wenn sich die Bedingungen ändern, etwa unter Antibiotikastress, kann IntI diese Kassetten umsortieren — neue hinzufügen, andere entfernen oder ihre Reihenfolge verändern — wodurch das Bakterium seine Abwehr schnell anpassen kann.
Seltsame Tags mit wichtiger Rolle
Über die gut untersuchten attI- und attC-Tags hinaus fokussierten die Autorinnen und Autoren auf eigentümliche, teilweise deletierte Versionen von attI, genannt ΔattI-Stellen. Diese finden sich in „ungewöhnlichen“ Genkassetten, in denen das übliche attC-Tag durch ein Fragment von attI ersetzt wurde. Beim Durchsuchen von über 1.700 kompletten Integronen aus öffentlichen Datenbanken entdeckte das Team acht verschiedene ΔattI-Typen in Klasse-1- und Klasse-2-Integronen, überwiegend in krankenhausassoziierten Bakterien. Sie identifizierten 26 ungewöhnliche ΔattI-artige Kassetten, von denen viele Resistenz gegen mehrere Antibiotikafamilien vermitteln. Eine davon, die das blaOXA-10-Resistenzgen trägt, war besonders häufig — ein Hinweis darauf, dass selbst diese ungewöhnlich aussehenden Kassetten weit verbreitet und klinisch relevant sind.
Ungewöhnliche Kassetten im Funktionstest
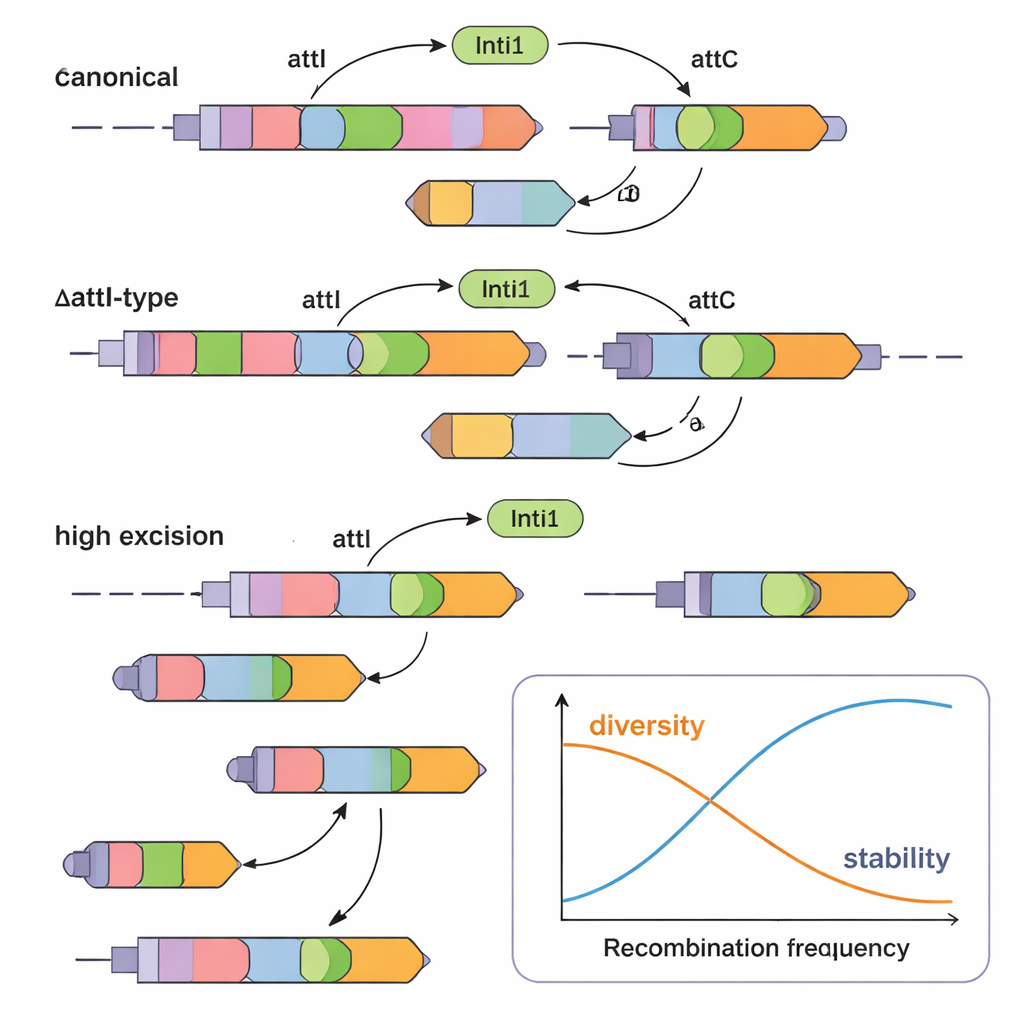
Um zu prüfen, ob diese ΔattI-artigen Kassetten tatsächlich funktionieren, rekonstruierten die Forschenden mehrere Beispiele im Labor. Sie setzten sie auf Plasmide in E. coli zusammen mit dem Enzym IntI1 und maßen, wie oft Kassetten herausgeschnitten (Exzision) oder in eine attI-Stelle eingefügt wurden. Sie verglichen kanonische Konstrukte (mit einem normalen attC an einem Ende) mit ungewöhnlichen, bei denen das downstream-liegende attC durch ein kurzes oder langes ΔattI-Fragment ersetzt war. Das überraschende Ergebnis: Viele ΔattI-artige Kassetten waren voll funktionsfähig. Manche wurden weniger effizient exzidiert als klassische Kassetten, aber genauso gut eingesetzt, während andere, insbesondere solche mit einem bestimmten ΔattI2-Fragment, mit Raten exzidiert wurden, die den Standardkassetten ähnelten. Das zeigt, dass selbst teilweise deletierte Rekombinationstags weiterhin robuste Substrate für die Integron-Maschinerie darstellen können.
Warum duplizierte Gene selten bleiben
Die Autoren gingen auch einem weiteren Rätsel nach: Warum sieht man selten dieselbe Resistenzkassette direkt hintereinander in Integronen, obwohl dies die Resistenz durch höhere Genkopienzahl steigern könnte. Sie konstruierten künstliche Kassetten, flankiert von identischen Rekombinationsstellen auf beiden Seiten — entweder zwei attI1-Stellen oder zwei identische attC-Stellen um dasselbe Gen. In diesen Konstruktionen schnitt IntI1 sie mit auffallender Effizienz heraus, oft über 97 % und bis zu 100 %. Anders gesagt: Sobald eine perfekte Tandemkassette entsteht, wird sie fast sofort wieder entfernt. Diese eingebaute Instabilität erklärt, warum duplizierte Kassetten in der Natur selten sind, es sei denn, starker Antibiotikadruck begünstigt aktiv ihre Erhaltung.
Ein eingebautes Gleichgewicht zwischen Wandel und Kontrolle
In der Gesamtschau zeigen die Ergebnisse ein feines Gleichgewicht. Integrone nutzen eine Mischung aus attI-, attC- und ΔattI-Stellen, um die Beweglichkeit verschiedener Kassetten zu regulieren. Kanonische Anordnungen unterstützen effizientes Umsortieren, während ΔattI-artige Kassetten und der rasche Verlust perfekter Duplikate verhindern, dass sich das Array mit Kopien desselben Gens füllt. Dieser Kompromiss erlaubt es Bakterien, eine vielfältige Auswahl an Resistenzoptionen zu erhalten und zugleich zu vermeiden, dass Konfigurationen zu instabil oder redundant werden. Für nichtfachliche Beobachter lautet die Kernbotschaft: Bakterien sammeln Resistenzgene nicht nur passiv; sie nutzen ein ausgeklügeltes DNA-System, das aktiv steuert, welche Gene behalten, welche kopiert und welche verworfen werden — ein Mechanismus, der ihnen hilft, in der antibiotikareichen Umgebung moderner Krankenhäuser zu gedeihen.
Zitation: Gonzales Machuca, A., Molina, M.C., Álvarez, V.E. et al. Trade-off between canonical and unusual recombination sites promotes diversity and stability of gene cassette arrays of mobile integrons. Sci Rep 16, 6133 (2026). https://doi.org/10.1038/s41598-026-36353-0
Schlüsselwörter: Antibiotikaresistenz, Integrone, Genkassetten, bakterielle Evolution, Krankenhausinfektionen