Clear Sky Science · de
Herunterregulierung von CDC25C unterdrückt HCC-Wachstum durch mitochondrialen Stress-induzierten Autophagie und Apoptose
Warum diese Leberkrebsstudie wichtig ist
Leberkrebs gehört zu den tödlichsten Krebsarten weltweit, und viele Patientinnen und Patienten werden zu spät diagnostiziert, als dass Operationen oder Standardtherapien gut wirken würden. Diese Studie untersucht einen einzelnen zellulären „Schalter“, ein Protein namens CDC25C, das offenbar das Wachstum von Leberkrebs vorantreibt, während es für gesunde Leberzellen weniger kritisch ist. Durch das Herunterregulieren dieses Schalters stellten die Forschenden fest, dass sie Krebszellen durch Stress der Mitochondrien letztlich über die zelleigenen Reinigungs- und Selbstzerstörungssysteme töten können — ein Hinweis auf eine vielversprechende und selektivere Behandlungsstrategie.
Ein Wachstumsschalter in Lebertumoren
Jede Zelle muss entscheiden, wann sie sich teilt und wann sie stoppt. CDC25C ist eines der Schlüsselproteine, das Zellen durch den Zellteilungszyklus treibt. Bei Leberkrebs steht dieser Schalter oft auf „ein“ und fördert so das Tumorwachstum und die Ausbreitung. Das Team verwendete Maus-Leberkrebszellen und normale Maus-Leberzellen sowie tumorbefallene Mäuse, um CDC25C künstlich zu reduzieren. Sie bestätigten mithilfe gängiger genetischer und proteinbasierter Tests, dass CDC25C in der Versuchsgruppe im Vergleich zu Kontrollen deutlich vermindert war und schufen so ein belastbares Modell, um zu untersuchen, was passiert, wenn dieser Wachstumsschalter heruntergeregelt wird.
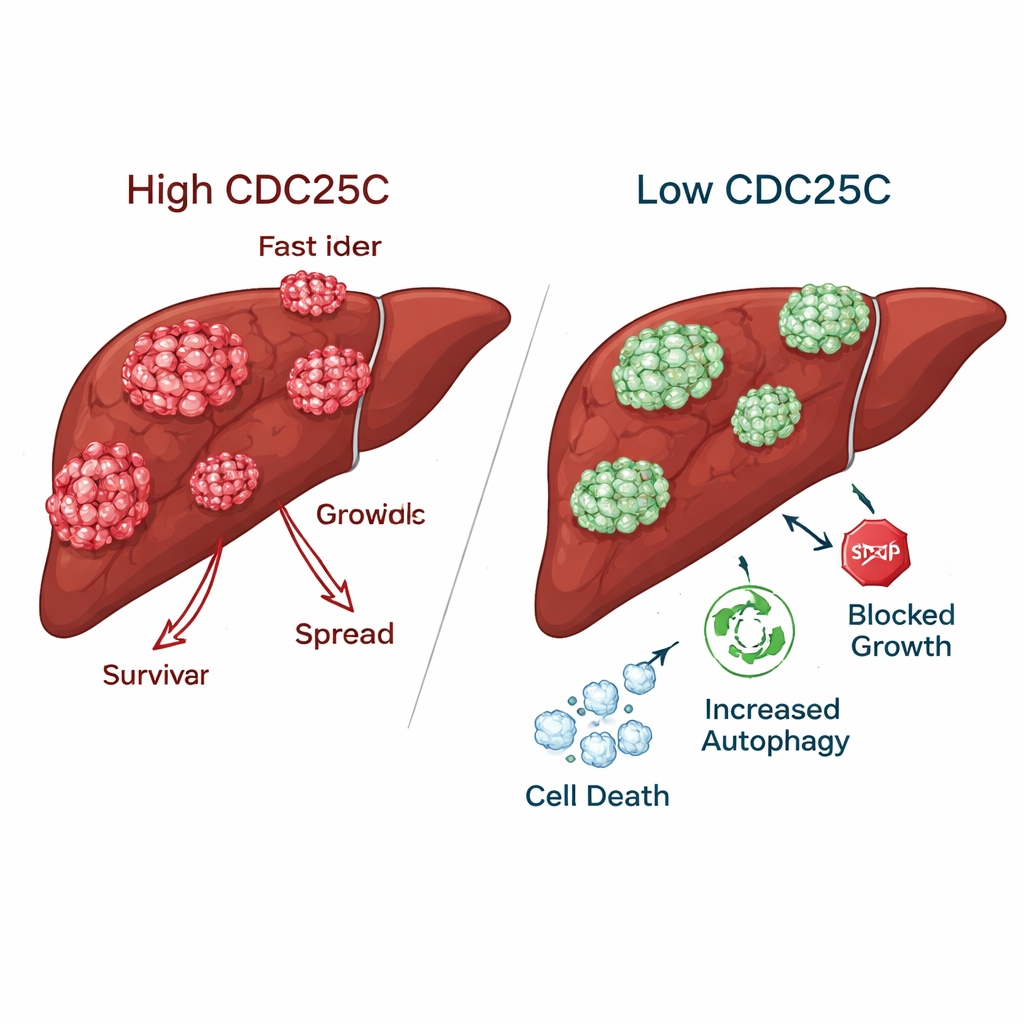
Krebs verlangsamen bei Schonung gesunder Leberzellen
Wurde CDC25C in Leberkrebszellen reduziert, verloren die Tumoren viele ihrer aggressiven Eigenschaften. Krebszellen bildeten deutlich weniger Kolonien, wanderten langsamer über künstliche „Wunden“ und konnten in Labortests schlechter durch Barrieren eindringen. Im Gegensatz dazu zeigten normale Leberzellen bei gesenktem CDC25C-Wert tatsächlich bessere Wachstums- und Bewegungsfähigkeiten, was darauf hindeutet, dass gesundes Gewebe eine CDC25C-Hemmung tolerieren oder sogar davon profitieren könnte. In Mäusen zeigten Tumore mit reduziertem CDC25C sowohl auf Gen- als auch auf Proteinebene niedrigere Werte dieses Proteins, was bestätigt, dass derselbe Effekt auch in lebenden Organismen auftrat.
Powerhouse-Stress und die Reinigungscrew der Zelle
Bei Betrachtung der Zellen im Elektronenmikroskop stellten die Forschenden fest, dass Krebszellen mit geringem CDC25C geschwollene, geschädigte Mitochondrien enthielten — die winzigen Kraftwerke der Zelle — sowie blasenartige Strukturen, sogenannte Autophagosomen, die auf eine Aktivierung des zellinternen Recyclingsystems, der Autophagie, hinweisen. Sie maßen dann zentrale Indikatoren für mitochondrialen Stress: Calciumspiegel und reaktive Sauerstoffspezies (ROS), die beide in Krebszellen nach CDC25C-Reduktion erhöht waren. Marker der mitochondrialen Stressantwort, einschließlich Hilfsproteinen wie HSP60 und zweier mitochondrialer „Qualitätskontroll“-Enzyme, waren ebenfalls erhöht, ebenso wie CHOP, ein stressbezogener Faktor, der mitochondriale Probleme mit weiterreichenden zellulären Reaktionen verbindet. Auffällig war, dass sich diese Stresssignale in normalen Leberzellen in die entgegengesetzte Richtung bewegten, was die Idee stützt, dass Krebs- und gesunde Zellen sehr unterschiedlich auf den Verlust von CDC25C reagieren.
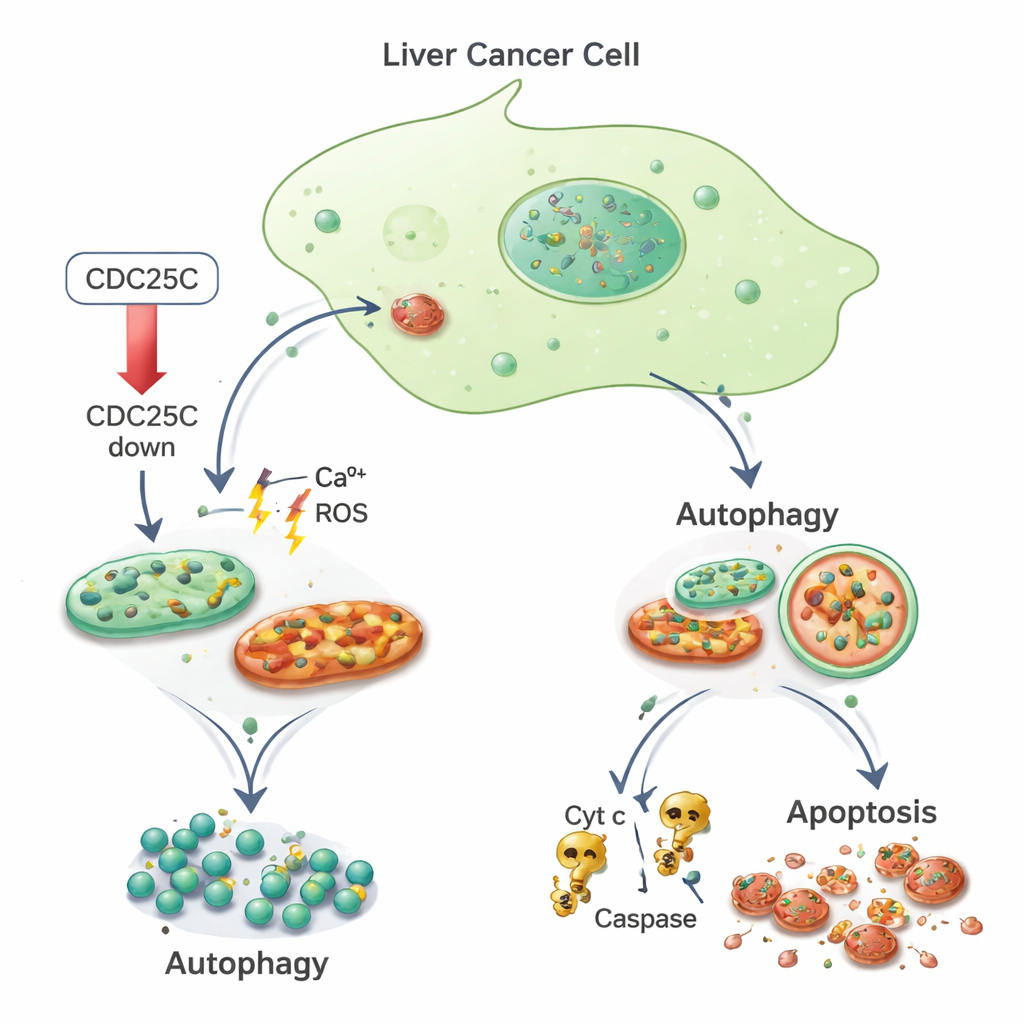
Von Stress zu Selbstverdau und Zelltod
Das Team fragte als Nächstes, wie diese gestressten Krebszellen zurechtkamen. Sie fanden heraus, dass Marker der Autophagie sowohl in Krebs- als auch in normalen Leberzellen erhöht waren, wenn CDC25C reduziert wurde. Proteine wie LC3 und p62, die Bildung und Aktivität von Autophagosomen widerspiegeln, stiegen an, was darauf hindeutet, dass die Zellen ihre Aufräummaschinen hochfuhren. Zugleich schien in Krebszellen die mitochondriale Schädigung die Zellen über die Reparaturfähigkeit hinaus zu treiben und in den programmierten Zelltod zu verlagern. Mithilfe fluoreszierender Färbungen und Durchflusszytometrie beobachteten die Forschenden mehr Krebszellen mit fragmentierten, hell gefärbten Zellkernen — ein Kennzeichen der Apoptose — und eine verringerte mitochondriale Membranpotenzial. Sie fanden außerdem erhöhte Spiegel von Cytochrom c sowie der Enzyme Caspase-3 und Caspase-9, klassische Komponenten des mitochondriengetriebenen Todeswegs. Normale Leberzellen zeigten unter denselben Bedingungen mit erniedrigtem CDC25C hingegen weniger Apoptose.
Was das für künftige Therapien bedeuten könnte
Für eine interessierte Leserschaft lautet die Kernaussage, dass das Herunterregeln von CDC25C offenbar Leberkrebszellen an einer verwundbaren Stelle trifft: Es überlastet ihre Kraftwerke, treibt das Recycling der Zelle in den Übertrieb und löst letztlich eine saubere Selbstzerstörung aus — während gesunde Leberzellen größtenteils verschont bleiben. Die Autorinnen und Autoren folgern, dass CDC25C mehr ist als ein einfacher Wachstumsschalter; es bestimmt auch, wie Zellen mit Stress, Aufräumprozessen und Tod umgehen. Da Krebszellen stark von CDC25C abhängig sind und sein Verlust bei ihnen zu tödlichem mitochondrialem Stress und Apoptose führt, könnten Medikamente, die dieses Protein oder seine nachgeschalteten Stresswege hemmen, eines Tages eine selektivere Möglichkeit bieten, Leberkrebs zu behandeln und dabei das gesunde Lebergewebe weniger zu schädigen.
Zitation: Miao, X., Zheng, F., Mo, X. et al. CDC25C downregulation suppresses HCC growth via mitochondrial stress-induced autophagy and apoptosis. Sci Rep 16, 5631 (2026). https://doi.org/10.1038/s41598-026-36351-2
Schlüsselwörter: hepatozelluläres Karzinom, CDC25C, mitochondrialer Stress, Autophagie, Apoptose