Clear Sky Science · de
TET1 unterdrückt das Fortschreiten des hepatozellulären Karzinoms durch Modulation der PI3K/Akt‑Signalwege
Warum ein Leberenzym für Krebs wichtig ist
Primärer Leberkrebs, insbesondere die Form des hepatozellulären Karzinoms, gehört weltweit zu den tödlichsten Krebsarten. Viele Patientinnen und Patienten werden zu spät für eine kurative Operation diagnostiziert, und vorhandene Medikamente helfen nur einem Teil von ihnen. Diese Studie untersucht ein Molekül namens TET1, ein Enzym, das chemische Markierungen auf der DNA verändert, und stellt eine einfache, aber wichtige Frage: Fördert TET1 das Wachstum von Lebertumoren, und könnte es ein neues Therapieziel werden?
Ein verborgener Editor in unserer DNA
Unsere Gene werden nicht nur durch den DNA-Code selbst gesteuert, sondern auch durch chemische Markierungen, die Gene an- oder ausschalten. Eine verbreitete Markierung ist die DNA‑Methylierung, die wie ein Dimmer für die Genaktivität wirkt. TET1 gehört zu einer Enzymfamilie, die diese Markierungen entfernt oder umformt und so Zellen hilft, auf ihre Umgebung zu reagieren und ihre normale Funktion zu erhalten. Wird dieses System gestört, können Zellen in krankhafte Zustände abrutschen, einschließlich Krebs. Frühere Forschungen zeigten, dass TET1 je nach Gewebe das Tumorwachstum bremsen oder fördern kann, doch seine genaue Rolle beim menschlichen Leberkrebs war unklar und umstritten.
TET1‑Spiegel steigen in Lebertumoren
Um herauszufinden, was TET1 beim Leberkrebs bewirkt, werteten die Forschenden zunächst große öffentliche Gen‑Datenbanken und anschließend Patientinnen‑ und Patientenproben aus. In mehreren Krebsarten waren die TET1‑Spiegel ungewöhnlich hoch, darunter auch beim Leberkrebs. Konzentriert auf Lebertumoren verglichen sie Tumorgewebe mit dem nahegelegenen nicht‑tumorösen Lebergewebe derselben Patientinnen und Patienten. In acht gepaarten Proben war das TET1‑Protein im Tumor durchweg erhöht. Öffentliche Datensätze mit Hunderten von Patienten zeigten dasselbe auf RNA‑Ebene: Leberkarzinome wiesen mehr TET1 auf als gesunde Lebern oder lediglich vernarbte Lebern. Patienten mit höheren TET1‑Werten in ihren Tumoren neigten zu fortgeschrittenerer Erkrankung und hatten eine kürzere Gesamt‑ sowie krankheitsfreie Überlebenszeit, was darauf hindeutet, dass TET1 mit Tumoraggressivität und ungünstiger Prognose verknüpft ist.
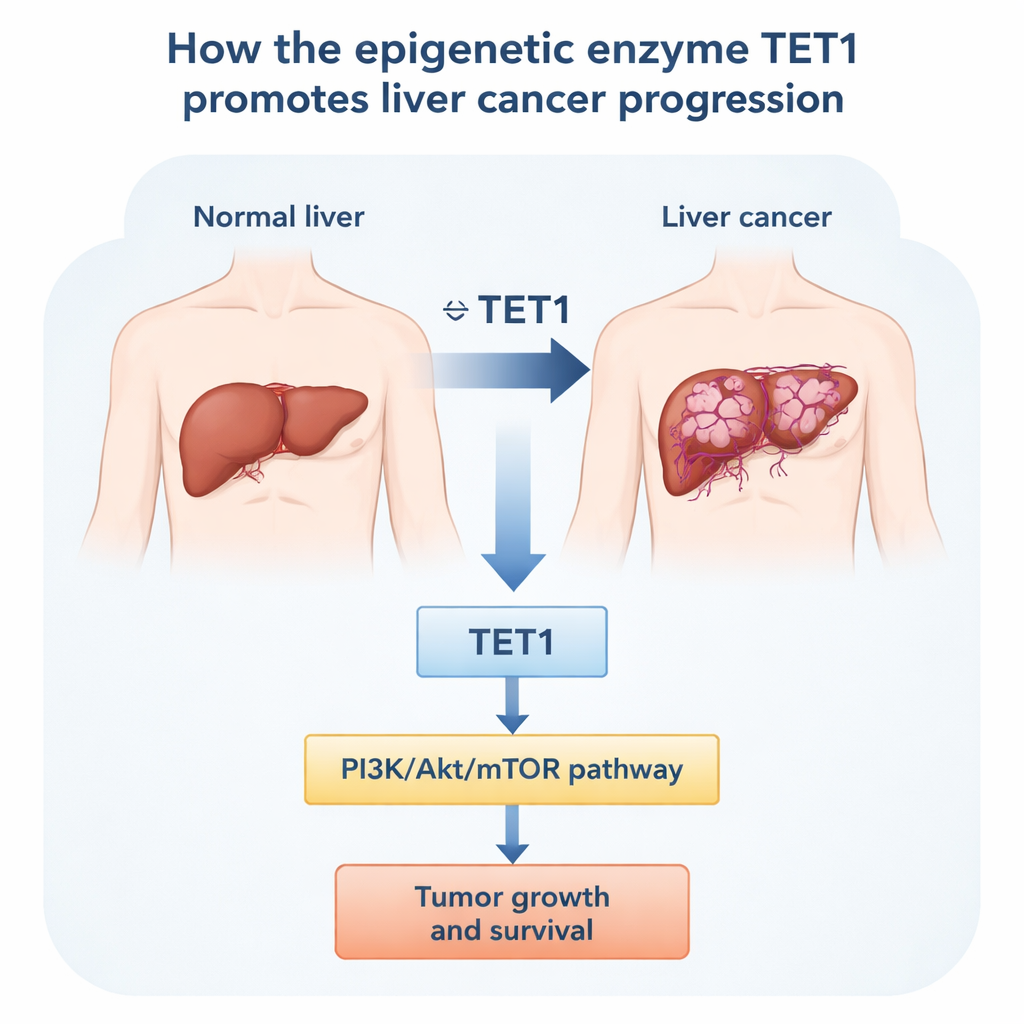
TET1 herunterzufahren bremst Tumorzellen
Als Nächstes fragten die Forschenden, was passiert, wenn TET1 in Leberkrebszellen im Labor reduziert wird. Mithilfe kurzer RNA‑Fragmente zur Stilllegung des TET1‑Gens senkten sie TET1‑Spiegel in mehreren menschlichen Leberkrebszelllinien drastisch, auch in solchen mit hepatitis‑B‑Virus‑assoziierten Veränderungen. Nach der Suppression teilten sich die Zellen langsamer, bildeten weniger Kolonien und zeigten eindeutige Stressanzeichen. Durch Flusszytometrie stellte man fest, dass mehr Zellen in der frühen G1‑Phase des Zellzyklus verharrten, anstatt weiter zur Teilung voranzuschreiten. Gleichzeitig stieg der Anteil an Zellen, die programmierter Zelltod (Apoptose) erleiden, deutlich an. Diese Effekte traten sowohl in typischen Leberkrebszellen als auch in einer HBV‑positiven Linie auf, was darauf hinweist, dass TET1 das Überleben und das fortlaufende Wachstum über verschiedene Leberkrebs‑Hintergründe hinweg unterstützt.
Ein Wachstumsweg unter TET1‑Kontrolle
Um aufzudecken, wie TET1 diesen Einfluss ausübt, analysierten die Forschenden die Gene, die sich zwischen normalen Leberzellen und Krebszellen unterscheiden. Tausende Gene wichen ab, viele davon gruppierten sich in bekannten Wachstums‑ und Überlebensnetzwerken. Ein Signalweg stach hervor: PI3K/Akt/mTOR, eine zentrale Signalkette, die viele Krebsarten nutzen, um Stoffwechsel zu steigern, Zelltod zu widerstehen und Therapien zu entgehen. Datenbankanalysen zeigten, dass TET1‑Spiegel parallel zu Kernkomponenten dieses Weges stiegen und invers zu PTEN, einem natürlichen Bremsmechanismus der PI3K/Akt‑Aktivität, fielen. Wurde TET1 in Leberkrebszellen stillgelegt, nahmen die aktivierten, „phosphorylierten“ Formen von PI3K, Akt und besonders mTOR ab. Die Behandlung der Zellen mit einem chemischen Inhibitor, der die Aktivität der TET‑Familie blockiert, verringerte ebenfalls die Phosphorylierung von Akt und mTOR. Diese Ergebnisse deuten darauf hin, dass die enzymatische Aktivität von TET1 — seine Fähigkeit, DNA‑Marken umzugestalten — in die PI3K/Akt/mTOR‑Kaskade einfließt und das Gleichgewicht zugunsten von Wachstum und Überleben verschiebt statt hin zu Kontrolle und Hemmung.
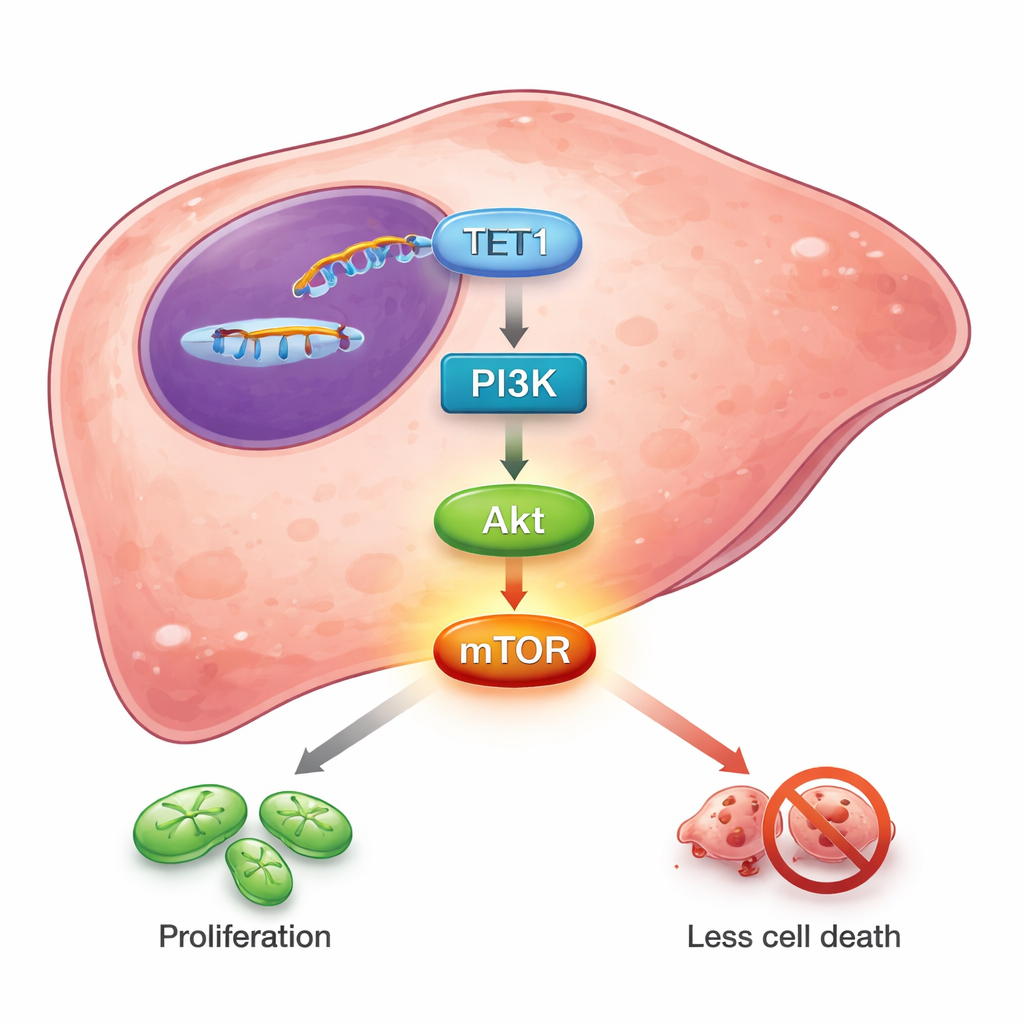
Vom molekularen Einblick zu möglichen Behandlungen
Insgesamt zeichnet diese Arbeit TET1 eher als Verbündeten von Lebertumoren denn als deren Schutzfaktor. Ein hoher TET1‑Spiegel unterstützt die Proliferation und das Ausweichen vor dem Zelltod von Leberkrebszellen, teils indem er den PI3K/Akt/mTOR‑Signalweg aktiviert hält. Beim Patienten gehen höhere TET1‑Werte im Tumor mit fortgeschrittenerer Erkrankung und schlechterer Prognose einher. Für die interessierte Leserin bzw. den interessierten Leser lautet die Botschaft: Ein Enzym, das still und leise chemische Markierungen auf der DNA bearbeitet, kann maßgeblich darüber entscheiden, ob Leberkrebszellen überleben oder zugrunde gehen. Durch die Entwicklung von TET1‑Inhibitoren oder die Kombination solcher Wirkstoffe mit bestehenden PI3K/Akt‑gerichteten Therapien könnten künftige Behandlungen eine wichtige Stütze der Tumore abschneiden und das Überleben von Menschen mit dieser schweren Erkrankung verbessern.
Zitation: Qi, S., Chen, M., Ding, Z. et al. TET1 suppresses hepatocellular carcinoma progression by modulating the PI3K/Akt signaling pathways. Sci Rep 16, 5791 (2026). https://doi.org/10.1038/s41598-026-36334-3
Schlüsselwörter: Leberkrebs, TET1, Epigenetik, PI3K Akt mTOR, hepatozelluläres Karzinom