Clear Sky Science · de
Fäkales Mikrobiom sagt die Behandlungsantwort nach Beginn von Semaglutid- oder Empagliflozin‑Einnahme voraus
Warum Ihre Darmbakterien die Diabetesbehandlung beeinflussen könnten
Menschen mit Typ‑2‑Diabetes erhalten zunehmend neuere Medikamente wie Semaglutid (oft aus Abnehmwerbung bekannt) und Empagliflozin, die helfen, den Blutzucker und das Körpergewicht zu senken. Doch nicht alle sprechen gleichermaßen gut an. Diese Studie stellt eine einfache, aber wirkungsvolle Frage: Können die Billionen von Bakterien in unserem Darm erklären, wer am meisten von diesen Medikamenten profitiert, und könnten sie eines Tages eine individuellere Diabetesbehandlung ermöglichen?
Studienaufbau und gemessene Größen
Forscher begleiteten 20 Erwachsene mit Typ‑2‑Diabetes, die bereits das Standardmedikament Metformin einnahmen und übergewichtig bzw. adipös waren. Ihre Ärztinnen und Ärzte ergänzten je nach medizinischer Notwendigkeit entweder Semaglutid oder Empagliflozin. Über ein Jahr lieferten die Teilnehmerinnen und Teilnehmer viermal Stuhlproben sowie dreimal Blut‑ und Urinproben. Die Stuhlproben dienten der Profilierung der Darmbakterien, während Blut‑ und Urintests wichtige Gesundheitsmarker wie Langzeitblutzucker (HbA1c), Körpergewicht, Nierenfunktion und Hinweise auf Entzündung verfolgten. Dieses Design erlaubte dem Team, sowohl die Wirkung der Medikamente auf die Gesundheit zu beobachten als auch zu prüfen, ob das Ausgangs‑Mikrobiom diese Veränderungen vorhersagen kann. 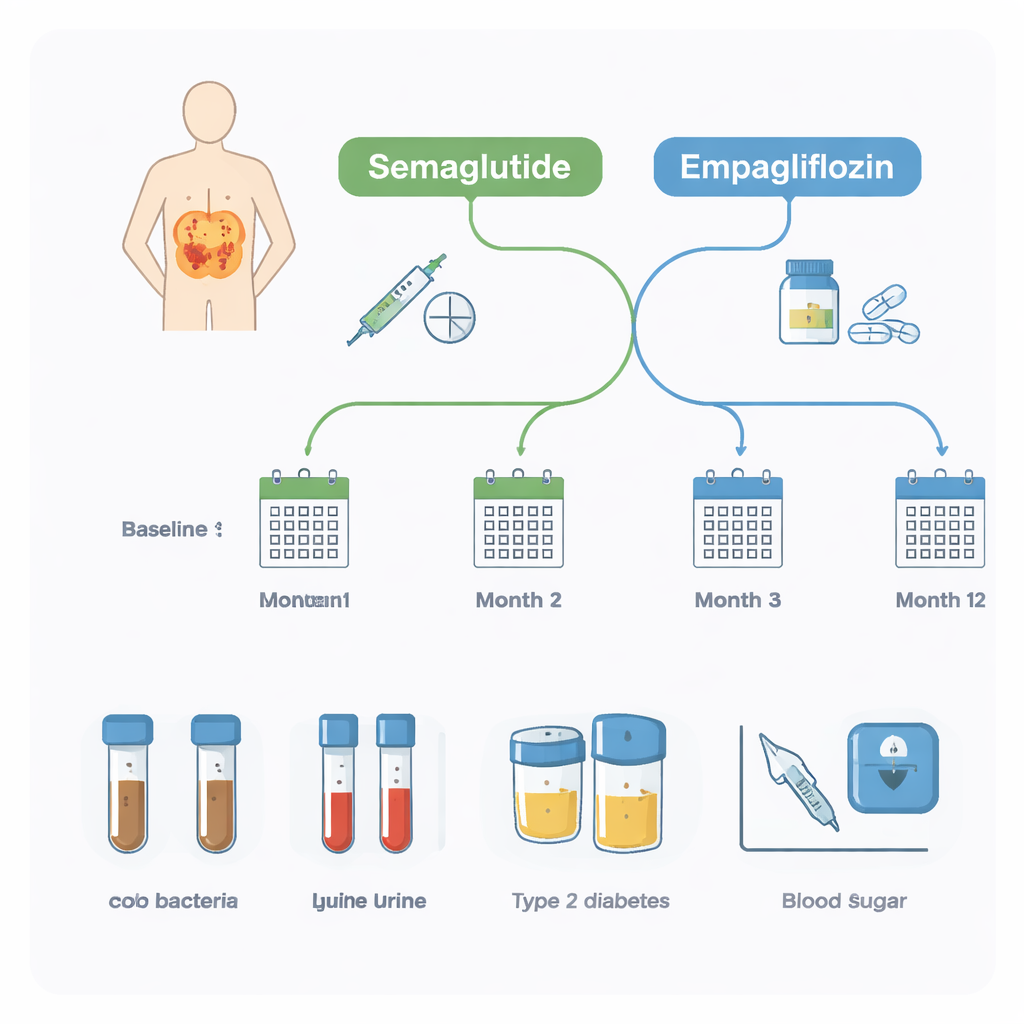
Wie sich die Medikamente auf Gesundheit und Darmgemeinschaften auswirkten
Klinisch verbesserten beide Medikamente die Blutzuckerkontrolle bis zum dritten Behandlungsmonat, und Semaglutid führte besonders zu einem ausgeprägten und anhaltenden Gewichtsverlust über 12 Monate. Bei der Untersuchung der bakteriellen Diversität im Darm – wie viele verschiedene Typen vorhanden sind und wie gleichmäßig sie verteilt sind – ergab sich kein klarer Gesamteffekt nach Beginn eines der beiden Arzneimittel. Ebenso blieben die meisten offenbareren Veränderungen in der Zusammensetzung bakterieller Gruppen statistisch nicht robust, sobald strenge Korrekturen für Mehrfachtests angewendet wurden. Einige Bakteriengruppen und vorhergesagte Stoffwechselwege schienen sich zwischen Monat 3 und 12 zu verändern, diese Muster waren jedoch modest und reflektierten wahrscheinlich indirekte Effekte einer verbesserten Stoffwechselfunktion oder veränderter Lebensweise statt einer direkten Wirkung der Medikamente.
Darmbakterien als potenzielle Prädiktoren für Therapieerfolg
Die interessantesten Befunde ergaben sich aus der Analyse des Mikrobioms vor Behandlungsbeginn und der Frage, ob es vorhersagen kann, wer sich am stärksten verbessert. Bei Personen, die Semaglutid erhielten, zeigten Hunderte von mikrobiellen Ausgangsmerkmalen nominale Zusammenhänge mit späteren Veränderungen klinischer Marker, insbesondere der weißen Blutkörperchen und eines Entzündungsmaßes, des Neutrophilen‑zu‑Lymphozyten‑Verhältnisses. Nach strenger statistischer Filterung blieb eine Bakteriengruppe namens Alistipes signifikant assoziiert: Individuen mit mehr dieses Bakteriums zum Ausgangszeitpunkt neigten zu einem stärkeren Rückgang der Entzündungszellen. Mehrere bakterielle Gattungen und mikrobielle Stoffwechselwege im Ausgangsbefund korrelierten außerdem damit, wie stark das HbA1c bis zum dritten Monat sank, was andeutet, dass die anfängliche Darmgemeinschaft beeinflussen könnte, wie stark Semaglutid den Blutzucker senkt. In der Empagliflozingruppe waren zahlreiche Bakterien und Wege ebenfalls mit Veränderungen von HbA1c und Nierenfunktionsparametern verknüpft, doch überstanden keine dieser Assoziationen die konservativsten statistischen Tests, teilweise weil die Studie klein war.
Was die Ergebnisse bedeuten – und was nicht
Wichtig ist: Diese Arbeit behauptet nicht, dass Semaglutid oder Empagliflozin das Darmmikrobiom allein dramatisch umgestalten, noch dass ein bestimmtes Bakterium Erfolg oder Misserfolg garantiert. Vielmehr legt sie nahe, dass subtile Merkmale der bereits bestehenden Darmgemeinschaft mit der individuellen Reaktion verbunden sein können – nicht nur in Bezug auf den Blutzucker, sondern auch auf Entzündung und andere Gesundheitsmarker. Da alle Teilnehmenden bereits Metformin einnahmen, das seinerseits das Darmmikrobiom beeinflusst, war ein zusätzlicher Einfluss der neueren Medikamente möglicherweise schwerer nachzuweisen. Die bescheidene Stichprobengröße und einige fehlende Proben schränken zudem die Zuverlässigkeit ein, mit der einzelne bakterielle Gruppen als wahre Treiber der Arzneimittelantwort identifiziert werden können.
Blick nach vorn: maßgeschneiderte Diabetesbehandlung
Für Laien lautet die Kernbotschaft: Ihre Darmbakterien könnten eines Tages Ärzten helfen, das Diabetesmedikament zu wählen, das am besten für Sie wirkt. In dieser frühen Studie war die Zusammensetzung der Mikroben in vor Behandlungsbeginn entnommenen Stuhlproben mit der Stärke der Verbesserungen von Blutzucker und Entzündung durch Semaglutid und Empagliflozin verknüpft, während die Medikamente selbst nur subtile, langsame Veränderungen in den Darmgemeinschaften zeigten. Größere und längere Studien werden nötig sein, um zu bestätigen, welche Mikroben wirklich relevant sind und ob deren Veränderung die Wirkung der Behandlung steigern kann. Gelingt das, könnte ein einfacher Stuhltest Teil der personalisierten Diabetesversorgung werden und helfen, das richtige Medikament mit dem passenden Mikrobiom abzugleichen. 
Zitation: Klemets, A., Reppo, I., Krigul, K.L. et al. Fecal microbiome predicts treatment response after the initiation of semaglutide or empagliflozin uptake. Sci Rep 16, 6126 (2026). https://doi.org/10.1038/s41598-026-36318-3
Schlüsselwörter: Darmmikrobiom, Typ-2-Diabetes, Semaglutid, Empagliflozin, personalmedizin