Clear Sky Science · de
Virtuelles Screening neuartiger Alkaloide als potente Inhibitoren der G2032R-mutierten ROS1‑Kinase beim nicht‑kleinzelligen Lungenkrebs
Warum das für zukünftige Lungenkrebsbehandlungen wichtig ist
Viele Menschen mit einer bestimmten Form von Lungenkrebs sprechen zu Beginn gut auf moderne zielgerichtete Therapien an, doch die Krankheit kann zurückkehren, wenn der Tumor Resistenzen entwickelt. Diese Studie untersucht, ob naturbelassene Verbindungen, sogenannte Alkaloide, einen neuen Weg bieten könnten, eine hartnäckige, gegen Medikamente resistente Version eines krebstreibenden Proteins zu blockieren — und zwar mithilfe fortgeschrittener Computersimulationen statt jahrelanger Vorarbeiten im Labor.
Ein Krebs‑Signal, das lernt, heutigen Medikamenten auszuweichen
Der nicht‑kleinzellige Lungenkrebs (NSCLC) ist die häufigste Form von Lungenkrebs. Bei einer kleinen, aber wichtigen Patientengruppe wird der Tumor durch ein fehlerhaftes Protein namens ROS1 angetrieben. Normalerweise hilft ROS1, das Zellwachstum zu steuern, doch bei Umlagerungen des Gens sendet das Protein dauerhafte „Wachstums‑und Teilungs“-Signale und fördert so den Krebs. Medikamente wie Crizotinib und später Lorlatinib wurden entwickelt, um in ROS1 zu passen und es auszuschalten. Im Lauf der Zeit erwerben viele Tumoren jedoch eine winzige Änderung — einen Austausch einer Aminosäure im Protein, genannt G2032R — die wie eine Ausbuchtung an der Tür zum Andockraum des Medikaments wirkt. Diese Veränderung erschwert es bestehenden Wirkstoffen, hineinzupassen, und Patientinnen und Patienten verlieren den Nutzen der Therapie.
Auf der Suche nach frischen Ideen in natürlichen Molekülen
Alkaloide sind eine große Familie stickstoffhaltiger Verbindungen, die von Pflanzen und anderen Organismen produziert werden. Dazu gehören bekannte Arzneistoffe wie Chinin gegen Malaria und Vinblastin gegen Krebs. Aufgrund ihrer vielfältigen und komplexen Formen sind Alkaloide ein bevorzugtes Fundgebiet für neue Medikamente. In dieser Arbeit stellten die Forschenden eine digitale Bibliothek mit 447 verschiedenen Alkaloiden zusammen und nutzten eine Reihe von Computerprogrammen, um vorherzusagen, welche davon am besten an die veränderte G2032R‑Variante von ROS1 binden könnten, während sie einige der Schwachstellen aktueller Medikamente umgehen.
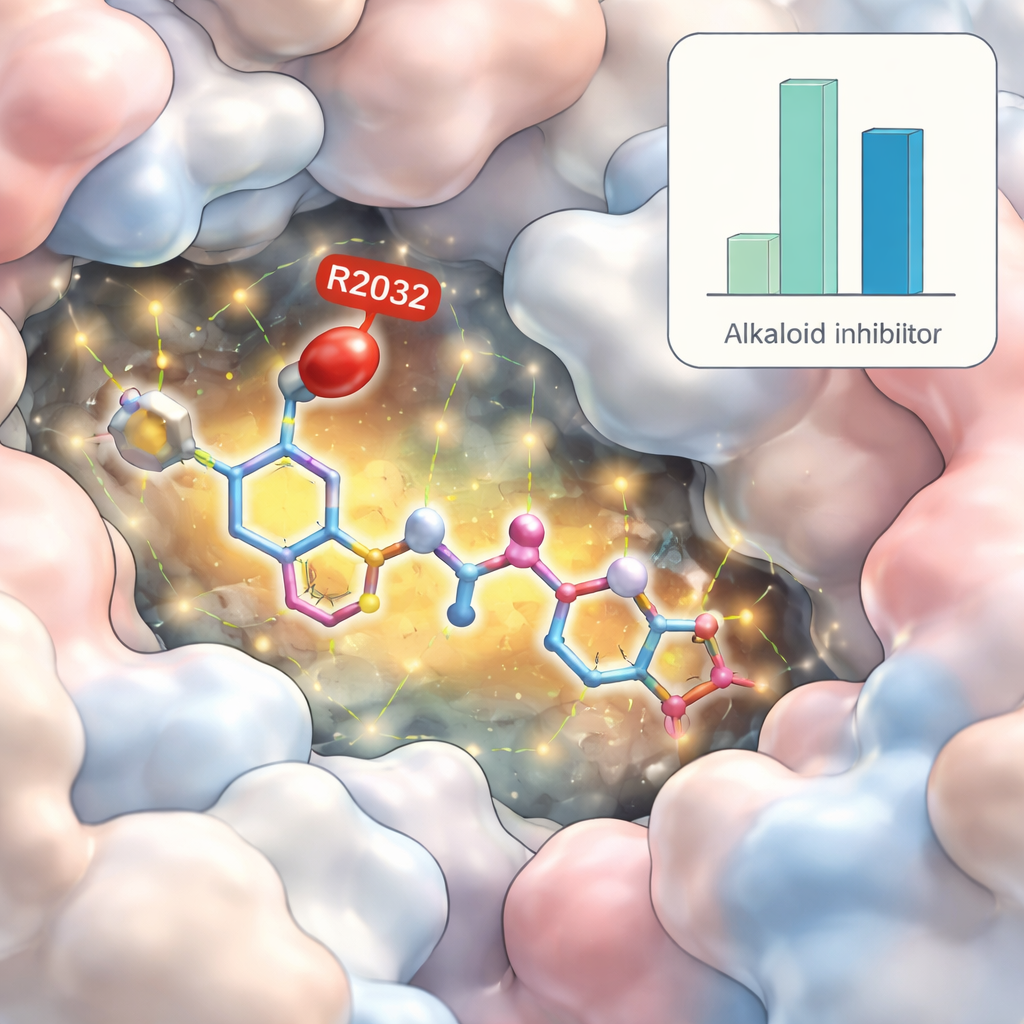
Screening, Belastungstests und Sicherheits‑Checks am Rechner
Das Team verwendete zunächst eine Methode namens virtuelles Screening, bei der jedes Alkaloid rechnerisch in die 3‑D‑Struktur des mutierten ROS1‑Proteins „gedockt“ wurde, um abzuschätzen, wie stark es binden könnte. Aus diesem großen Satz ragten zwei Moleküle mit besonders starken vorhergesagten Bindungen heraus: Yibeinosid A, ein steroidähnliches Alkaloid aus der Zwiebel einer Fritillaria‑Pflanze, und Vomicin, ein Indolalkaloid aus dem Baum Strychnos nux‑vomica. Ihre Bewertungen waren so gut wie oder besser als die von Lorlatinib, einem aktuellen ROS1‑Blocker. Die Forschenden untersuchten anschließend, wie diese Verbindungen voraussichtlich in der Taschen des Proteins sitzen und welche chemischen Kontakte sie ausbilden, einschließlich der Frage, ob sie die gerade jene Mutation nutzen können, die bestehende Medikamente ausschaltet.
Die besten Kandidaten durch virtuelle Bewegungstests schicken
Um über statische Momentaufnahmen hinauszugehen, führten die Wissenschaftler molekulardynamische Simulationen durch, die modellieren, wie sich Protein und Wirkstoff im Wasser über die Zeit bewegen und verformen. Diese „Stresstests“ deuteten darauf hin, dass Komplexe mit Yibeinosid A besonders stabil blieben, mit nur geringen Bewegungen des Proteinrückgrats und einer kompakten Form, ähnlich der mit Lorlatinib beobachteten. Vomicin zeigte ebenfalls starke Bindung, verursachte jedoch etwas mehr Bewegung und Lockerung der Proteinoberfläche. Wichtig ist, dass Yibeinosid A voraussichtlich ein dichtes Netzwerk von Wasserstoffbrücken und hydrophoben Kontakten bildet, einschließlich einer direkten Wechselwirkung mit dem veränderten Rest an Position 2032, wodurch die resistenzverursachende Ausbuchtung eher zu einem Ankerpunkt als zu einem Hindernis werden könnte.
Frühe Hinweise zu Nutzen und Risiken
Weil ein starker Binder dennoch ein ungeeignetes Arzneimittel sein kann, wenn er sich im Körper ungünstig verhält, nutzte das Team zusätzliche Software, um Absorption, Verteilung, Metabolismus und Toxizität abzuschätzen. Beide Alkaloide wurden als gut im Darm resorbierbar vorhergesagt, doch Vomicin zeigte Warnzeichen: wahrscheinlich DNA‑schädigend und in Tierversuchen krebserregend sowie insgesamt toxischer. Yibeinosid A dagegen wies ein günstigeres prognostiziertes Sicherheitsprofil auf; die Hauptsorge war mögliche Belastung der Leber — ein häufiges Problem, das im Labor sorgfältig weiter untersucht werden müsste. Kombinierte man alle Energie‑Berechnungen, erschienen sowohl Yibeinosid A als auch Vomicin stärker an die mutierte ROS1 gebunden als Lorlatinib, doch nur Yibeinosid A verband diese starke Bindung mit vergleichsweise beruhigenderen Sicherheitsvorhersagen.
Was das bedeutet und wie es weitergeht
Diese Studie liefert kein sofort einsetzbares Medikament, zeigt aber überzeugend auf Computerebene, dass Yibeinosid A ein vielversprechender Ausgangspunkt für Wirkstoffe sein könnte, die G2032R‑mutiertes ROS1 bei resistentem Lungenkrebs angreifen. Indem gezeigt wird, dass ein Naturprodukt sowohl in die veränderte Proteintasche passt als auch grundlegende virtuelle Sicherheitschecks besteht, reduziert die Arbeit die Auswahl auf einen realistischen Leitstoff, den Chemiker und Biologen in echten Zellen und Tieren testen können. Bestätigen zukünftige Experimente diese Vorhersagen, könnte Yibeinosid A — oder daraus inspirierte verbesserte Derivate — eines Tages Patienten helfen, deren Tumoren aktuellen ROS1‑gerichteten Therapien entwichen sind.
Zitation: Cho, SC., Wang, YW., Chu, CA. et al. Virtual screening of novel alkaloids as potent inhibitors for G2032R-mutant ROS1 kinase in non-small-cell lung cancer. Sci Rep 16, 5342 (2026). https://doi.org/10.1038/s41598-026-36317-4
Schlüsselwörter: nicht‑kleinzelliger Lungenkrebs, ROS1‑Mutation, Arzneimittelresistenz, Alkaloide, virtuelles Screening