Clear Sky Science · de
Überwindung der Wirkstoffresistenz von Candida albicans-Biofilmen durch Azol‑Sophorolipid-Synergie
Warum hartnäckige Pilzinfektionen wichtig sind
Wer schon einmal eine hartnäckige Hefepilzinfektion, eine zentrale Venenverweilkanüle im Krankenhaus oder ein medizinisches Implantat hatte, ist potenziell gefährdet durch Candida albicans, einen häufigen Pilz, der gefährlich werden kann, wenn er schwer behandelbare Gemeinschaften bildet, sogenannte Biofilme. Diese schleimigen Schichten schützen die Mikroben vor vielen unserer besten Antimykotika, sodass Infektionen bestehen bleiben und mitunter lebensbedrohlich werden können. Die hier beschriebene Studie sucht nach einem neuen Weg, diese Verteidigung aufzubrechen, indem vorhandene Medikamente mit einem natürlichen, seifenähnlichen Molekül kombiniert werden, das von Hefen produziert wird.
Ein verborgener Schutz auf medizinischen Oberflächen
Candida albicans kann an Geweben und medizinischen Geräten haften und dann zu strukturierten Biofilmen heranwachsen—dichten Zellschichten, zusammengehalten von einer selbst erzeugten Matrix aus Zuckern, Proteinen und DNA. Innerhalb dieser Festung verlangsamt der Pilz seinen Stoffwechsel und pumpt Wirkstoffe wieder heraus, sodass Medikamente, die frei schwimmende Zellen leicht töten, bei Biofilm‑bewohnenden kaum wirken. Azol‑Medikamente wie Fluconazol und Itraconazol sind Grundpfeiler der antimykotischen Therapie, doch gegen ausgereifte Biofilme benötigen sie oft deutlich höhere Dosen, was Nebenwirkungen verursachen und trotzdem das Versagen der Therapie bedeuten kann. Kliniker sehen zunehmend Infektionen, die sowohl biofilmbasiert als auch resistent sind, was den Bedarf an Hilfsmolekülen unterstreicht, die den Biofilm selbst schwächen können.
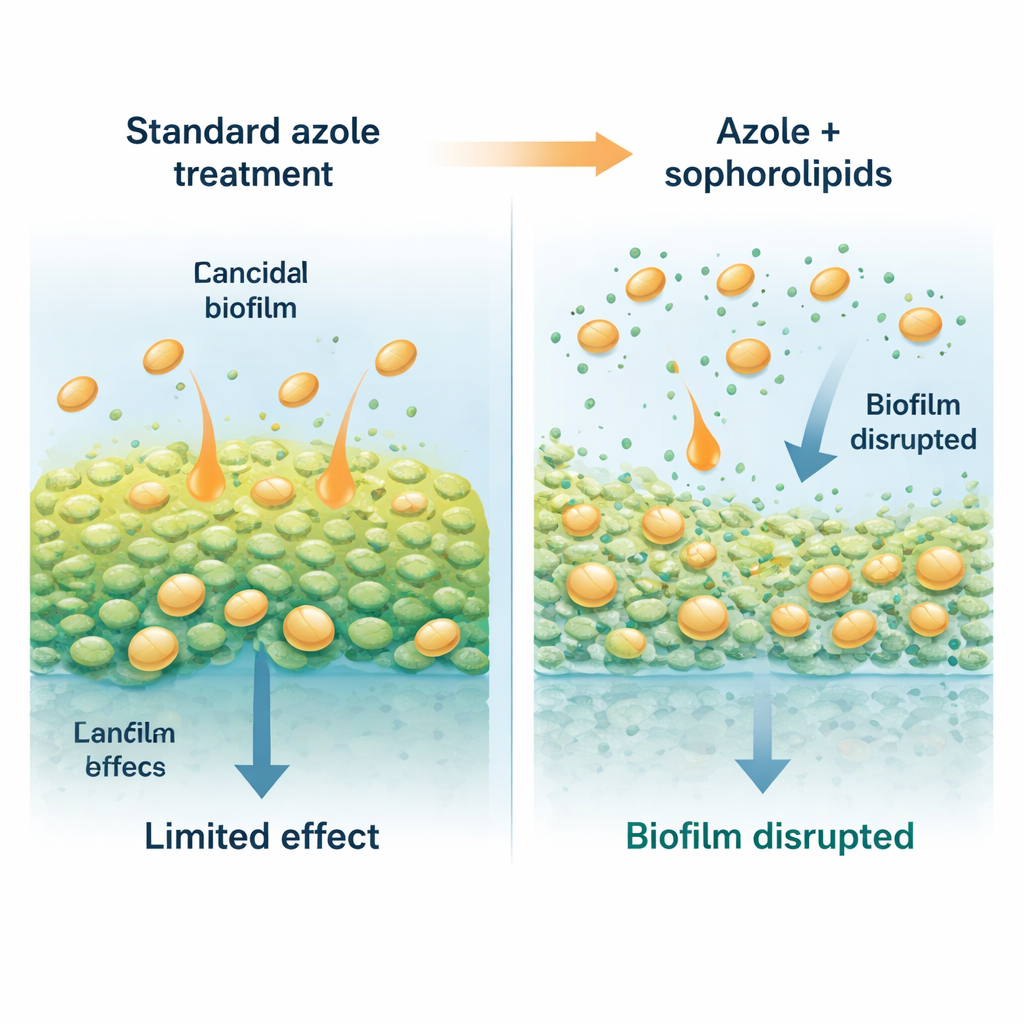
Seifenähnliche Helfer aus einer harmlosen Hefe
Die Forschenden wandten sich Sophorolipiden zu, natürlichen, biologisch abbaubaren Tensiden—Molekülen, die sich ein wenig wie sehr milde Reinigungsmittel verhalten—die von bestimmten nicht-pathogenen Hefen produziert werden. Diese Moleküle besitzen einen wasserliebenden Zucker‑Kopf und einen fettigen Schwanz, wodurch sie an Oberflächen und Grenzflächen Platz nehmen können. In dieser Studie wurde eine Hefe namens Starmerella riodocensis zur Produktion eines Sophorolipid‑Gemischs verwendet, das anschließend gereinigt und analysiert wurde. Für sich genommen töteten diese Sophorolipide freie Candida‑Zellen selbst bei hohen Dosen nicht, aber sie beeinträchtigten stark die Fähigkeit des Pilzes, Biofilme zu bilden und aufrechtzuerhalten. Besonders empfindlich waren junge, gerade entstehende Biofilme; selbst etablierte 24‑Stunden‑Biofilme ließen sich bei Exposition gegenüber gereinigten Sophorolipiden ausdünnen und abschwächen.
Gemeinsam mit bestehenden Antimykotika
Zentrale Frage war, ob Sophorolipide Standard‑Azolmedikamente wirksamer machen können. Das Team testete Kombinationen von Sophorolipiden mit drei weit verbreiteten Azolen: Fluconazol, Itraconazol und Ketoconazol. Beim Aussetzen von Biofilmen an diese Mischungen stellten sie fest, dass einige Paarungen mehr als nur additive Effekte zeigten—sie wirkten synergistisch, das heißt, die Kombination war stärker als man anhand der Wirkungen der Einzelkomponenten erwartet hätte. Die herausragende Partnerschaft war Itraconazol plus Sophorolipide. Gegen robuste, bereits gebildete Biofilme sank die Menge an Itraconazol, die nötig war, um den Biofilm halbieren, um das bis zu Sechzehnfache, während auch die erforderliche Sophorolipid‑Dosis im Vergleich zur alleinigen Anwendung von Sophorolipiden mehrere Male niedriger war. Kombinationen mit Fluconazol und Ketoconazol zeigten moderatere Verbesserungen, was darauf hindeutet, dass die chemische Natur jedes Medikaments beeinflusst, wie stark es vom Tensid‑„Assist“ profitiert.
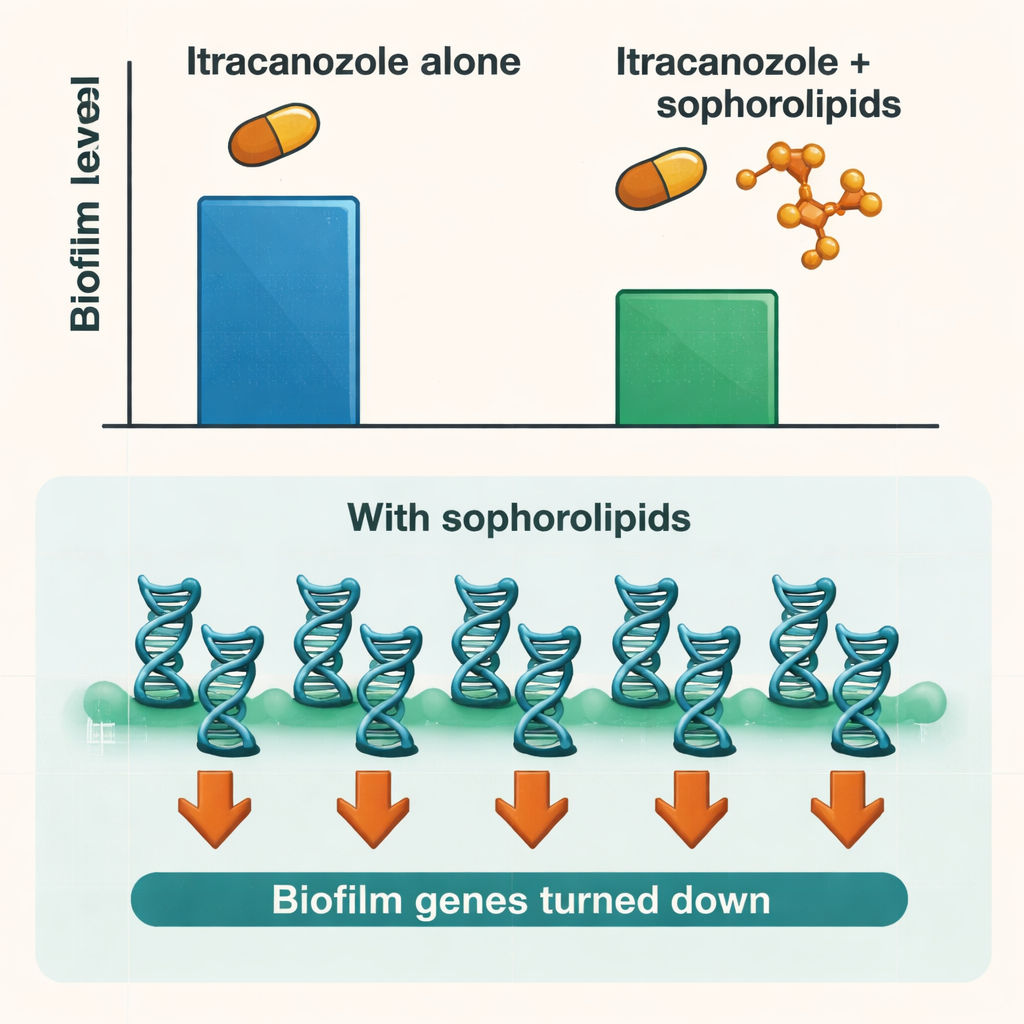
Stummschaltung des Biofilmprogramms des Pilzes
Um zu verstehen, was in den Pilzzellen vor sich ging, untersuchten die Forschenden die Aktivität wichtiger Candida‑Gene, die an Haftung an Oberflächen, am Wachstum als Filamente und am Aufbau der Biofilm‑Matrix beteiligt sind. Die Behandlung mit Sophorolipiden allein drosselte viele dieser Gene, insbesondere jene, die die frühesten Schritte der Adhäsion und den Übergang von hefelartigen zu filamentösen Formen steuern. Wenn Zellen in einem bestimmten Zellzyklusstadium synchronisiert wurden, das die Biofilmbildung begünstigt, waren die Gen‑stummmachenden Effekte noch stärker. Das deutet darauf hin, dass Sophorolipide nicht einfach den Biofilm wegwaschen; sie stören auch das biologische Programm des Pilzes zum Aufbau und zur Aufrechterhaltung seiner Schutzgemeinschaft.
Hoffnung auf schonendere, effektivere Behandlungen
Die Studie kommt zu dem Schluss, dass Sophorolipide aus Starmerella riodocensis als sichere, biofilm‑zielende Partner für Azolmedikamente dienen können, wobei die Kombination aus Itraconazol und Sophorolipiden besonders potent ist. Da Sophorolipide in Säugerzellen eine geringe Toxizität zeigen und hauptsächlich die Biofilmstruktur und die zugehörigen Gen‑Netzwerke schwächen, statt den Pilz direkt zu vergiften, könnten sie es ermöglichen, niedrigere Dosen konventioneller Medikamente zu verwenden und trotzdem hartnäckige Infektionen auf Geräten und Geweben zu beseitigen. Für Patientinnen und Patienten könnte diese Art von intelligenter Kombinationstherapie eines Tages in Behandlungen münden, die sowohl gegen resistente Candida‑Biofilme effektiver als auch schonender für den restlichen Körper sind.
Zitation: Jayasekara, L.C.B., Watchaputi, K., Butkinaree, C. et al. Overcoming Candida albicans biofilm drug resistance via azole-sophorolipid synergy. Sci Rep 16, 5963 (2026). https://doi.org/10.1038/s41598-026-36278-8
Schlüsselwörter: Candida-Biofilm, Azol-Antimykotika, Sophorolipide, Wirkstoffsynergie, antimikrobielle Resistenz