Clear Sky Science · de
Landesweite genomische Überwachung von Carbapenem- und Colistin-resistenten Klebsiella pneumoniae-Blutstromisolaten in Thailand (2020–2024)
Tödliche Blutinfektionen im Anstieg
Krankenhäuser weltweit sehen sich mit einem beunruhigenden Trend konfrontiert: Gewöhnliche Bakterien, die früher auf unsere stärksten Antibiotika reagierten, werden zunehmend nahezu unbehandelbar. Diese Studie konzentriert sich auf Klebsiella pneumoniae, ein Mikroorganismus, der in den Blutkreislauf eindringen und lebensbedrohliche Infektionen verursachen kann, und verfolgt, wie er sich in Thailand entwickelt hat, um selbst den Reservemedikamenten zu widerstehen. Zu wissen, wo sich diese Superkeime ausbreiten und wie sie Arzneimittel umgehen, ist entscheidend zum Schutz von Patienten, für die Therapieauswahl der Ärztinnen und Ärzte und zur Gestaltung der Gesundheitspolitik.
Verfolgung eines Krankenhaus‑Superkeims über ein ganzes Land
Die Forschenden analysierten 227 Klebsiella pneumoniae-Proben aus dem Blut von Patientinnen und Patienten in Krankenhäusern in ganz Thailand zwischen 2020 und 2024. Diese Proben stammten aus einem landesweiten Überwachungsnetzwerk, das routinemäßig Daten zu resistenten Infektionen sammelt. Labortests zeigten, dass über 93 % dieser Blutstromisolate gegen Carbapeneme resistent waren, eine potente Antibiotikaklasse, die oft eingesetzt wird, wenn andere Medikamente versagen. Besorgniserregend war, dass nahezu ein Drittel der carbapenemresistenten Stämme auch gegen Colistin resistent war, eines der letzten Mittel, zu denen Ärztinnen und Ärzte greifen, wenn sonst nichts mehr hilft. In Kombination von Standard‑Empfindlichkeitstests und Ganzgenomsequenzierung konnte das Team nicht nur sehen, gegen welche Medikamente die Bakterien resistent waren, sondern auch welche genetischen Tricks sie zur Überlebenssicherung nutzten.
Hochrisiko‑Klonen und regionale Muster
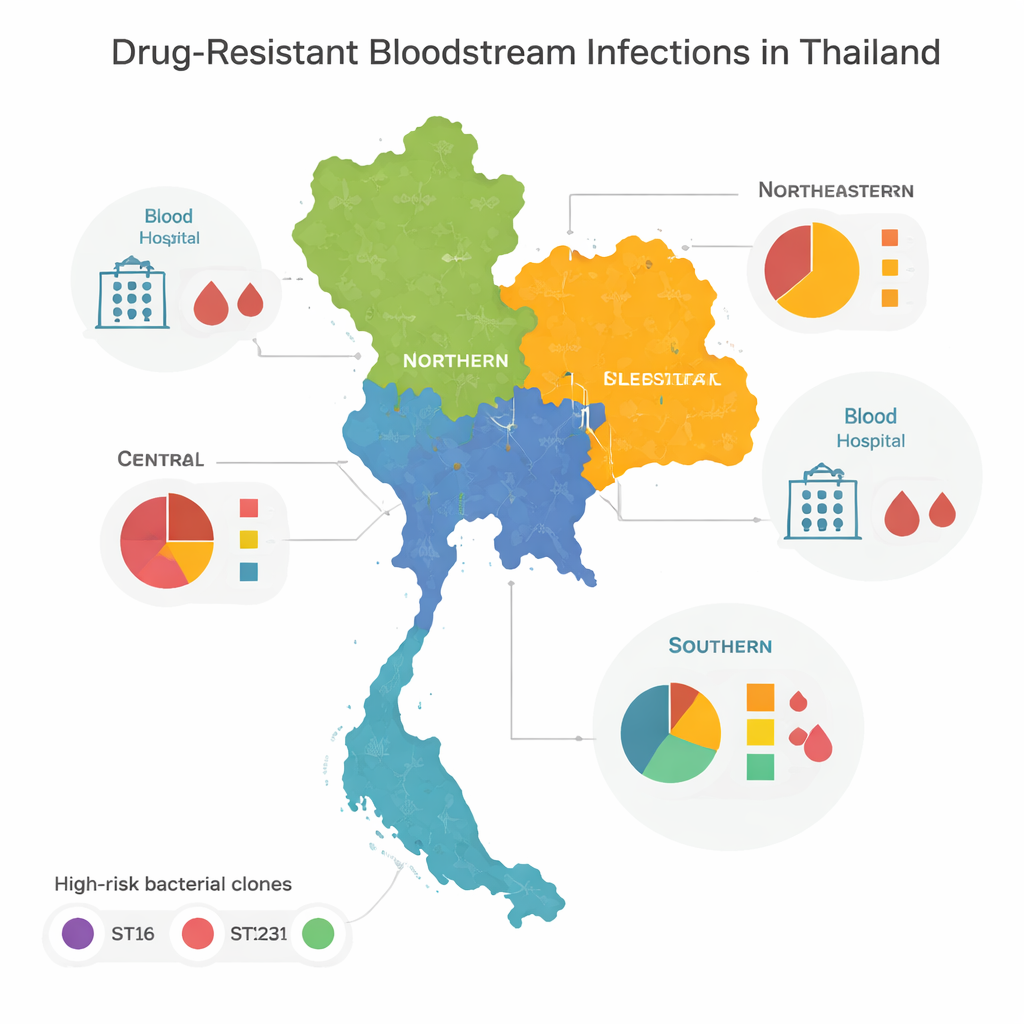
Beim Vergleich der Genome stellten die Forschenden fest, dass die meisten resistenten Bakterien zu einigen wenigen „Hochrisiko“-Familien oder Klonen gehörten, die weltweit für Ausbrüche in Krankenhäusern bekannt sind. Drei davon – bezeichnet als ST16, ST147 und ST231 – dominierten in Zentral-, Nord‑ und Nordost‑Thailand. Diese Klone hatten sich breit über die Regionen ausgebreitet, was auf häufige Verlagerung von Patientinnen und Patienten, Personal oder Bakterien zwischen Krankenhäusern hindeutet. Der Süden des Landes sah anders aus: Statt von wenigen Typen dominiert zu werden, wies er eine große Vielfalt an bakteriellen Abstammungen auf, viele nur einmal nachgewiesen. Diese Diversität deutet auf ein komplexeres Geflecht aus lokalen Ausbrüchen, Umweltquellen und grenzüberschreitender Bewegung hin, statt auf ein oder zwei sich rasant ausbreitende Klone.
Wie die Bakterien Antibiotika austricksen
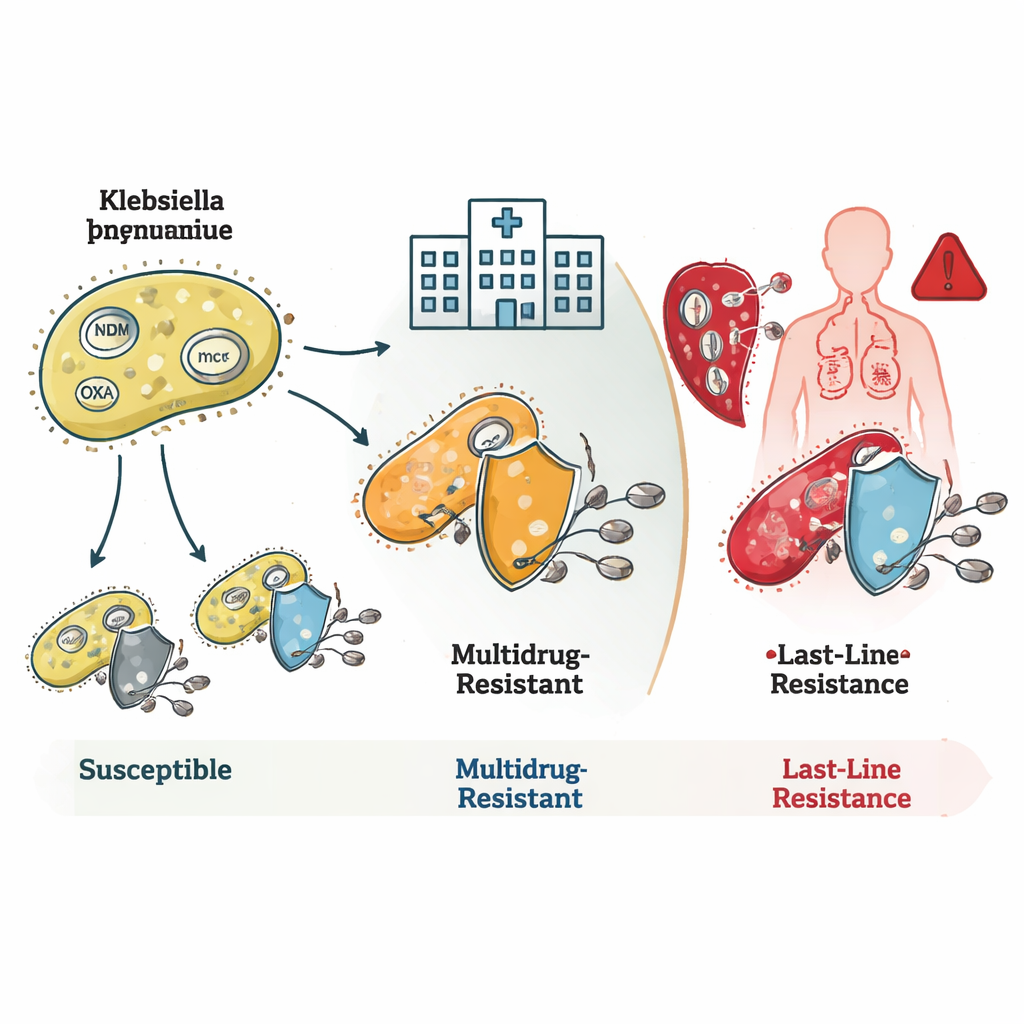
Die Studie zeigte, wie diese Bakterien mehrere Resistenzmechanismen kombinieren. Viele ST16‑ und ST231‑Stämme trugen Gene wie blaNDM und blaOXA, die Enzyme produzieren, welche Carbapenem‑Antibiotika zerstören, bevor diese wirken können. Einige wiesen zudem Veränderungen in ihrer äußeren Membran auf, die den Eintritt von Wirkstoffen reduzieren und so zusammen sehr hohe Resistenzen erzeugen. ST231‑Stämme trugen häufig zusätzlich das Gen rmtF1, das eine wichtige Wirkstoffgruppe, die Aminoglykoside, wirkungslos macht und die Therapieoptionen weiter einschränkt. ST147 fiel durch hohe genetische Flexibilität auf: Es kombinierte verschiedene Resistenzgene und Plasmide – kleine, mobile DNA‑Ringe – und wird so zu einem möglichen Knotenpunkt für die Weitergabe von Resistenzeigenschaften an andere Bakterien.
Versagen letzter Optionen und verborgene Gefahren
Der alarmierendste Befund betraf die Colistinresistenz, ein Medikament, das Ärztinnen und Ärzte für verzweifelte Situationen reservieren. Einige seltene Bakterienfamilien trugen mcr‑Gene, die über Plasmide zwischen Arten springen können und direkt Colistinresistenz vermitteln. Andere, insbesondere innerhalb des ST16‑Klonen, waren gegen Colistin resistent, obwohl sie keine bekannten Resistenzgene oder -mutationen trugen. Das deutet darauf hin, dass die Wissenschaft noch nicht alle Wege kennt, über die Bakterien dieses letzte wirksame Medikament neutralisieren können. Das Team identifizierte außerdem hypervirulente Stämme – Bakterien, die besonders gut schwere Erkrankungen verursachen können – darunter eine Linie, die hohe Virulenz mit Resistenz gegen alle getesteten Carbapeneme kombinierte, eine besonders gefährliche Kombination.
Warum genomische Überwachung wichtig ist
Um zu verstehen, wie genetische Veränderungen in realen Therapieversagen münden, nutzten die Forschenden statistische Modelle, um spezifische Resistenzgene mit tatsächlichen Laborergebnissen zu verknüpfen. Gene wie blaNDM‑1 und nahe Verwandte zeigten sehr starke Assoziationen mit Carbapenemresistenz und bestätigten so ihre zentrale Rolle bei Therapieversagen. Für Colistin jedoch zeigten die meisten resistenten Bakterien keine bekannten Resistenzmarker, was auf noch unerforschte Mechanismen hinweist. Die Autorinnen und Autoren argumentieren, dass der routinemäßige Einsatz von Ganzgenomsequenzierung in der Krankenhausüberwachung wie ein Frühwarnradar wirken kann: aufkommende Hochrisiko‑Klonen erkennen, ihre Ausbreitung über Regionen und Grenzen verfolgen und schnelle Infektionsschutzmaßnahmen lenken.
Was das für Patientinnen, Patienten und die Politik bedeutet
Für Laien ist die Botschaft klar und eindringlich: Einige Blutstrominfektionen in Thailand werden inzwischen von Bakterien verursacht, die nahezu gegen alle verfügbaren Medikamente resistent sind, und wenige gefährliche Familien dieser Mikroben breiten sich weit aus. Zugleich zeigt die Studie, dass Gesundheitssysteme mit den richtigen Werkzeugen – landesweiter Probenahme, genetischer Analyse und schneller Datenweitergabe – diese Bedrohungen früh erkennen und reagieren können. Der Ausbau genomischer Überwachung, die Entwicklung rascher molekularer Tests und strengere Infektionsschutzmaßnahmen könnten helfen, die Ausbreitung dieser Superkeime zu verlangsamen und Zeit für die Entwicklung neuer Therapien und Impfstoffe zu gewinnen.
Zitation: Krobanan, K., Kamjumphol, W., Leethongdee, P. et al. Nationwide genomic surveillance of carbapenem- and colistin-resistant Klebsiella pneumoniae bloodstream isolates in Thailand (2020–2024). Sci Rep 16, 5853 (2026). https://doi.org/10.1038/s41598-026-36228-4
Schlüsselwörter: antimikrobielle Resistenz, Klebsiella pneumoniae, Bakteriämie, genomische Überwachung, thailändisches Gesundheitswesen