Clear Sky Science · de
Abweichend exprimierte lange nichtkodierende RNAs bei der Differenzierung von aus Fettgewebe gewonnenen mesenchymalen Stammzellen zu nucleus-pulposus-ähnlichen Zellen
Warum Rückenschmerz und verdeckte RNA wichtig sind
Chronische Schmerzen im unteren Rücken gehören zu den Hauptgründen, warum Menschen krankheitshalber ausfallen oder einen Arzt aufsuchen. Eine zentrale Ursache ist der langsame Abbau der weichen Polster zwischen den Wirbelkörpern, den sogenannten Bandscheiben. Im Inneren jeder Bandscheibe befindet sich ein gallertartiger Kern, der Nucleus pulposus, der auf eine gesunde Population spezialisierter Zellen angewiesen ist, um elastisch und gut hydratisiert zu bleiben. Gehen diese Zellen verloren oder altern sie, trocknet die Bandscheibe aus, sackt zusammen und kann chronische Schmerzen auslösen. Forschende prüfen, ob Stammzellen — vielseitige Zellen, die sich in verschiedene Gewebe verwandeln können — so gelenkt werden könnten, dass sie diese abgenutzten Bandscheibenzellen ersetzen. Diese Studie stellt eine überraschend grundlegende Frage: Welche „stummen“ genetischen Signale schalten sich ein, wenn Stammzellen dazu gebracht werden, neue Bandscheibenzellen zu werden, und wie könnten diese Signale genutzt werden, um künftige Therapien zu verbessern?
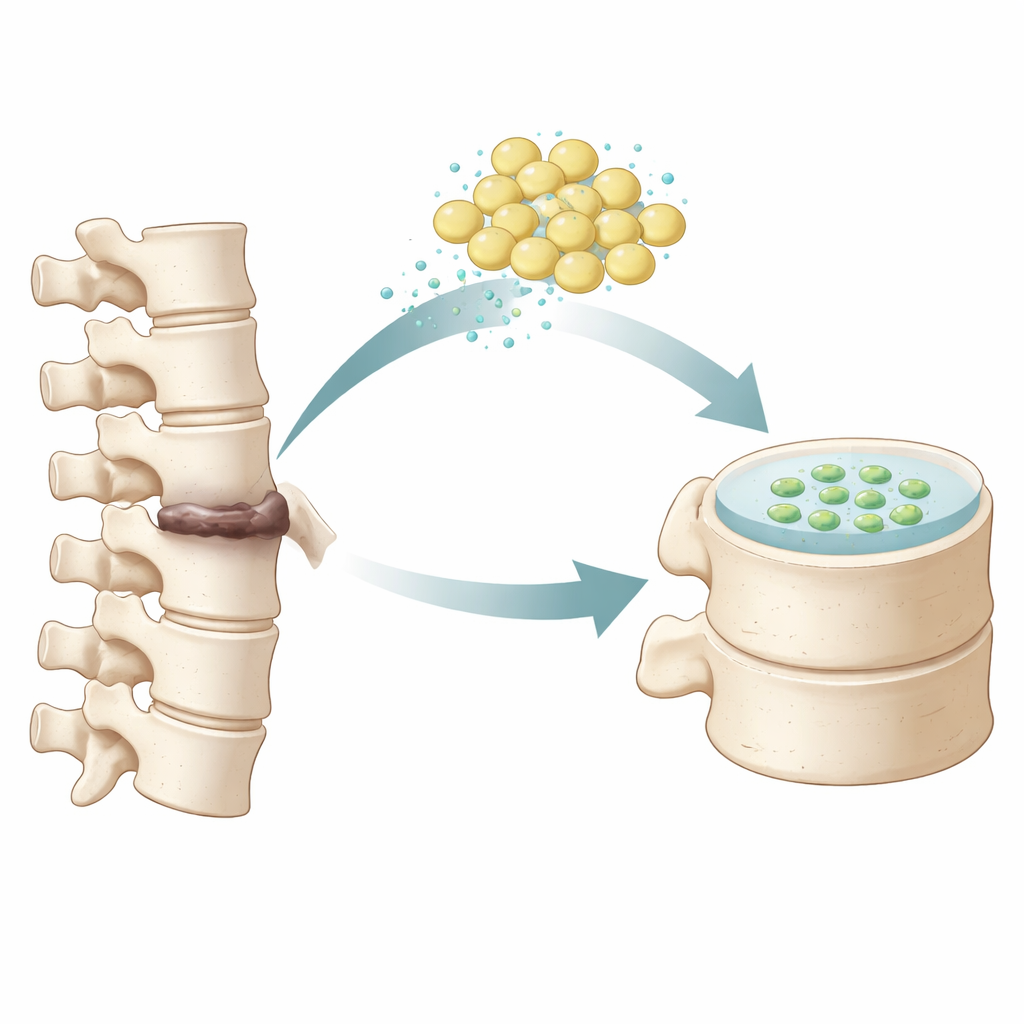
Vom Fettgewebe zur Bandscheibenreparatur
Die Forschenden konzentrierten sich auf menschliche aus Fettgewebe gewonnene mesenchymale Stammzellen, die relativ leicht zu gewinnen sind. Im Labor kultivierten sie diese Zellen in kleinen dreidimensionalen Pellets und setzten sie einer gezielt ausgewählten Mischung von Wachstumsfaktoren aus, die frühere Arbeiten als förderlich für eine Richtung hin zu einer nucleus-pulposus-ähnlichen Identität gezeigt hatten. Über mehrere Wochen überwachte das Team die Pellets mit üblichen mikroskopischen Färbungen und fluoreszenter Markierung. Die behandelten Zellen begannen, dem Aussehen und Verhalten der gallertartigen Kernzellen einer gesunden Bandscheibe ähnlicher zu werden: Sie produzierten typische Bestandteile des Bandscheibengewebes wie Kollagen und Aggrecan und schalteten Schlüsselgene ein, die mit der Identität von Nucleus-pulposus-Zellen verbunden sind.
Dem „Hintergrundgeplauder“ der Zelle lauschen
Neben den bekannten protein-kodierenden Genen produzieren Zellen auch lange nichtkodierende RNAs — RNA-Stücke, die keine Proteine herstellen, aber subtil steuern können, welche Gene ein- oder ausgeschaltet werden. Diese Moleküle treten zunehmend als wichtige Dirigenten im Orchester der Zelldifferenzierung hervor. Mit Hilfe hochdurchsatzfähiger RNA-Sequenzierung maß das Team sowohl traditionelle Boten-RNAs als auch lange nichtkodierende RNAs in Stammzellen, die eine bandscheibenähnliche Differenzierung durchliefen, und verglich sie mit undifferenzierten Kontrollzellen. Sie fanden weitreichende Umbauten der genetischen Landschaft: Die Aktivitätslevel von 500 langen nichtkodierenden RNAs und 601 Boten-RNAs veränderten sich, wobei einige stärker exprimiert und andere herunterreguliert wurden, als sich die Zellen in Richtung eines nucleus-pulposus-ähnlichen Zustands verschoben.
Wichtige Signalwege und Master-Regulatoren
Um diese umfangreiche Liste veränderter Moleküle zu interpretieren, nutzten die Wissenschaftler bioinformatische Werkzeuge, die Gene nach ihren zellulären Rollen gruppieren. Viele der veränderten Gene standen im Zusammenhang mit dem Aufbau und der Organisation der extrazellulären Matrix — dem Gefüge aus Kollagen, Zuckerbestandteilen und anderen Molekülen, das dem Bandscheibengewebe seine stoßdämpfenden Eigenschaften verleiht. Die Weganalyse hob die PI3K–Akt-Signalkaskade und Systeme hervor, die das zelluläre Zytoskelett steuern; diese scheinen während der Differenzierung besonders aktiv zu sein und deuten darauf hin, dass diese Schaltkreise die Umwandlung von aus Fett stammenden Stammzellen zu bandscheibenähnlichen Zellen antreiben. Durch den Aufbau von Interaktionsnetzwerken identifizierte das Team eine Reihe von langen nichtkodierenden RNAs — darunter MALAT1, MEG3, GAS5, ZNF331 und JARID2-assoziierte RNAs —, die offenbar als Knotenpunkte der Kommunikation zwischen regulatorischen RNAs, Boten-RNAs und microRNAs fungieren. Diese Hubs könnten als Hauptschalter wirken, die steuern, wie effizient Stammzellen sich auf ein bandscheibenähnliches Schicksal festlegen.
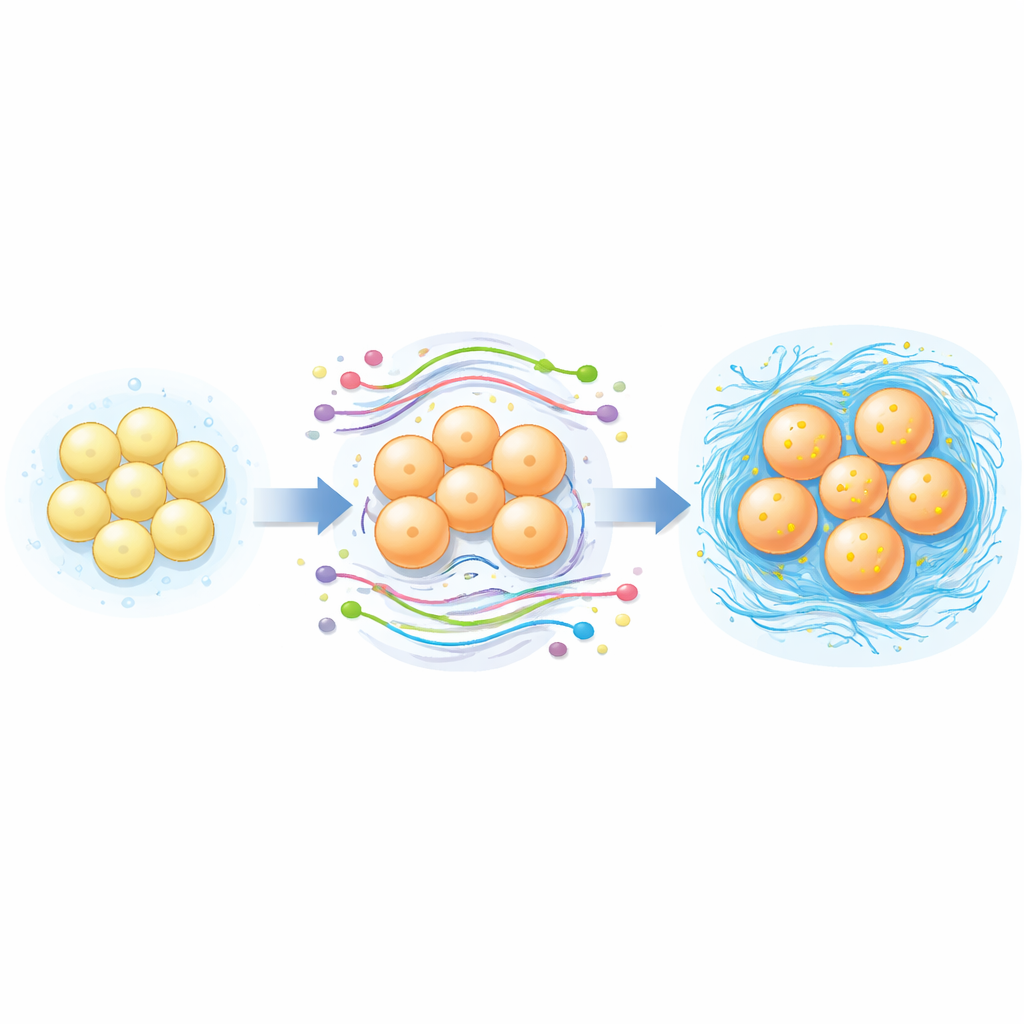
Hinweise für bessere Stammzelltherapien
Die Bandscheibendegeneration schafft ein besonders feindliches Umfeld — sauer, arm an Sauerstoff und reich an entzündlichen Molekülen —, das transplantierte Stammzellen behindern kann. Indem diese Studie kartiert, welche RNAs und Signalwege sich während der erfolgreichen Laborumwandlung von aus Fett gewonnenen Stammzellen in nucleus-pulposus-ähnliche Zellen ändern, liefert sie ein Verzeichnis molekularer Ziele, die angepasst werden könnten, um Überleben und Leistungsfähigkeit therapeutischer Zellen in echten Patienten zu verbessern. Obwohl die Arbeit in vitro und an einer begrenzten Anzahl von Proben durchgeführt wurde, legt sie den Grundstein für Folgeexperimente, die beispielsweise bestimmte lange nichtkodierende RNAs oder Signalwege modifizieren könnten, um die Bandscheibenregeneration zu verstärken.
Was das für Menschen mit Rückenschmerzen bedeutet
Für Menschen mit chronischen Rückenschmerzen werden diese Ergebnisse die Behandlung nicht sofort verändern, doch sie schließen ein wichtiges fehlendes Puzzleteil: wie Stammzellen lernen, genau die Art von Bandscheibenzellen zu werden, die für die Reparatur nötig sind. Die Studie zeigt, dass diese Umwandlung nicht nur von bekannten Genen geleitet wird, sondern auch von einem komplexen Netzwerk langer nichtkodierender RNAs und Signalwege, das das Verhalten der Zelle formt. Durch die Entschlüsselung dieser verborgenen Kontrollebene kommen Forschende dem Ziel näher, intelligentere Stammzelltherapien zu entwerfen, die der feindlichen Umgebung beschädigter Bandscheiben besser standhalten und deren stoßdämpfenden Kern zuverlässiger wiederaufbauen können — womit sie möglicherweise in Zukunft länger anhaltende Linderung bieten.
Zitation: Zhu, J., Jin, L., Jin, K. et al. Aberrantly expressed long noncoding RNAs in adipose-derived mesenchymal stem cells differentiation to nucleus pulposus-like cells. Sci Rep 16, 8029 (2026). https://doi.org/10.1038/s41598-026-36219-5
Schlüsselwörter: Bandscheibendegeneration, Stammzelltherapie, Nucleus-pulposus-Zellen, lange nichtkodierende RNA, RNA-Sequenzierung