Clear Sky Science · de
Cubosomale Nanopartikel von Lycopin als neuartige Plattform zur Verbesserung von Antioxidans- und Antikrebs‑Eigenschaften mit einer Molekulardocking‑Studie
Tomatenkraft in einem winzigen Paket
Viele Menschen haben gehört, dass der Verzehr von Tomaten vor Krebs schützen kann, dank eines roten Pigments namens Lycopin. Allein ist Lycopin jedoch schwer vom Körper aufzunehmen und erreicht Tumoren nicht besonders effektiv. Diese Studie untersucht einen cleveren Umweg: Lycopin wird in ultrakleine, fettbasierte Partikel — sogenannte Cubosomen — verpackt, um zu prüfen, ob diese „eingeschrumpfte Tomatenkraft“ in Zellkultur besser gegen Dickdarmkrebszellen wirken kann.
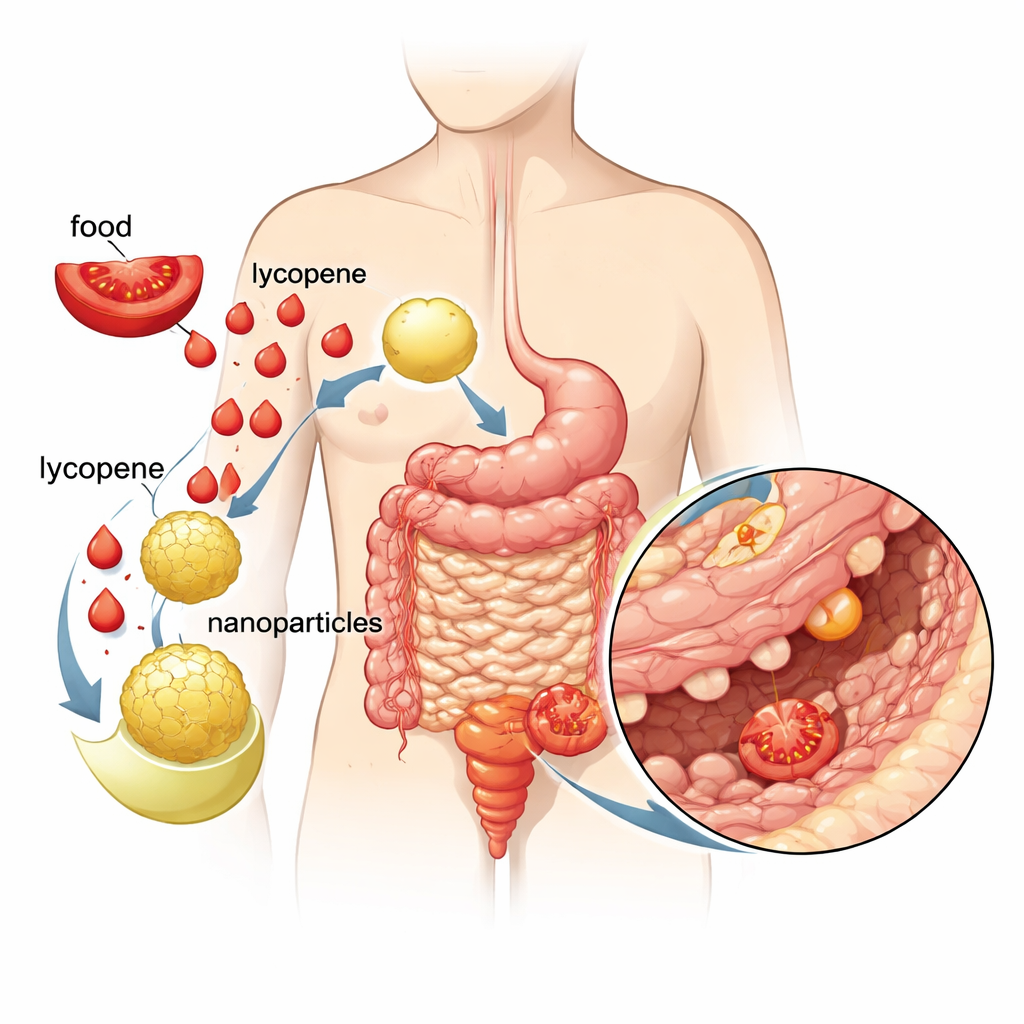
Warum gewöhnliches Lycopin versagt
Lycopin ist ein starkes natürliches Antioxidans, das in Tomaten, Wassermelonen und anderen roten Früchten vorkommt. Es kann schädliche Moleküle, sogenannte freie Radikale, neutralisieren, die DNA, Proteine und Fette in unseren Zellen schädigen und zu chronischen Erkrankungen wie Krebs und Herzkrankheiten beitragen. Allerdings ist Lycopin extrem fettlöslich und löst sich nur schlecht in wasserbasierten Flüssigkeiten wie denen unseres Verdauungssystems. Deshalb gelangt nur ein Bruchteil dessen, was wir essen, tatsächlich ins Blut und zu den Zielgeweben. Diese schlechte Löslichkeit und Instabilität begrenzen Lycopins Nützlichkeit als praktische Therapie, obwohl sein Schutzpotenzial gut dokumentiert ist.
Ein besserer Träger
Um diese Hürden zu überwinden, entwickelten die Forscher cubosomale Nanopartikel — winzige, weiche Partikel aus biokompatiblen Lipiden und Stabilisatoren, die sich zu einer schwamm‑ bzw. wabenartigen Innenstruktur anordnen. Diese Strukturen können fettlösliche Moleküle wie Lycopin einschließen, sie vor Abbau schützen und graduell freisetzen. In dieser Arbeit luden die Forscher Lycopin erfolgreich in Cubosomen von etwa 150 Nanometern Durchmesser, wobei der Großteil des Lycopins effizient eingeschlossen war. Tests zeigten, dass mehr als drei Viertel des Lycopins innerhalb von 15 Minuten in Lösung freigesetzt wurden — eine dramatische Verbesserung im Vergleich zu freiem Lycopin, das sich kaum in Wasser löst.
Prüfung der antioxidativen und krebsbekämpfenden Wirkung
Die Wissenschaftler verglichen dann freies Lycopin und Lycopin‑Cubosomen auf zwei Arten. Zuerst maßen sie, wie gut jede Form freie Radikale mit Standardtests für Antioxidantien neutralisieren kann. In beiden Tests waren für die nanoverpackte Form deutlich geringere Mengen nötig, um denselben antioxidativen Effekt zu erzielen, was auf eine viel stärkere Aktivität hinweist. Zweitens setzten sie humane Darmkrebszellen (HT‑29) beiden Formen aus. Mithilfe eines Standardtests zur Zellvitalität fanden sie, dass cubosomales Lycopin Krebszellen effizienter abtötete als freies Lycopin — es waren niedrigere Dosen nötig, um das Zellwachstum zu halbieren. Flow‑Cytometrie‑Experimente zeigten, dass die Nanopartikel‑Form deutlich mehr Zellen in eine Ruhephase drängte, in der sie sich nicht teilen, und einen ausgeprägten Anstieg programmierter Zellsterblichkeit (Apoptose) im Vergleich zu unbehandelten Zellen auslöste.
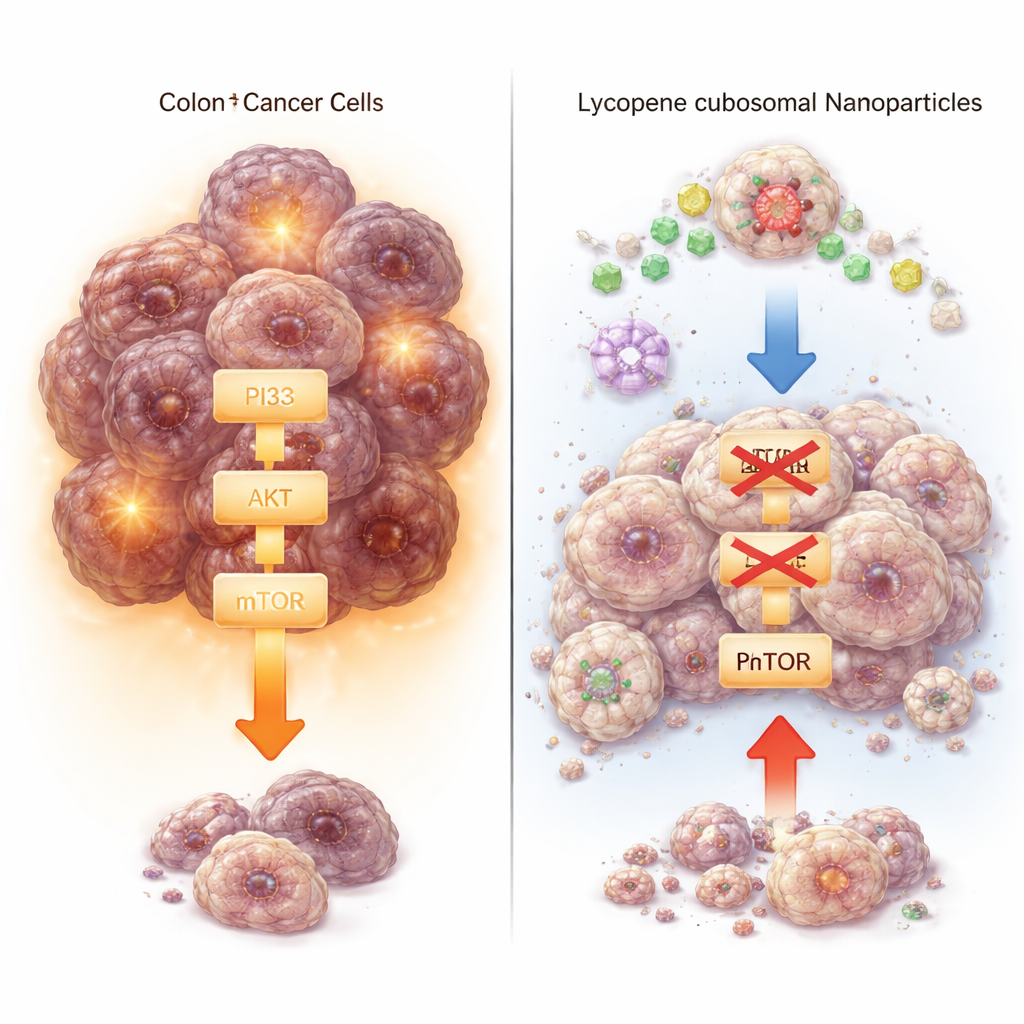
Einblick in die zellulären Kontrollschaltungen
Über das bloße Zählen überlebender Zellen hinaus untersuchten die Forscher zentrale molekulare Schalter, die Wachstum und Tod steuern. Sie konzentrierten sich auf den PI3K–AKT–mTOR‑Signalweg, eine Signalkette, die Krebszellen häufig nutzen, um zu überleben und sich zu vermehren, sowie auf Proteine, die entweder das Zelltodprogramm fördern oder blockieren. Mit Genexpressionsanalysen und Proteinmessungen fanden sie, dass sowohl freies Lycopin als auch Lycopin‑Cubosomen PI3K, AKT, mTOR und das Überlebensprotein Bcl‑2 herunterregulierten, während sie die für den Zelltod verantwortliche Enzymaktivität von Caspase‑3 erhöhten. Diese Veränderungen waren bei der cubosomalen Form durchgängig stärker. Computergestützte Docking‑Simulationen stützten die Idee, dass Lycopin in die aktive Tasche von PI3K passen kann, was einen direkten Mechanismus nahelegt, wie es diesen Wachstumsweg stören könnte.
Was das für künftige Behandlungen bedeuten könnte
Kurz gesagt: Das Einpacken von Lycopin in cubosomale Nanopartikel machte es leichter löslich, stabiler und in Labortests deutlich wirksamer. Die Nanoform neutralisierte nicht nur schädliche Moleküle effektiver, sondern schaltete auch Wachstumssignale von Krebszellen herunter und förderte deren Selbstzerstörung. Da diese Ergebnisse aus Zellkulturen und Computermodellen stammen — nicht aus Patientenstudien — deuten sie auf eine vielversprechende Strategie hin: den Einsatz intelligenter, fettbasierter Nanopartikel, um eine bekannte ernährungsbedingte Verbindung in eine gezielte Unterstützung gegen Darmkrebs zu verwandeln. Wenn zukünftige Tier‑ und klinische Studien diese Vorteile und die Sicherheit bestätigen, könnten Lycopin‑Cubosomen bestehende Therapien ergänzen, indem sie einen schonenderen, naturnahen Weg bieten, die antioxidativen Abwehrkräfte zu unterstützen und Tumorzellen zu schwächen.
Zitation: Alsunbul, M., El-Masry, T.A., El-Bouseary, M.M. et al. Cubosomal nanoparticles of lycopene as a novel platform for enhancement in antioxidant and anticancer properties with a molecular docking study. Sci Rep 16, 5941 (2026). https://doi.org/10.1038/s41598-026-36217-7
Schlüsselwörter: lycopin, nanopartikel, kolorektales Karzinom, Antioxidantien, Arzneimittel‑Freisetzung