Clear Sky Science · de
Pyridinium- und bromsubstituierte distyryl-BODIPY-Farbstoffe für mitochondriengezielte photodynamische Therapie
Krebszellen von innen zum Leuchten bringen
Die photodynamische Therapie ist eine Krebsbehandlung, bei der lichtaktivierbare Wirkstoffe eingesetzt werden, um Tumorzellen zu töten und dabei weitgehend gesundes Gewebe zu schonen. Diese Studie untersucht eine neue Familie fluoreszierender Farbstoffe, die gezielt die Kraftwerke der Zelle — die Mitochondrien — ansteuern sollen und bei Bestrahlung mit tiefrotem Licht toxische Sauerstoffspezies erzeugen können, die Krebszellen zerstören. Die Arbeit zeigt sowohl das Potenzial als auch die Fallstricke beim molekularen Design solcher Farbstoffe.
Warum die Kraftwerke der Zelle anvisieren?
Mitochondrien sind entscheidend für die Energieerzeugung und spielen eine Rolle dabei, ob eine Zelle überlebt oder zugrunde geht. Krebszellen weisen oft eine stärker geladene mitochondriale Membran auf als normale Zellen, wodurch sie positiv geladene Moleküle stärker anziehen. Die Forschenden nutzten dies, indem sie eine positiv geladene Pyridiniumgruppe an das bekannte fluoreszierende BODIPY-Gerüst ankoppelten. Dieses Design lenkt die Farbstoffe in die Mitochondrien, wo lichtausgelöste chemische Reaktionen maximalen Schaden an Krebszellen anrichten können, während andererorts wenig Schaden entsteht.
Intelligentere lichtaktivierte Farbstoffe entwerfen
Das Team entwickelte drei eng verwandte Farbstoffe, genannt PyBHI, PyBMI und PyBBrI, die sich hauptsächlich in der Anzahl der Bromatome unterscheiden (keine, eins bzw. zwei). Alle besitzen eine lange, ausgedehnte Struktur, die ihre Lichtabsorption und -emission in den nahen Infrarotbereich verschiebt — ein nützliches Fenster, in dem Licht tiefer in Gewebe eindringen kann. Theoretisch könnten diese Farbstoffe zwei interne Wege nutzen, um einen „Triplett“-angeregten Zustand zu erreichen, der reaktiven Singulett-Sauerstoff erzeugt: einen durch die schweren Bromatome und einen durch eine vorübergehende Verschiebung der elektrischen Ladung innerhalb des Moleküls. 
Wenn Theorie auf experimentelle Realität trifft
Trotz des eleganten Designs zeigten ausführliche Tests, dass die Farbstoffe nicht so effizient Singulett-Sauerstoff erzeugten wie erhofft. Mit chemischen Sonden, die beim Reagieren mit Singulett-Sauerstoff ihre Farbe verlieren, bestimmten die Forschenden sehr geringe Sauerstoffbildungs-Ausbeuten für alle drei Farbstoffe, mit nur moderater Verbesserung bei zunehmender Bromierung. Ultraschnelle Laserexperimente erklärten das: Nach Lichtabsorption gelangen die Farbstoffe schnell in ladungsverschobene Zustände, die überwiegend harmlos als Wärme relaxieren, statt in den gewünschten Triplett-Zustand überzugehen. In den bromierten Varianten öffnen die schweren Atome zwar einen Pfad zum Triplett-Zustand, dieser ist aber deutlich langsamer als der konkurrierende Energieverlust und begrenzt so die Gesamtwirkungsrate.
Gezielter Angriff auf Tumormitochondrien in lebenden Zellen
In einem biologischen Umfeld ändert sich das Bild. In kultivierten menschlichen Brust-(MCF-7) und Gebärmutterhals-(HeLa)-Krebszellen zeigten konfokale Mikroskopieaufnahmen, dass sich alle drei Farbstoffe stark in den Mitochondrien anreichern und mit einem Standard-Mitochondrienstainer kolokalisieren. Toxizitätstests im Dunkeln deuteten darauf hin, dass die Farbstoffe ohne Licht weitgehend unschädlich sind. Unter Rotlichtbestrahlung jedoch verursachte der di-bromierte Farbstoff PyBBrI erheblichen Zelltod, wobei bereits niedrige Nanomolar-Dosen die Zellviabilität halbierten. Die beiden anderen Farbstoffe waren deutlich weniger wirksam. 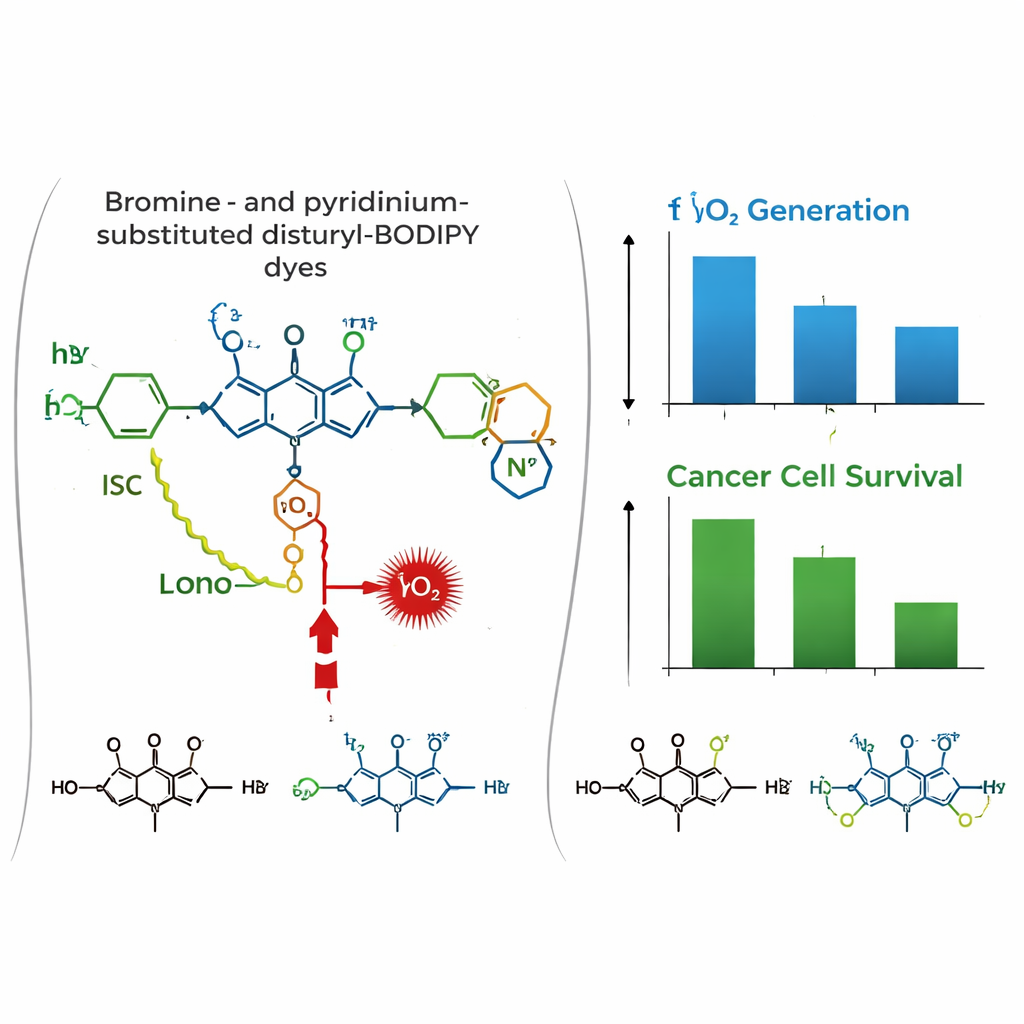
Was das für künftige Krebstherapien bedeutet
Für Nichtfachleute lautet die Kernbotschaft: Kleine chemische Veränderungen können das Verhalten lichtaktivierter Krebswirkstoffe drastisch verändern, und ihre Wirksamkeit in realen Zellen kann besser — oder schlechter — sein als aus einfachen Messungen vorhergesagt. In diesem Fall zeigte der am stärksten modifizierte Farbstoff PyBBrI im Reagenzglas nur mäßige Bildung reaktiven Sauerstoffs, erwies sich aber als hochwirksam gegen Krebszellen, sobald er deren Mitochondrien erreichte. Die Arbeit unterstreicht sowohl die Bedeutung, Wirkstoffe gezielt an verwundbare Strukturen innerhalb von Krebszellen zu lenken, als auch die Komplexität der Vorhersage photodynamischer Effizienz. Sie weist den Weg zu nächsten Generationen mitochondriengezielter Therapien, die nahinfrarotes Licht nutzen, um die zellabtötende Chemie genau dort selektiv „einzuschalten“, wo sie gebraucht wird.
Zitation: Kim, C., Badon, I.W., Jo, J. et al. Pyridinium- and bromine-substituted distyryl-BODIPY dyes for mitochondria-targeted photodynamic therapy. Sci Rep 16, 6789 (2026). https://doi.org/10.1038/s41598-026-36213-x
Schlüsselwörter: photodynamische Therapie, mitochondriengezielte Farbstoffe, BODIPY, Singulett-Sauerstoff, Krebszellen