Clear Sky Science · de
γ-Strahlung induziert regionsspezifische subzelluläre Veränderungen von Markern der amyotrophen Lateralsklerose und frontotemporalen Demenz im Schweinehirn
Warum winzige Strahlendosen und Schweinehirne wichtig sind
Die meisten von uns verbinden Strahlung instinktiv mit Schaden, besonders für das Gehirn. Doch unsere Umwelt enthält immer niedrige Strahlungsdosen aus medizinischen Untersuchungen, Flugreisen und natürlichen Quellen. Gleichzeitig rätseln Wissenschaftler noch immer darüber, was die amyotrophe Lateralsklerose (ALS) — die tödliche Krankheit, die Baseballstar Lou Gehrig lähmte — und die nahe verwandte frontotemporale Demenz (FTD), die Verhalten und Persönlichkeit angreift, auslöst. Die Studie stellt eine überraschend hoffnungsvolle Frage: Könnte eine einmalige, moderate Dosis Gamma‑Strahlung die Gehirnchemie so verändern, dass die Effekte nicht rein schädlich sind und vielleicht sogar schützend gegenüber molekularen Veränderungen wirken, die mit ALS und FTD assoziiert sind?
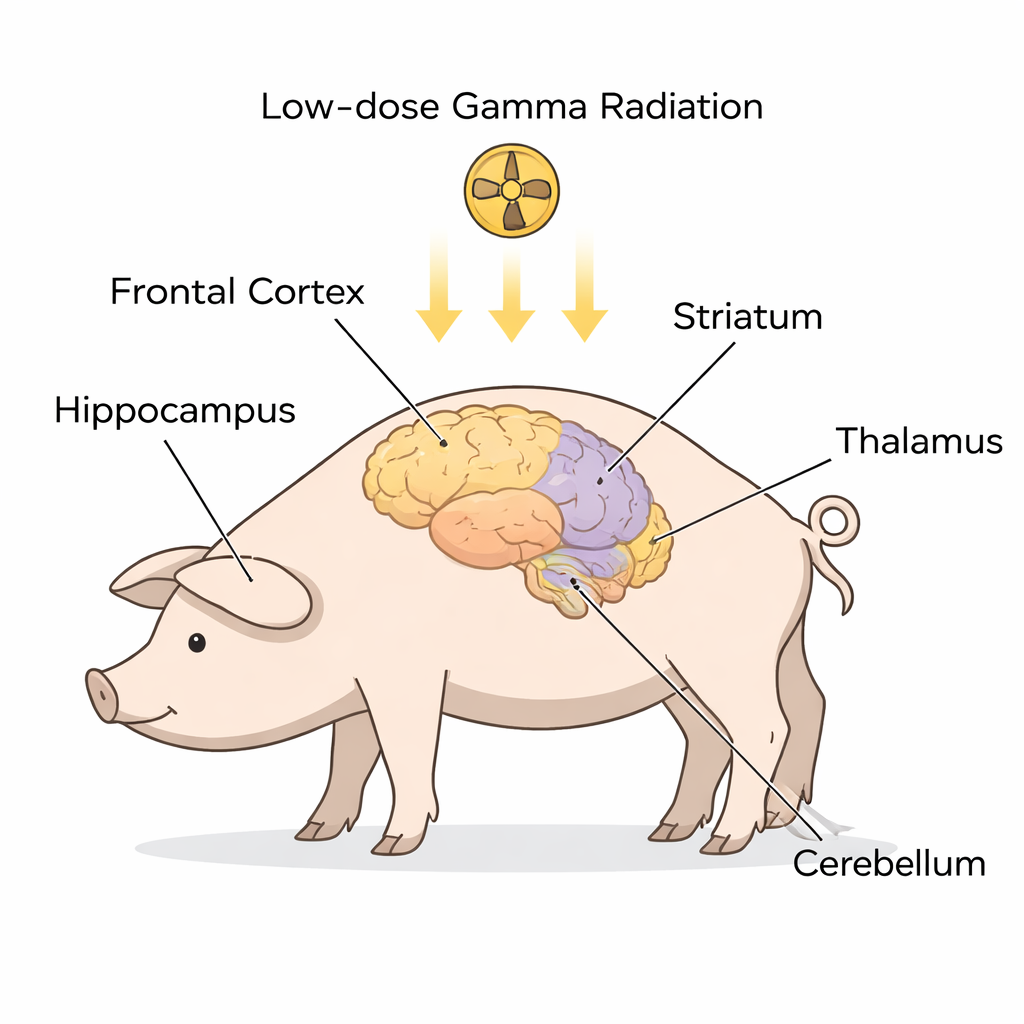
Ein genauerer Blick auf ALS‑Warnzeichen im Gehirn
Anstatt Patientinnen und Patienten mit bereits manifestem ALS zu untersuchen, arbeiteten die Forschenden mit gesunden Göttinger Minischweinen, deren Gehirne anatomisch unserem ähnlich sind. Neun Tiere erhielten einmalig eine Ganzkörper‑Exposition mit niedrig dosierter Gamma‑Strahlung, sechs wurden narkotisiert, aber nicht bestrahlt und dienten als Kontrollen. Etwa einen Monat später sezierte das Team fünf Schlüsselregionen des Gehirns, die häufig bei ALS und FTD betroffen sind — den Frontalkortex, Hippocampus, Striatum, Thalamus/Hypothalamus und das Kleinhirn. In jeder Region trennten sie das Zellmaterial in zwei Hauptkompartimente: das Zytoplasma (die flüssige Innenraum der Zelle) und den Zellkern (das Kompartiment, das die DNA enthält). Mittels Western‑Blot maßen sie die Konzentrationen mehrerer Proteine, die stark mit ALS und ALS‑FTD verbunden sind, darunter SOD1, FUS, C9orf72, STMN2, Ubiquitin, TDP‑43 und eine modifizierte Form, die phosphorylierte TDP‑43.
Strahlung lässt einige Marker unverändert — andere verschoben
Eine beruhigende Beobachtung war, dass die Gesamtmengen von SOD1, einem Protein, dessen Mutationen bei manchen erblichen Formen von ALS ursächlich sind, in keiner Region nach der Bestrahlung verändert waren. Ebenso blieben die Hauptformen von TDP‑43 — das Protein, das am häufigsten in ALS‑assoziierten Proteinaggregaten gefunden wird — sowohl im Kern als auch im Zytoplasma über alle Regionen hinweg stabil. Doch nicht alles war statisch. Das Team beobachtete regionsspezifische und kompartimentspezifische Verschiebungen bei mehreren anderen Proteinen. So nahm beispielsweise FUS, ein Protein, das normalerweise im Zellkern lokalisiert ist, aber bei ALS fehlgelenkt verklumpen kann, im Zytoplasma des Thalamus/Hypothalamus nach Strahlung ab, während seine Kernlevel im Frontalkortex anstiegen und im Hippocampus sanken. Das ALS‑assoziierte Protein C9orf72 veränderte sich nicht im Zytoplasma, zeigte jedoch einen Rückgang in den Kernkompartimenten des Hippocampus. Auch STMN2, ein Protein, das für die Aufrechterhaltung von Nervenfasern wichtig ist, nahm in den Hippocampuskernen ab, was auf eine koordinierte Reaktion dieser beiden Moleküle in jener memory‑bezogenen Region hindeutet.
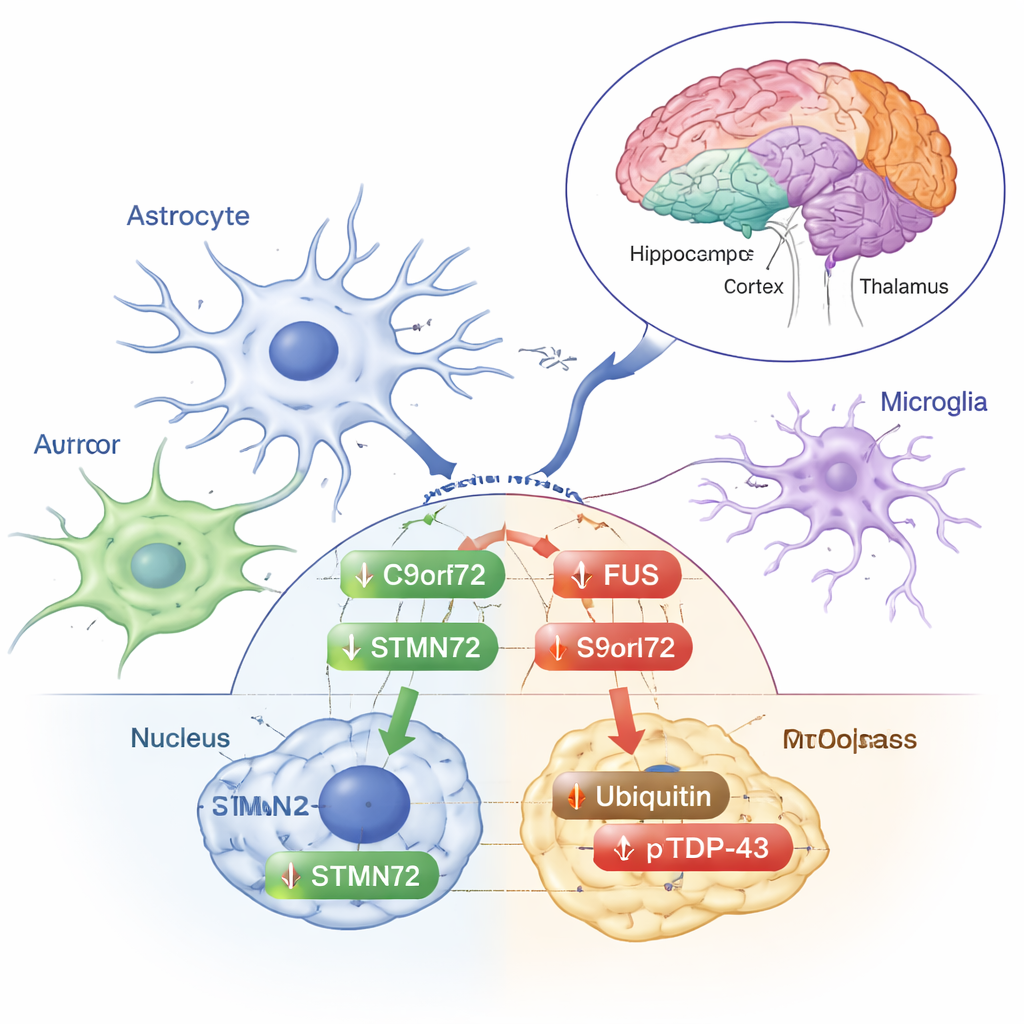
Stresssignale oder früher Schutz?
Andere Veränderungen erinnerten eher an klassische Stressreaktionen. Ubiquitin — das kleine Markierungsprotein, das die Zelle verwendet, um beschädigte Proteine für den Abbau zu kennzeichnen — nahm in der zytoplasmatischen Fraktion des Frontalkortex zu. Die phosphorylierte Form von TDP‑43, die oft in den abnormalen Ablagerungen bei ALS und FTD angereichert ist, stieg im Zytoplasma des Frontalkortex, Striatums und Thalamus/Hypothalamus an, obwohl das Gesamt‑TDP‑43 unverändert blieb. Diese Verschiebungen deuten darauf hin, dass niedrig dosierte Strahlung die Protein‑Handhabung der Zelle anstößt, ohne die vollständigen Muster von Fehlfaltung und Aggregation auszulösen, die die Krankheit definieren. Die Autorinnen und Autoren betonen, dass diese Reaktionen je nach Gehirnregion und danach, ob ein Protein innerhalb oder außerhalb des Kerns liegt, variieren — ein Hinweis auf die fein abgestimmte Reaktion des Gehirns auf Stress.
Was das für das ALS‑Risiko — und mögliche Vorteile — bedeuten könnte
Bedeutet das, dass niedrig dosierte Strahlung ALS verursacht? Die Daten sprechen gegen ein simples Ja. Die Forschenden fanden weder die charakteristische Fehlverlagerung noch die Anhäufung der wichtigsten ALS‑Proteine, und viele Veränderungen deuteten eher auf veränderte Regulation als auf direkten Schaden hin. Interessanterweise fügen sich die Ergebnisse in frühere Arbeiten derselben Gruppe und anderer ein, die nahelegen, dass kleine Strahlendosen manchmal eine sogenannte Hormesis auslösen können — ein Phänomen, bei dem milde Stressoren Reparaturwege aktivieren und schädliche Proteine reduzieren, etwa solche, die mit Alzheimer oder Parkinson assoziiert sind, in Tiermodellen. Die vorliegende Studie deutet darauf hin, dass zumindest kurzfristig eine einmalige niedrige Gamma‑Dosis ALS‑assoziierte Marker in Richtungen verschiebt, die adaptiv statt destruktiv sein könnten.
Große Fragen und vorsichtiger Optimismus
Für nicht‑fachliche Leserinnen und Leser ist die wichtigste Erkenntnis, dass das Verhältnis von Strahlung und Gehirngesundheit nuancierter ist als «alle Strahlung ist schlecht». In diesem Großtiermodell erzeugte die niedrig dosierte Gamma‑Exposition subtile, regionsspezifische Verschiebungen von Proteinen, die mit ALS und FTD verknüpft sind, ohne die schädlichen Muster zu reproduzieren, die in Patientenhirnen beobachtet werden. Diese Veränderungen könnten die Versuche des Gehirns widerspiegeln, mit Stress umzugehen und zu reparieren, und in einigen Fällen sogar vorteilhaft sein. Allerdings wurde nur einen Monat nach einer einzigen Exposition und ausschließlich im Gehirn (nicht im Rückenmark, wo ALS am stärksten zuschlägt) untersucht. Langzeit‑ und Wiederholungsdosisstudien sind nötig, bevor man an eine Übersetzung dieser Befunde auf Menschen denkt. Dennoch eröffnet diese Arbeit ein neues Fenster darauf, wie alltägliche Strahlungsniveaus mit den Molekülen interagieren, die schweren neurodegenerativen Erkrankungen zugrunde liegen — und sie wirft die Möglichkeit auf, dass in kontrollierten Settings kleine Dosen eines Tages genutzt werden könnten, um die eigenen Abwehrmechanismen des Gehirns zu stimulieren.
Zitation: Iacono, D., Murphy, E.K., Perl, D.P. et al. γ-Radiation induces region-specific subcellular alterations of amyotrophic lateral sclerosis and frontotemporal dementia markers in swine brain. Sci Rep 16, 5627 (2026). https://doi.org/10.1038/s41598-026-36208-8
Schlüsselwörter: amyotrophe Lateralsklerose, frontotemporale Demenz, niedrigdosierte Strahlung, Gehirnproteine, Minischweinmodell