Clear Sky Science · de
Das Lyses-Kassettchen des Jumbophagen PhiKZ
Wie Riesenviren Bakterien aufreißen
Viren, die Bakterien infizieren – Bakteriophagen oder kurz Phagen genannt – werden als präzise Waffen gegen gefährliche Infektionen wie jene durch Pseudomonas aeruginosa, einen Krankenhaus-Superkeim, erforscht. Ein besonders großer Phage, phiKZ, beschäftigt die Wissenschaftler, weil er in seinem Wirt ein schützendes „nucleus-ähnliches“ Kompartiment aufbaut. Bisher war jedoch unklar, wie dieser Riesenphage den Wirt schließlich aufbricht, um zu entkommen. Diese Studie enthüllt die Genmenge und die molekularen Werkzeuge, die phiKZ verwendet, um den finalen explosiven Schritt zeitlich zu steuern und durchzuführen.
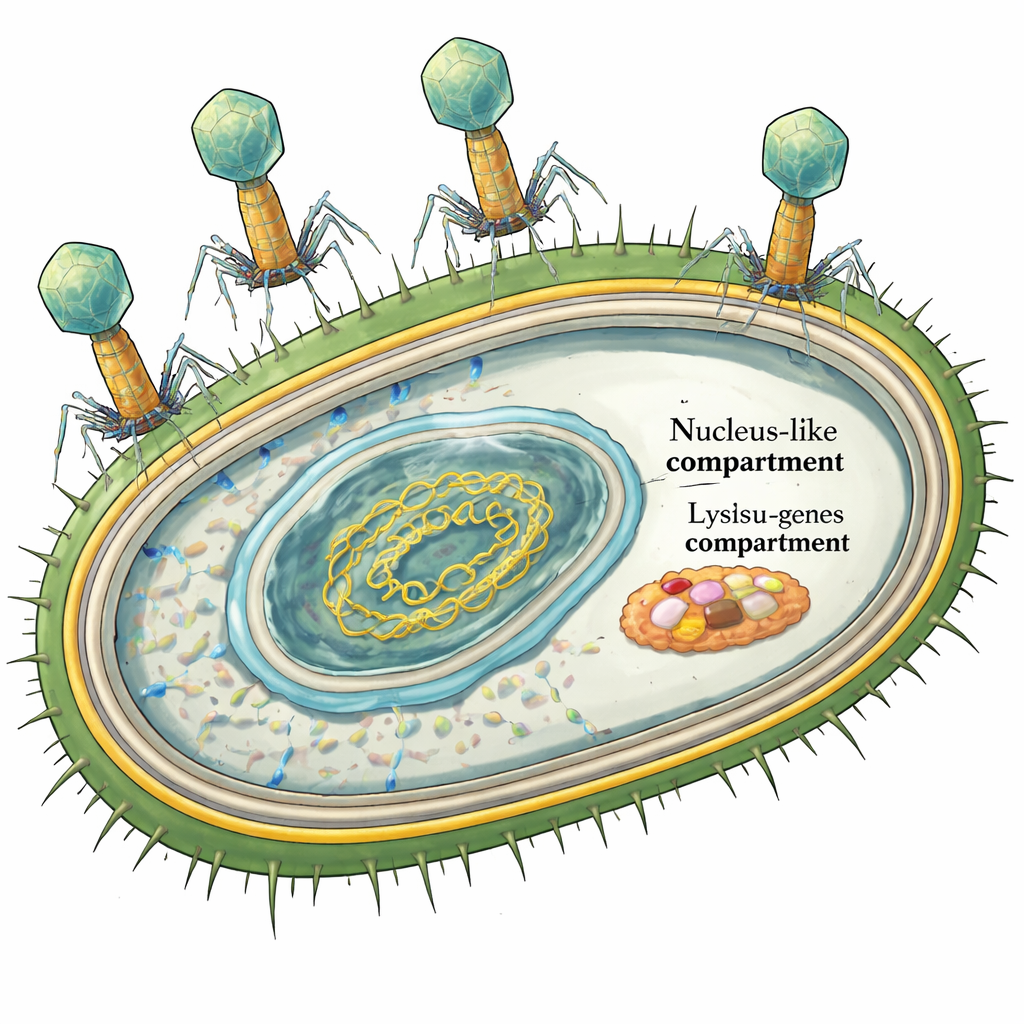
Der Riesenphage und sein Fluchtplan
PhiKZ ist ein „Jumbo“-Phage mit einem Genom von mehr als 200.000 DNA-Basen. Frühere Arbeiten zeigten detailliert, wie er seine DNA in einer Proteinhülle versteckt, um bakterielle Abwehrmechanismen zu umgehen. Der letzte Akt der Infektion – die kontrollierte Zerstörung der bakteriellen Zelle – blieb jedoch ein Rätsel. Die meisten Phagen, die Bakterien mit zwei Membranen infizieren, wie Pseudomonas, nutzen ein vierteiliges Lyse-System: ein Protein durchsticht die innere Membran, ein weiteres zersetzt die Zellwand, und ein zweiteiliges Komplex sorgt für das Kollabieren der äußeren Membran. Da im Genom von phiKZ kein erkennbares „Loch-bildendes“ Gen auffiel, schlugen manche Forscher vor, er könnte eine gänzlich andere Strategie verwenden, um sein wandspaltendes Enzym an die richtige Stelle zu bringen.
Das versteckte Lyse-Werkzeug finden
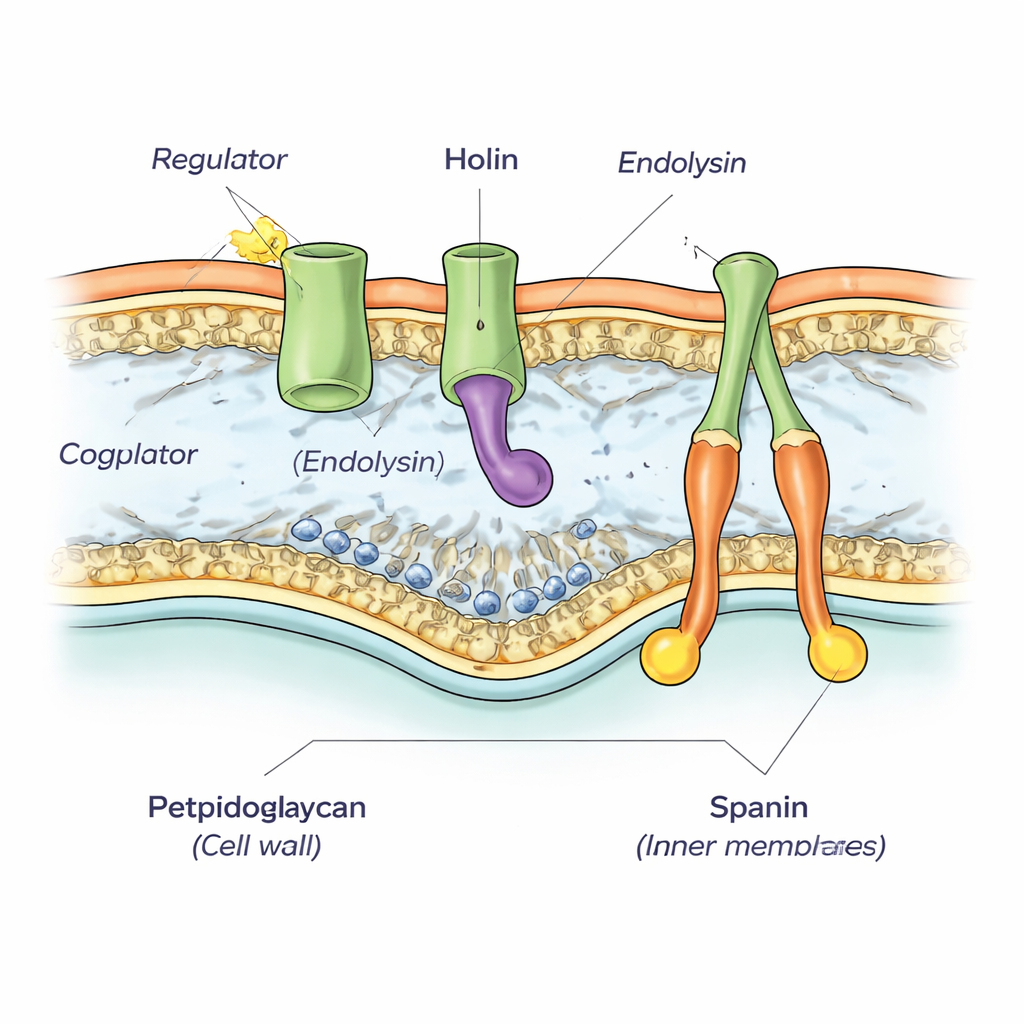
Durch eine erneute Untersuchung der Region des phiKZ-Genoms um ein bekanntes wandzersetzendes Enzym (Endolysin) entdeckten die Autoren einen dicht gepackten Cluster von fünf Genen. Mittels Sequenzanalyse und Computerprognosen zeigten sie, dass zwei dieser Gene die Spanine kodieren, ein Proteinpaar, das innere und äußere Membran verbindet und später deren Fusion unterstützt. Ein weiteres Gen kodiert das Endolysin selbst. Ein viertes Gen erwies sich als das fehlende Holin – das Protein, das sich leise in der inneren Membran ansammelt, bevor es plötzlich große Poren öffnet. Die Forscher bestätigten diese Funktionen experimentell, indem sie phiKZ-Gene in gut untersuchte Lambda-Phagen- und Escherichia-coli-Systeme transplantierten und zeigten, dass die phiKZ-Versionen fehlende Teile ersetzen konnten.
Ein Zeitpunkt-Schalter für die Zerstörung der Zelle
Das fünfte Gen im Cluster kodiert ein kleines Protein, das im bakteriellen Zytoplasma verbleibt, statt sich in einer Membran einzufügen. Als die Autoren dieses Protein zusammen mit dem Holin in E. coli exprimierten, starben die Zellen merklich früher als beim Holin allein, obwohl der Rest der Lyse-Maschinerie fehlte. Das deutet darauf hin, dass das zusätzliche Protein als Regulator wirkt und das Holin zu früherer oder verstärkter Porenbildung anstupst. Als das Team Abschnitte des langen, nach innen gerichteten Schwanzs des Holins entfernte, konnte der Regulator die Beschleunigung nicht mehr bewirken und blockierte in einigen Fällen sogar die Lyse. Strukturelle Modelle, erzeugt mit AlphaFold-Software, unterstützten eine physische Partnerschaft zwischen dem inneren Schwanz des Holins und dem Regulator, die einen stabilen Zwei-Protein-Komplex bilden.
Hinweise auf einen Verzögerungsmechanismus bei hoher Virusdosis
Als die Forscher Bakterienkulturen mit unterschiedlichen Mengen an phiKZ-Partikeln infizierten, fiel ihnen ein interessantes Muster auf. Bei niedriger Virusdosis lysierte die Kultur relativ schnell und scharf. Bei hoher Dosis verzögerte sich die Lyse jedoch und zog sich über mehr als zwei Stunden hin. Diese kontraintuitive Verlangsamung erinnert an ein klassisches Phänomen namens Lysis-Inhibition, bekannt von einem anderen Phagen namens T4, bei dem zusätzliche Infektionen das Virus veranlassen, das Aufplatzen der Zelle aufzuschieben, damit mehr Partikel produziert werden können. Weil phiKZ ein Holin-Regulator-Paar besitzt, das sowohl die Lyse vorantreiben als auch unter bestimmten Bedingungen blockieren kann, schlagen die Autoren vor, dass ein ähnliches Verzögerungssystem auch bei diesem Jumbophagen existieren könnte.
Warum das für die Phagentherapie wichtig ist
Indem gezeigt wird, dass phiKZ eine konventionelle, aber ausgefeilte Lyse-Kassette trägt – mit Holin, Endolysin, Spaninen und einem Zeitregulator – demonstriert diese Arbeit, dass selbst exotische Jumbophagen auf vertraute Werkzeuge zurückgreifen, um aus ihren Wirten zu eruieren. Für Nicht-Spezialisten ist die Kernaussage: Das „Ausbruchs-Timing“ therapeutischer Phagen lässt sich durch kleine regulatorische Proteine beeinflussen, die mit den porenbildenden Holinen kommunizieren. Das Verständnis und die mögliche gezielte Veränderung dieser Zeitgeber könnten helfen, Phagenbehandlungen zu entwerfen, die Bakterien entweder so schnell wie möglich töten oder, wenn es vorteilhaft ist, die Lyse hinauszögern, um vor dem finalen Schlag die virale Vermehrung zu maximieren.
Zitation: Manohar, P., Wan, J., Ganser, G. et al. The Lysis cassette of jumbophage PhiKZ. Sci Rep 16, 5840 (2026). https://doi.org/10.1038/s41598-026-36188-9
Schlüsselwörter: Lyse von Bakteriophagen, phiKZ Jumbo-Phage, Holin-Endolysin-System, Pseudomonas aeruginosa-Phage, Lysis-Inhibition