Clear Sky Science · de
FcIgG-GE11-Melittin als neuartiges EGFR-gerichtetes Peptibody mit starker zytotoxischer Aktivität gegen Krebszellen
Bienenvenom trifft auf präzise Krebstherapie
Viele vielversprechende Krebsmedikamente sind für den restlichen Körper einfach zu schädlich, um sicher eingesetzt zu werden. Ein auffälliges Beispiel ist Melittin, das Hauptgift im Bienengift: Es kann Krebszellen zerstören, jedoch auch rote Blutkörperchen und gesundes Gewebe schädigen. Diese Studie untersucht einen cleveren Umweg – den Bau einer „Lenkwaffe“, die Melittin direkt zu Tumorzellen bringt, die einen bestimmten Oberflächenmarker tragen, und dabei normale Zellen weitgehend verschont.
Warum ein häufiger Krebs-Schalter ein Ziel ist
Ein Schlüsselfaktor in vielen Tumoren ist ein Molekül namens epidermaler Wachstumsfaktor-Rezeptor, kurz EGFR. Dieser Rezeptor sitzt auf der Zelloberfläche und hilft, Wachstum und Überleben zu steuern. In mehreren Krebsarten – darunter Lunge, Dickdarm, Prostata sowie einige Kopf-Hals- und Nierenkrebsarten – wird EGFR übermäßig produziert und treibt unkontrollierte Zellteilung voran. Deshalb sind Wirkstoffe, die an EGFR andocken, zu einer wichtigen Klasse zielgerichteter Therapien geworden. Bestehende EGFR-Medikamente blockieren jedoch meist Signale; sie durchlöchern Krebszellen nicht aktiv. Die Forscher fragten, ob sie Melittins starke zellauflösende Fähigkeit nutzen und selektiv an EGFR-reiche Tumorzellen liefern könnten.
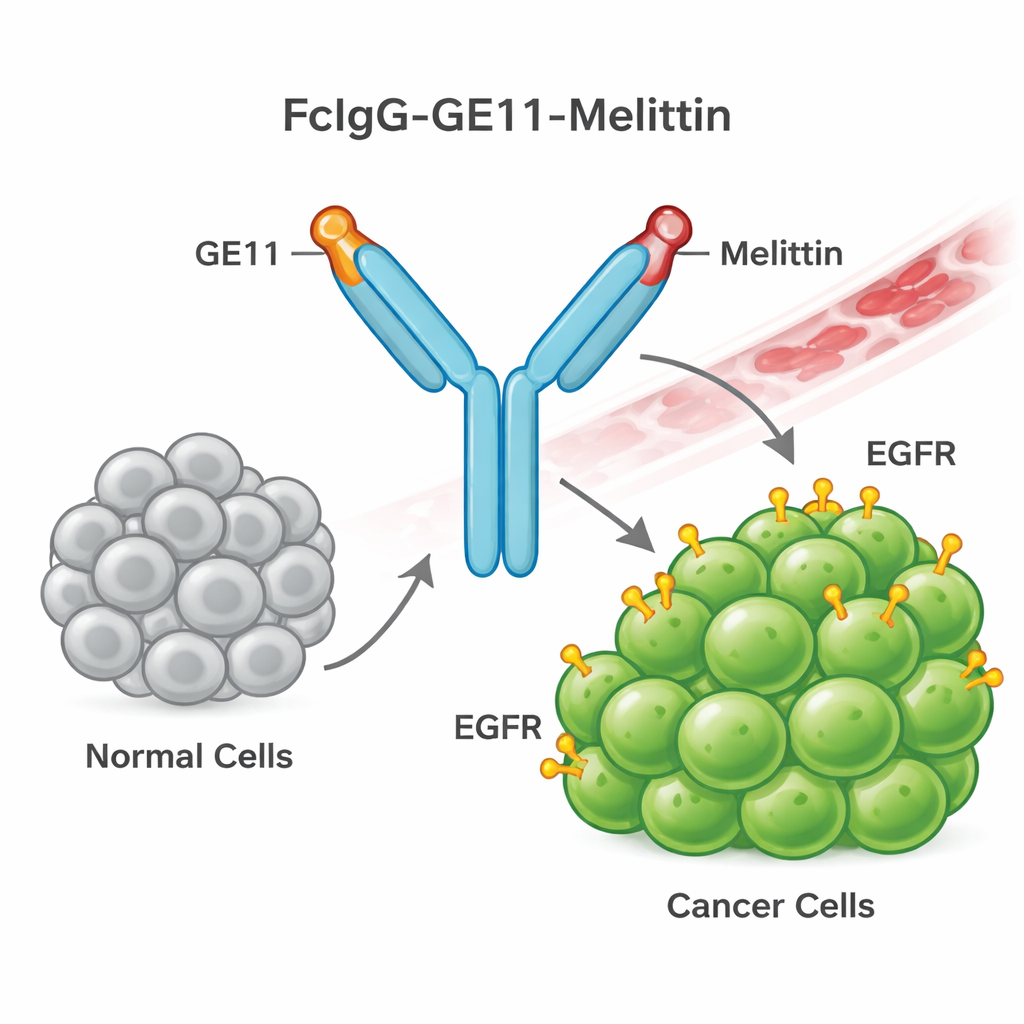
Bau einer gelenkten Bienen-Gift-Waffe
Dazu entwarf das Team ein neues Fusionsprotein, das sie FcIgG-GE11-Melittin nennen. Es kombiniert drei Teile: einen Antikörper‑„Schwanz“ (den Fc‑Bereich des humanen IgG), der die Stabilität im Blutkreislauf verbessert und die Reinigung erleichtert; ein kurzes Leitpeptid namens GE11, das EGFR auf Krebszellen erkennt und bindet; und Melittin, das Bienengiftpeptid, das Zellmembranen aufreißen kann. Bakterien wurden so verändert, dass sie dieses Fusionsprotein in großen Mengen produzieren. Das Protein wurde anschließend aufgefaltet und gereinigt, und Labortests bestätigten, dass es die erwartete dimerische Form annahm und das humane Antikörper‑Tag trug, was zeigt, dass die Konstruktion korrekt gebaut worden war.
Anhaften an Tumorzellen, nicht an irgendwelche Zellen
Die nächste Frage war, ob dieses Designer‑Molekül tatsächlich EGFR-reiche Krebszellen findet und daran haftet. Mit Durchflusszytometrie testeten die Autoren die Bindung an A549‑Lungenkrebszellen, die dafür bekannt sind, EGFR zu überexprimieren. Zellen, die mit FcIgG-GE11-Melittin behandelt wurden, zeigten einen starken Anstieg der Fluoreszenz, was darauf hindeutet, dass viele Fusionsmoleküle an ihrer Oberfläche angeheftet hatten. Ein nicht verwandter Peptibody, Romiplostim, zeigte nahezu keine Bindung und diente als Negativkontrolle. Das Bindungsprofil des neuen Konstrukts stimmte eng mit dem von Cetuximab überein, einem bekannten EGFR‑Antikörper, und unterstützt die Idee, dass die GE11‑Komponente das Fusionsprotein korrekt zu seinem Ziel leitet.
Krebszellen töten und Blutkörperchen schonen
Das Team prüfte dann, wie gut das Fusionsprotein verschiedene Krebszelllinien in Kultur abtöten konnte. Freies Melittin allein war extrem wirksam, aber unspezifisch und reduzierte das Zellüberleben bereits bei niedrigen Dosen stark in Lungen‑ (A549), Prostata‑ (DU145) und Dickdarm‑ (SW480) Krebszellen. Im Gegensatz dazu zeigte FcIgG-GE11-Melittin eine dosisabhängige Tötung, die in EGFR-positiven Zellen am stärksten war, während eine EGFR‑arme Brustkrebszelle (MDA-MB-453) relativ resistent war. Dieses Muster legt nahe, dass der Angriff des Fusionskonstrukts vom EGFR‑Targeting und nicht von zufälliger Membranschädigung abhängt. Am wichtigsten ist, dass freies Melittin in Experimenten mit menschlichen roten Blutkörperchen bereits bei moderaten Dosen nahezu vollständige Hämolyse verursachte, während das Fusionsprotein selbst bei sehr hohen Konzentrationen weniger als 5 % Hämolyse zeigte. Anders gesagt: Die Anbindung von Melittin an den EGFR‑suchenden Träger reduzierte seine Neigung, rote Blutkörperchen zu zerstören, dramatisch.
Was das für die zukünftige Krebsbehandlung bedeuten könnte
Insgesamt zeigt die Arbeit, dass die Kopplung eines potenten membranstörenden Toxins wie Melittin an ein präzises Zielsystem es von einer breit toxischen Substanz zu einer eher tumorselektiven Waffe machen kann. FcIgG-GE11-Melittin bindet stark an EGFR‑überexprimierende Krebszellen, tötet sie kontrolliert und dosisabhängig und verursacht im Labor nur minimale Schäden an roten Blutkörperchen. Obwohl vor einem Einsatz beim Menschen weitere Tierversuche und Sicherheitstests nötig sind, veranschaulicht dieser Ansatz, wie die Umgestaltung natürlicher Toxine in gelenkte Therapien neue Wege eröffnen könnte, EGFR‑positive Tumoren effektiver und mit weniger Nebenwirkungen zu behandeln.
Zitation: Hallaji, M., Fayaz, S., Allahyari, M. et al. FcIgG-GE11-Melittin as a novel EGFR targeted peptibody with potent cytotoxic activity against cancer cells. Sci Rep 16, 7047 (2026). https://doi.org/10.1038/s41598-026-36167-0
Schlüsselwörter: zielgerichtete Krebstherapie, EGFR, Bienenvergiftungs-Melittin, Peptibody, tumorselektive Toxine