Clear Sky Science · de
ONCOPLEX: ein von der Onkologie inspiriertes Hypergraph-Modell, das vielfältiges biologisches Wissen für die Vorhersage von Krebs-Treibergenen integriert
Warum diese Forschung wichtig ist
Krebs wird von einer kleinen Anzahl mächtiger genetischer Veränderungen angetrieben, die sich unter Tausenden harmloser Varianten verbergen. Diese wirklich gefährlichen „Treiber“-Gene zu finden, ist entscheidend für bessere Diagnosen und gezielte Therapien, doch es ist wie das Auffinden weniger Drahtzieher in einer riesigen, lauten Menschenmenge. Diese Studie stellt ONCOPLEX vor, ein neues künstlich-intelligentes Rahmenwerk, das Gene nicht einzeln betrachtet, sondern im Kontext der biologischen Signalwege, in denen sie zusammenwirken, und so eine schärfere Möglichkeit bietet, die Gene zu identifizieren, die Tumoren tatsächlich antreiben.
Krebs-Gene in ihrem biologischen Umfeld sehen
Die meisten aktuellen Methoden durchforsten Krebs-Genome nach Mutationen, die ungewöhnlich häufig auftreten oder in einfachen Gen-Netzwerken herausstechen. Diese Ansätze helfen, doch Biologie ist selten so einfach. Gene wirken meist in Gruppen innerhalb von Signalwegen, die Zellwachstum, DNA-Reparatur und viele andere Prozesse steuern. ONCOPLEX nimmt diese Komplexität an, indem es Gene als Punkte und Signalwege als größere überlappende Gruppen darstellt, die gleichzeitig viele Gene enthalten können. Diese Struktur, bekannt als Hypergraph, erlaubt dem Modell, mehrgliedrige Beziehungen direkt zu berücksichtigen, anstatt sie in viele separate Paare zu zerlegen.
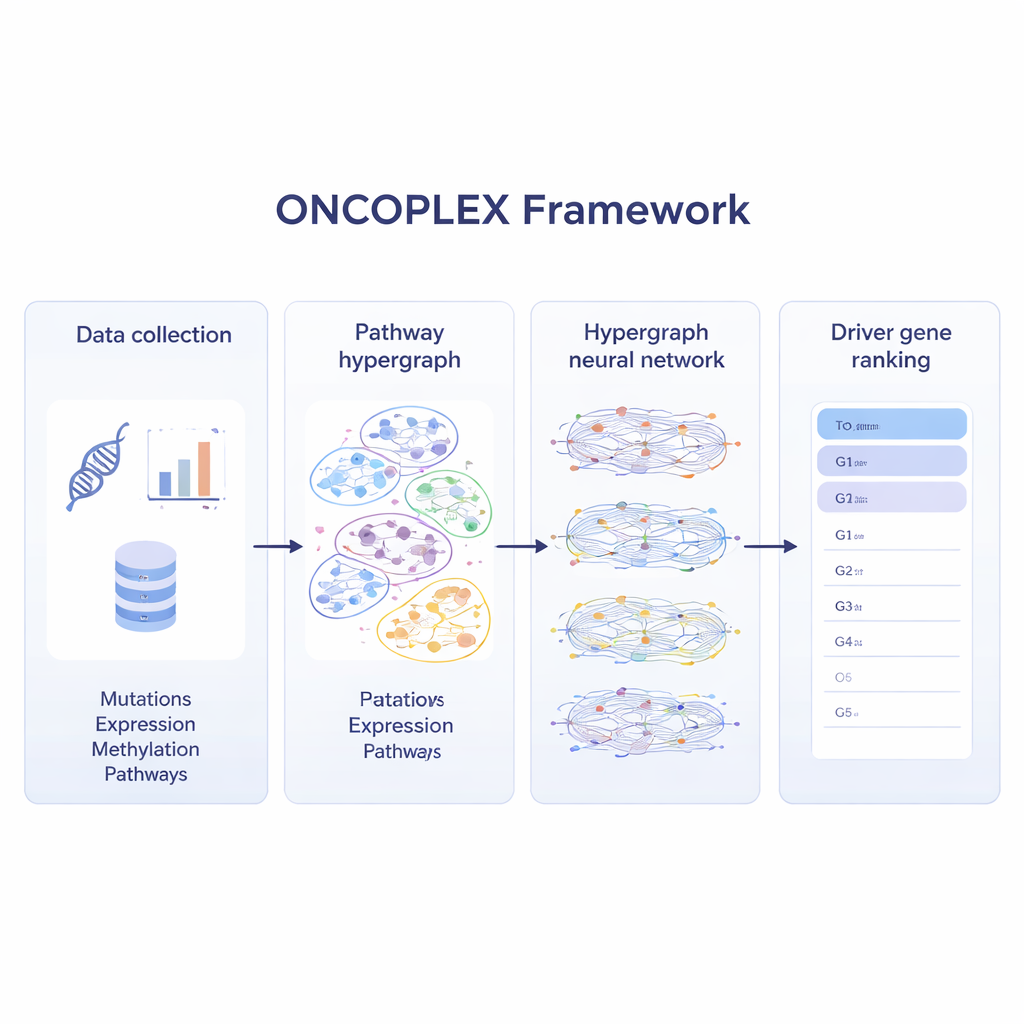
Viele Schichten von Krebsdaten verschmelzen
Um moderne Krebsdatensätze optimal zu nutzen, kombiniert ONCOPLEX mehrere Informationsarten zu jedem Gen. Es verwendet Mutationshäufigkeiten, Veränderungen in der Genaktivität, chemische Markierungen auf der DNA (Methylierung) sowie eine umfangreiche Menge biologischer Merkmale wie evolutionäre Konservierung und funktionelle Annotationen. Diese Merkmale werden jedem Gen im Hypergraph zugeordnet. Ein spezialisiertes neuronales Netzwerk leitet dann Informationen durch die Signalwege, sodass die Repräsentation jedes Gens sowohl von seinen eigenen Daten als auch vom Verhalten der Gene, mit denen es zusammenarbeitet, geprägt wird. Das Modell wird mit Genen trainiert, die bereits als Krebs-Treiber bekannt sind, lernt aber gleichzeitig auch aus vielen unbeschrifteten Genen, die wichtig sein könnten, aber noch nicht anerkannt sind.
Bestehende Werkzeuge in vielen Krebsarten übertreffen
Die Forschenden testeten ONCOPLEX mit Daten aus The Cancer Genome Atlas, sowohl durch Zusammenfassen vieler Tumortypen als auch durch Untersuchung von 11 einzelnen Krebsarten, darunter Brust-, Lungen-, Leber-, Blasen- sowie Kopf- und Halskrebs. Sie verglichen es mit mehreren führenden graph- und hypergraph-basierten Methoden. In allen Fällen war ONCOPLEX besser darin, bekannte Treiber-Gene von den weitaus häufigeren Nicht-Treibern zu unterscheiden, und rangierte wahrscheinliche Treiber weiter oben in seinen Listen. Sein Vorteil zeigte sich besonders deutlich bei den höchstrangigen Genen, wo eine genaue Identifikation für Folgeexperimente und klinische Übersetzung am wertvollsten ist.
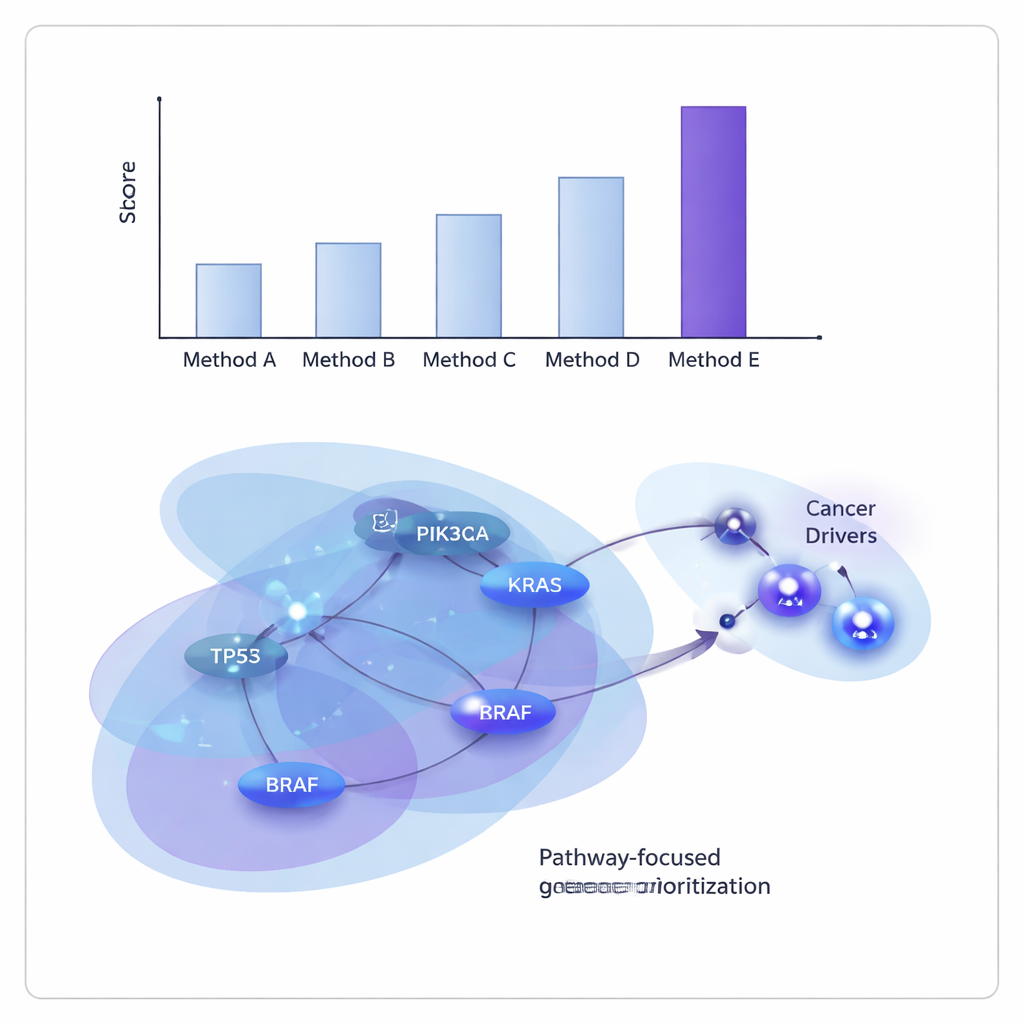
Geteilte und krebsartspezifische Täter aufdecken
Über rohe Leistungszahlen hinaus lieferten die von ONCOPLEX erstellten Ranglisten vielerlei bekannte Krebs-Gene wie KRAS, BRAF und Mitglieder des PI3K–AKT-Signalwegs, was bestätigt, dass das Modell etablierte biologische Zusammenhänge erfasst. Es hob außerdem vielversprechende Kandidaten hervor, die in bestimmten Krebsarten noch nicht fest als Treiber anerkannt sind, darunter Gene wie GRB2 und MAPK3 bei Brustkrebs sowie SHC1 bei Magenkrebs. Als das Team die am höchsten gerankten Gene mittels Weganreicherungsanalyse untersuchte, fanden sie starke Signaturen bekannter Krebswege, darunter ErbB-Signalgebung und PI3K–AKT–mTOR sowie immunbezogene Wege, was darauf hindeutet, dass ONCOPLEX Netzwerke identifiziert, die klinisch relevant sind.
Stärken, Grenzen und nächste Schritte
Indem gezeigt wird, dass reichhaltigere biologische Merkmale seine Vorhersagen stetig verbessern, demonstriert ONCOPLEX den Wert der Verschmelzung vieler Datenquellen in einem wegzentrierten Rahmenwerk. Gleichzeitig deckt die Studie eine Einschränkung auf: Da viele Krebsarten eine große Anzahl gemeinsamer Signalwege teilen, neigt das Modell manchmal dazu, stark wirkende „Pan-Cancer“-Gene gegenüber solchen zu bevorzugen, die wirklich spezifisch für eine Tumorart sind. Die Autoren schlagen vor, dass künftige Arbeiten verfeinern sollten, wie Weginformation genutzt wird, damit gemeinsame und krebsartspezifische Signale klarer voneinander getrennt werden können.
Was das für Patientinnen, Patienten und Kliniker bedeutet
Für Nicht-Spezialisten ist die Kernaussage, dass ONCOPLEX eine biologisch realistischere Methode bietet, um nach Genen zu suchen, die Krebs antreiben. Indem Gene in der Gesellschaft betrachtet werden, in der sie sich befinden — innerhalb von Signalwegen statt isoliert — verbessert es unsere Fähigkeit, sowohl bekannte als auch zuvor übersehene Treiber zu erkennen, selbst in Krebsarten, über die bislang wenig bekannt ist. Solche Werkzeuge können Forschenden helfen zu priorisieren, welche Gene im Labor untersucht werden sollten, die Suche nach neuen Wirkstoffzielen leiten und letztlich präzisere, wegbewusste Behandlungsstrategien in der Onkologie unterstützen.
Zitation: Alotaibi, E.M., Alkhnbashi, O.S. & Tran, V.D. ONCOPLEX: an oncology-inspired hypergraph model integrating diverse biological knowledge for cancer driver gene prediction. Sci Rep 16, 5164 (2026). https://doi.org/10.1038/s41598-026-36127-8
Schlüsselwörter: Krebs-Treibergene, Hypergraph-neuronale Netzwerke, Multi-Omics-Integration, Weg-Analyse, präzisionsonkologie