Clear Sky Science · de
Die Einzelzell-transkriptionelle Landschaft der pädiatrischen Zystischen Fibrose-Lunge aus minimalinvasiven Atemwegsproben
Warum das für Kinder mit zystischer Fibrose wichtig ist
Zystische Fibrose ist vor allem für zähen Schleim und Lungeninfektionen bekannt, doch unter diesen Symptomen tobt ein komplexer Kampf zwischen Immunzellen und der empfindlichen Auskleidung der Atemwege. Diese Studie blickt bei Kindern Zelle für Zelle auf diesen Kampf, anhand winziger Proben, die während routinemäßiger Lungenkontrollen gewonnen wurden. Indem die Forschenden kartieren, welche Zellen vorhanden sind und wie aktiv sie sind, zeigen sie, dass schädliche Entzündungsmuster früh im Leben beginnen und sich möglicherweise nur schwer rückgängig machen lassen – selbst mit modernen Medikamenten, die den zugrundeliegenden Gendefekt korrigieren.
Einzelzellblick in junge Lungen
Um zu erforschen, was in den Lungen von Kindern vor sich geht, nutzte das Team minimalinvasive Instrumente während flexibler Bronchoskopien – Eingriffe, die diese Patienten aus medizinischen Gründen ohnehin erhielten. Sie bestrichen sanft die innere Oberfläche der Luftröhre und Bronchien und sammelten Spülflüssigkeit aus tiefer gelegenen Abschnitten der Lunge. Die Proben stammten von zwei Kindern mit zystischer Fibrose (einem Säugling und einem Teenager) und drei altersentsprechenden Kindern ohne Erkrankung. Mit Einzelzell-RNA-Sequenzierung, einer Technik, die abliest, welche Gene in Tausenden einzelner Zellen aktiviert sind, erzeugten sie eine hochauflösende Karte der Immunzellen und der Zellen, die die Atemwege auskleiden, in den Lungen jedes Kindes. 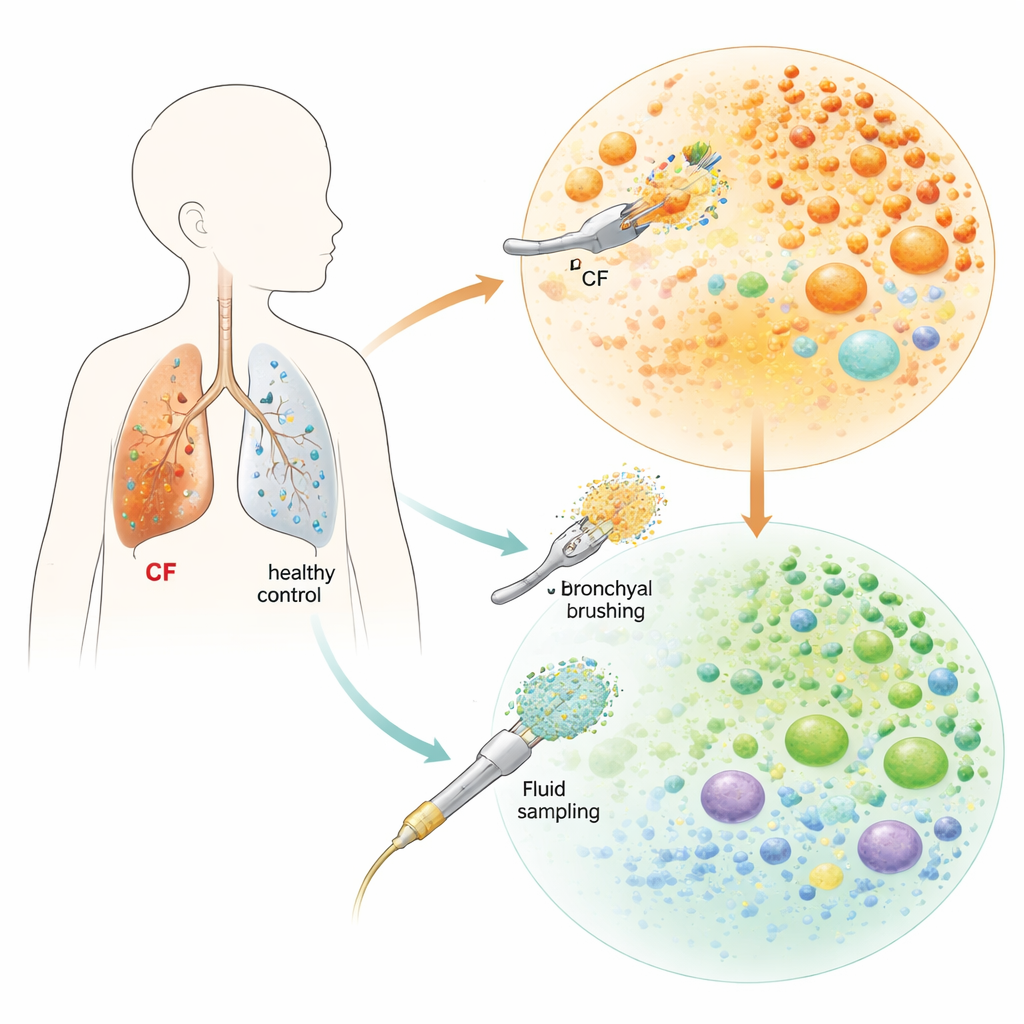
Ein dichtes Feld an Ersthelfer-Immunzellen
In den Spülproben von Kindern ohne zystische Fibrose dominierten Makrophagen – Aufräumzellen, die die Luftwege durchstreifen und zur Ruhe beitragen. Bei den Kindern mit zystischer Fibrose zeigte sich hingegen eine dramatische Verschiebung zugunsten von Neutrophilen, schnell reagierenden „Ersthelfer“-weißen Blutkörperchen, die Gewebe schädigen können, wenn sie verweilen. Neutrophile waren nicht nur häufiger, sie traten auch in mehreren unterschiedlichen Ausprägungen auf. Dazu gehörten unreife Formen, hochaktivierte entzündliche Zellen und eine auffällige Untergruppe, die durch Stress-Response-Proteine, sogenannte Hitzeschockproteine, gekennzeichnet war. Solche Stressreaktionen mögen zunächst schützend sein, sie können Neutrophile jedoch in einen langlebigen, aggressiven Zustand bringen, der die Entzündung am Lodern hält und den Luftwegsschaden vorantreiben kann, wie er bei der zystischen Fibrose beobachtet wird.
Entzündete Verteidiger und fehlende Verstärkung
Auch die in den Lungen mit zystischer Fibrose verbliebenen Makrophagen sahen anders aus. Statt der in der Vergleichsgruppe üblichen Mischung von „Hausmeister“-Typen waren in den Proben der zystischen Fibrose Makrophagen angereichert, die starke Immunsignale produzieren, was auf eine Verschiebung hin zu einer stärker entzündlichen Rolle hindeutet. Gleichzeitig fanden sich relativ wenige T‑Zellen – ein weiterer zentraler Arm des Immunsystems – in der Atemwegsflüssigkeit der Kinder mit zystischer Fibrose. Frühere Arbeiten haben gezeigt, dass Neutrophile T‑Zellen durch Nährstoffentzug funktionsunfähig machen können, wodurch diese effektiv aus den Atemwegen verdrängt werden. Diese Kombination aus aggressiven Neutrophilen, aktivierten Makrophagen und spärlichen T‑Zellen könnte erklären, warum Lungen bei zystischer Fibrose über Jahre entzündet bleiben und anfällig für Infektionen sind.
Ein Atemwegs-Epithel, das sich in den Kampf einmischt
Die Bürstenproben erlaubten den Forschenden, die Zellen zu untersuchen, die die Atemwege auskleiden: Basalzellen (die die Auskleidung erneuern können), Flimmerzellen (mit haarähnlichen Projektionen, die Schleim abtransportieren) und sekretorische Zellen (die Schleim und Schutzmoleküle produzieren). Die Gesamtzusammensetzung dieser Zelltypen war zwischen zystischer Fibrose und Vergleichskindern ähnlich, aber ihr Verhalten war es nicht. Bei zystischer Fibrose schalteten sekretorische Zellen Gene an, die mit Immunabwehr und antimikrobieller Aktivität verknüpft sind, was darauf hindeutet, dass sie als Teil der entzündlichen Reaktion Überstunden leisten. Flimmerzellen aktivierten ebenfalls Gene, die mit Entzündung und Resistenz gegen eine Form des Zelltods zusammenhängen, die mit Eisen und oxidativem Stress verknüpft ist. Zusammengenommen deuten diese Muster auf eine Atemwegoberfläche hin, die nicht nur Zuschauerin, sondern ein aktiver, entzündeter Mitspieler im Krankheitsgeschehen ist. 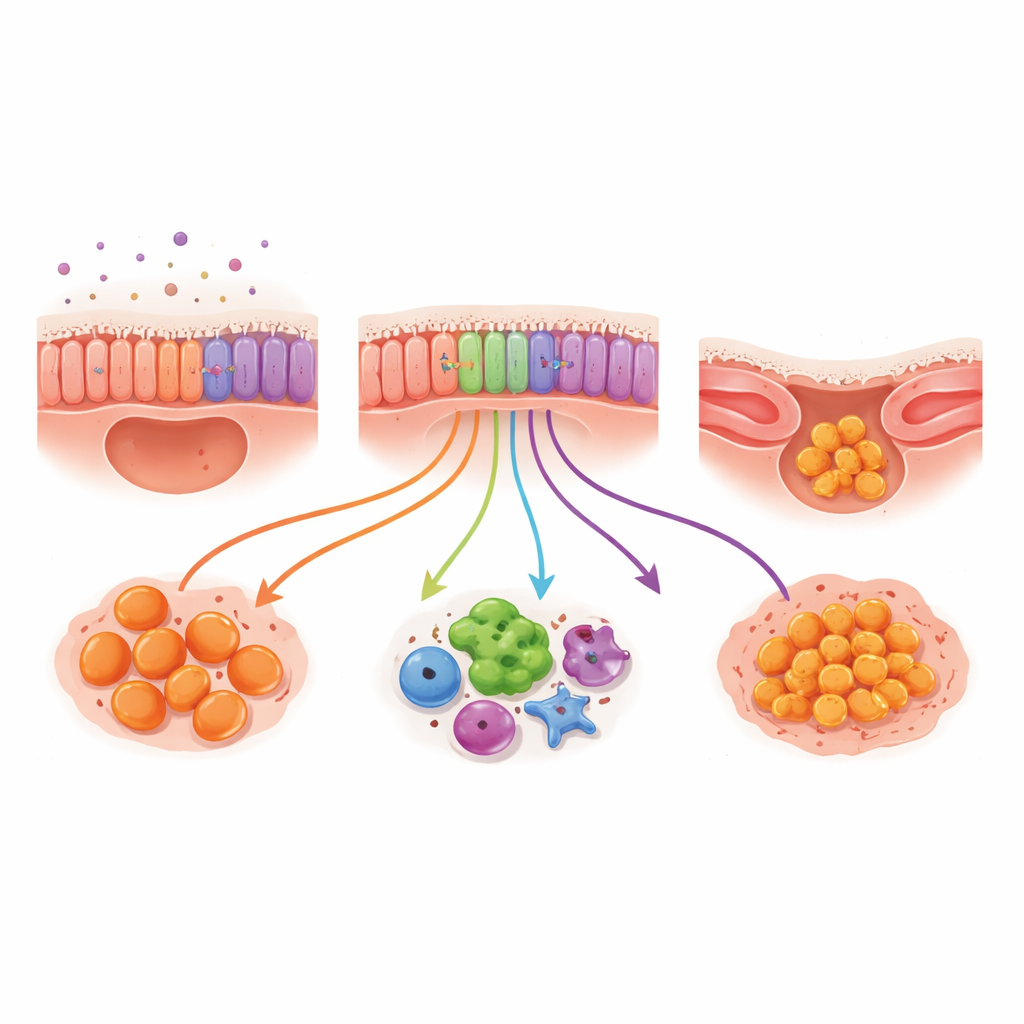
Zell‑zu‑Zell‑Dialoge, die Lungenschaden antreiben
Um zu verstehen, wie Epithelzellen und Neutrophile einander beeinflussen, analysierte das Team „Gespräche“ zwischen ihnen – Signale, die von einem Zelltyp gesendet und von einem anderen empfangen werden. Sie fanden heraus, dass Epithelzellen häufig als Sender agieren und mehrere molekulare Systeme nutzen, um Neutrophile zu erreichen. Einige dieser Signale dürften dazu beitragen, die Entzündung zu dämpfen, andere ermutigen Neutrophile, zusammenzuströmen, sich zu aktivieren und Material aufzunehmen. Dieses Hin und Her deutet darauf hin, dass das Epithel versucht, Schadenskontrolle und Abwehr in Balance zu halten, doch bei zystischer Fibrose scheinen die pro‑entzündlichen Signale zu überwiegen und die Lunge in einem chronischen Zustand schwelender Schädigung zu halten.
Warum frühe Veränderungen schwer umkehrbar sind
Ein zentrales Ergebnis ist, dass diese entzündlichen Muster sowohl beim Säugling als auch beim Teenager vorhanden waren, der ein fortgeschrittenes zystische-Fibrose‑Medikament eingenommen hatte, das das fehlerhafte Protein verbessert. Trotz dieser zielgerichteten Therapie ähnelten die Lungenzellen des Teenagers weiterhin eher denen des unbehandelten Säuglings als denen der Vergleichskinder. Das legt nahe, dass, sobald strukturelle Schäden und verankerte Entzündungen entstanden sind, die bloße Wiederherstellung der Proteinfunktion möglicherweise nicht ausreicht, um die Immun- und Epithellandschaft zurückzusetzen. Die Studie zeigt außerdem, dass schonende Probenahme der Atemwege kombiniert mit Einzelzell- und räumlicher Genanalyse diese Veränderungen im Zeitverlauf verfolgen kann. Dieser Ansatz könnte helfen, neue anti‑entzündliche und antimikrobielle Behandlungen zu entwickeln und zu testen, die darauf abzielen, die Lungenstruktur von Anfang an zu erhalten.
Zitation: Sun, Y., Vicencio, A.G., Beasley, M.B. et al. The single-cell transcriptional landscape of the pediatric cystic fibrosis lung from minimally invasive respiratory specimens. Sci Rep 16, 8113 (2026). https://doi.org/10.1038/s41598-026-36125-w
Schlüsselwörter: zystische Fibrose Lunge, neutrophile Entzündung, Einzelzell-RNA-Sequenzierung, Atemwegsepithel, pädiatrische Bronchoskopie