Clear Sky Science · de
Umfassende Bewertung der genotoxischen Wirkung durch Goldnanostäbe mithilfe multimodeller biologischer Systeme
Warum winzige Goldstäbchen für unsere DNA wichtig sind
Gold erinnert vielleicht an Schmuck oder Finanzen, doch in der modernen Medizin wird es auch zu winzigen Stäbchen geformt, die tausendfach dünner sind als ein menschliches Haar. Diese „Goldnanostäbchen“ können Ärzten helfen, Tumoren klarer darzustellen, Krebszellen zu erhitzen und abzutöten sowie Wirkstoffe sehr gezielt zu liefern. Dieselben ungewöhnlichen Eigenschaften, die diese Partikel so wirksam machen, werfen jedoch auch eine zentrale Frage auf: Schädigen sie das genetische Material in unseren Zellen? Diese Studie betrachtet breit gefächert Bakterien, Hefe und menschliche Leberkrebszellen, um zu klären, wie Goldnanostäbchen mit DNA interagieren und welche Folgen das für medizinische Anwendungen und Sicherheitsvorschriften haben könnte. 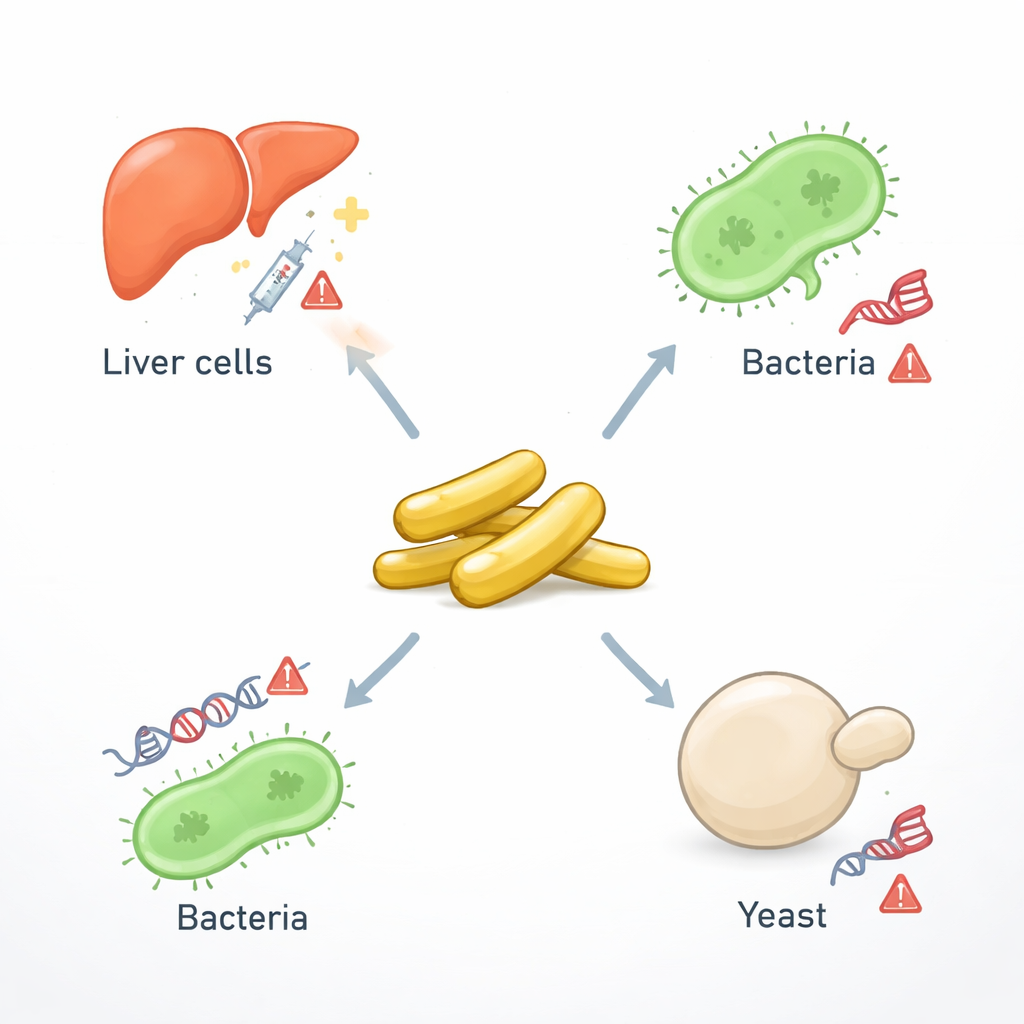
Von Reagenzgläsern zu lebenden Zellen
Um Risiken und Nutzen von Goldnanostäbchen zu untersuchen, stellten die Forschenden zuerst einheitliche, stabförmige Partikel von etwa 50 Nanometern Länge her — viel zu klein, um sie mit bloßem Auge zu sehen, aber klein genug, um in Zellen einzudringen. Anschließend testeten sie diese Partikel in mehreren biologischen Systemen, die zusammen eine Art „Toxizitätspipeline“ bilden. Zwei häufige Bakterien, Salmonella typhimurium und Escherichia coli, dienten als schnelle, einfache Sensoren für DNA-Schäden. Speziell konstruierte Hefestämme, von denen jeweils ein einzelnes Gen entfiel, das mit Stressantworten oder Zelltod verknüpft ist, lieferten ein modell, das menschlichen Systemen näherkommt, da Hefen viele grundlegende Signalwege mit uns teilen. Schließlich wurden menschliche Leberkrebszellen (HepG2), die häufig zur Prüfung von Arzneimitteln und Chemikalien verwendet werden, Goldnanostäbchen ausgesetzt, damit das Team Veränderungen bei zentralen krebsrelevanten Genen verfolgen konnte.
Wenn DNA in Schweifform zerreißt
In Bakterien und Hefe nutzten die Wissenschaftler eine empfindliche Methode, den sogenannten Kometen-Assay, um DNA-Schäden einzelner Zellen „sichtbar“ zu machen. Bei diesem Verfahren werden Zellen in ein Gel eingebettet, schonend aufgebrochen und einem elektrischen Feld ausgesetzt. Unversehrte DNA bleibt größtenteils an Ort und Stelle, während gebrochene Stränge herausströmen und eine Form bilden, die an einen Kometen mit hellem Kopf und hinterziehendem Schweif erinnert. Durch Messung von Länge und Intensität des Schweifs können Forschende das Ausmaß der genetischen Schädigung abschätzen. Sowohl in Salmonella als auch in E. coli führten Goldnanostäbchen zu deutlichen, dosisabhängigen Zunahmen in allen Kometenmaßen: mehr Zellen mit Schweifen, längere Schweife und ein höherer Prozentsatz der in den Schweif gezogenen DNA. Hefeknockout-Stämme zeigten dasselbe Muster, wobei einige Stämme — insbesondere solche ohne Gene für Stress- und Mitochondrienfunktionen — auffallend stärkere DNA-Fragmentierung als normale Hefen aufwiesen. 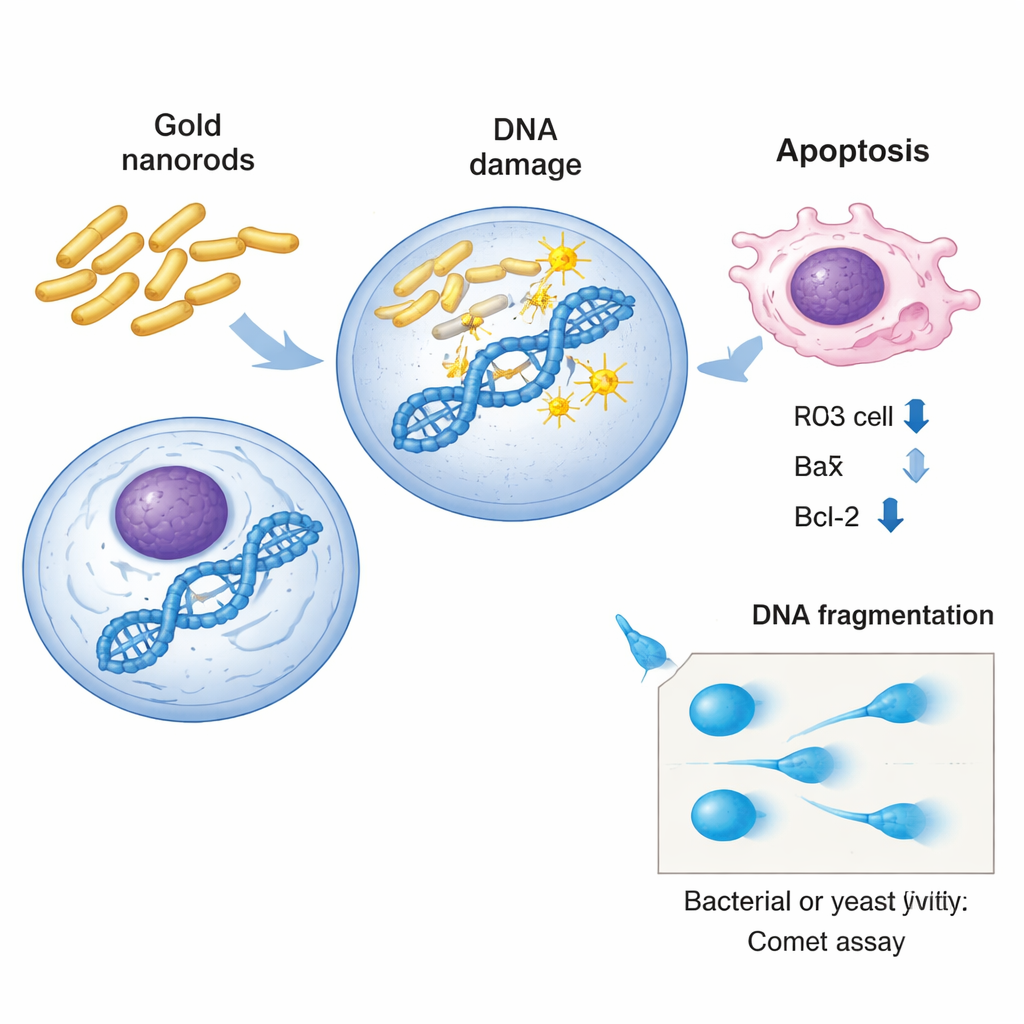
Gen-Netzwerke und Todesprogramme in menschlichen Zellen
In menschlichen Leberkrebszellen schauten die Forschenden tiefer als nur auf physische DNA-Brüche und untersuchten, wie die inneren Kontrollsysteme der Zellen reagierten. Mittels Echtzeit-PCR maßen sie die Aktivität von drei bekannten Wächter- und Ausführergenen für Zellschicksal: p53 und Bax, die den Zelltod fördern, wenn Schäden erkannt werden, sowie Bcl-2, das das Überleben der Zelle unterstützt. Nach Exposition gegenüber halbstarken toxischen Dosen von Goldnanostäbchen stiegen die Werte von p53 und Bax an, während Bcl-2 sank — ein molekulares Muster, das für programmierten Zelltod (Apoptose) spricht. Mit anderen Worten: Die Nanostäbchen verletzten nicht nur die DNA, sondern trieben die Krebszellen auch in die Selbstzerstörung. Um die Heferesultate mit menschlicher Biologie zu verbinden, nutzten die Forschenden die Plattform GeneMANIA, um Interaktionsnetzwerke rund um die in Hefe gelöschten Gene zu kartieren. Diese Analyse zeigte dichte Netze physikalischer und genetischer Wechselwirkungen, die mit Stressreaktionen, DNA-Reparatur und Mitochondrienfunktion verknüpft sind, und untermauerte die Idee, dass ähnliche Pathways sowohl in Hefe als auch in menschlichen Zellen verwundbar sind.
Das medizinische Versprechen gegen genetische Risiken abwägen
In der Summe zeichnen diese Experimente ein nuanciertes Bild von Goldnanostäbchen. Einerseits können sie eindeutig die DNA in sehr unterschiedlichen Organismen schädigen, und der Schaden nimmt mit der Dosis zu. Bestimmte genetische Hintergründe, wie Hefestämme ohne spezifische Stress- oder Mitochondriengene, sind besonders empfindlich, was andeutet, dass Menschen mit bestimmten genetischen Merkmalen ebenfalls unterschiedlich reagieren könnten. Andererseits kann in menschlichen Leberkrebszellen genau diese DNA-Schädigung und die daraus resultierende Aktivierung von Todeswegen das Ziel sein, das Ärzte beim Anvisieren von Tumoren erreichen wollen. Für Laien lautet die Kernbotschaft: Goldnanostäbchen sind mächtige Werkzeuge, die sowohl helfen als auch schaden können — sie können Krebszellen abtöten, aber auch genetische Risiken für andere Zellen und die Umwelt darstellen. Die Studie argumentiert, dass künftige medizinische Anwendungen dieser Partikel sorgfältig Dosis, gezielte Abgabe und Patientengenetik abwägen müssen, um ihre Vorteile zu nutzen und ihr genotoxisches Potenzial unter Kontrolle zu halten.
Zitation: Rashad, S.E., Haggran, A.A. & Abdoon, A.S.S. Comprehensive assessment of gold nanorod-induced genotoxicity using multi-model biological systems. Sci Rep 16, 5429 (2026). https://doi.org/10.1038/s41598-026-36119-8
Schlüsselwörter: Goldnanostäbe, DNA-Schädigung, Nanotoxikologie, Krebstherapie, Genotoxizitätstests