Clear Sky Science · de
Biochemische und epigenomische Zerlegung der TFIIE‑Funktion zeigt genselektive Anforderungen bei der menschlichen Transkription
Neubewertung eines „universellen“ Gen‑Schalters
Jede Zelle in Ihrem Körper ist auf ein fein abgestimmtes System angewiesen, das Gene an‑ und ausschaltet. Lehrbücher beschreiben dieses System oft als eine feste Werkzeugkiste aus „allgemeinen“ Faktoren, die alle Gene benötigen. Diese Studie setzt sich mit dieser Vorstellung für einen solchen Faktor, TFIIE, auseinander und zeigt, dass er kein Einheitsbaustein ist. Stattdessen scheint TFIIE besonders wichtig für bestimmte Gruppen von Genen zu sein, von denen viele an der Organisation unserer DNA und der Erhaltung der Genome‑Stabilität beteiligt sind. Zu verstehen, wann TFIIE erforderlich ist und wann es umgangen werden kann, liefert ein nuancierteres Bild davon, wie Zellen Genaktivität steuern und auf Stress oder Krankheit reagieren.
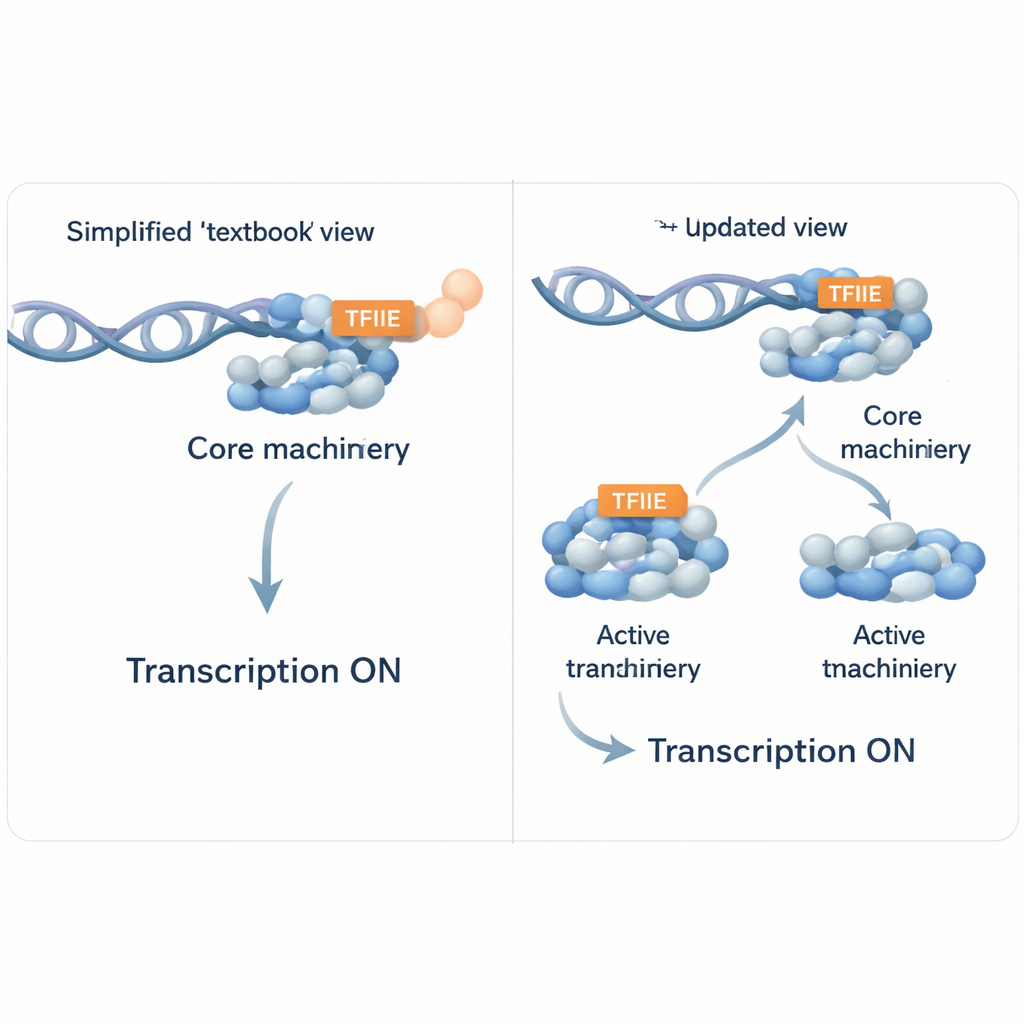
Wie Zellen normalerweise das Lesen von Genen starten
Um ein Gen einzuschalten, baut die Zelle eine große Proteinversammlung an der „Startlinie“ des Gens, dem Promotor, auf. Diese Assemblierung, bekannt als Präinitiationskomplex, umfasst die RNA‑Polymerase II (das Enzym, das DNA in RNA übersetzt) und mehrere Helferproteine, die traditionell als allgemeine Transkriptionsfaktoren bezeichnet werden. TFIIE ist einer dieser Helfer und galt lange Zeit als nahezu unverzichtbar an fast jedem aktiven Promotor. Es hilft bei der Rekrutierung eines weiteren Faktors, TFIIH, der die DNA öffnet und der Polymerase II das Starten des Kopiervorgangs ermöglicht. Unter vereinfachten Laborbedingungen mit nur gereinigten Komponenten wirkt TFIIE tatsächlich unentbehrlich: Wird es entfernt, findet kaum noch präzise Transkription statt.
Wenn die Lehrbuchregel bricht
Die Autoren fragten, was in einer realistischeren Umgebung geschieht, die dennoch genaue Kontrolle erlaubt. Sie verwendeten Nuklearextrakte aus menschlichen Zellen—komplexe Gemische, die Tausende von Proteinen enthalten—und entfernten selektiv einen großen Co‑Aktivator‑Komplex namens Mediator, der normalerweise hilft, entfernte regulatorische Elemente mit Promotoren zu verbinden. In diesen Mediator‑depletierten Extrakten fügten sie verschiedene gereinigte Versionen des Mediator‑Komplexes wieder hinzu und verfolgten, welche Proteine an ein Modellpromotorband gebunden wurden und ob RNA produziert wurde. Überraschenderweise konnte bei Wiederherstellung eines vollständigen Kern‑Mediator die RNA‑Polymerase II binden und Transkripte erzeugen, obwohl TFIIE am Promotor kaum nachweisbar war. Mit anderen Worten: In einer überfüllten nuklearen Umgebung mit vielen zusätzlichen Faktoren konnten einige Gene weiterhin ohne deutliche Rekrutierung von TFIIE transkribiert werden, was die Auffassung in Frage stellt, TFIIE sei immer erforderlich.
Fokussierung auf bestimmte Gen‑Nachbarschaften
Um zu sehen, wie sich diese biochemischen Befunde genomweit auswirken, untersuchten die Forscher öffentliche Datensätze, die abbilden, wo TFIIE und andere Schlüsselfaktoren in der DNA menschlicher Blutkrebszellen liegen. Mithilfe einer Technik namens ChIP‑seq konzentrierten sie sich auf Regionen um Transkriptionsstartstellen und fragten, welche Promotoren sowohl von TFIIE als auch von TBP (einer zentralen DNA‑bindenden „Landefläche“), einer Mediator‑Untereinheit (MED1) oder einer Komponente des ATAC‑Co‑Aktivator‑Komplexes (ZZZ3) besetzt sind. Sie fanden heraus, dass TFIIE nicht überall bindet, sondern an bestimmten Untergruppen von Promotoren. Einige Promotoren trugen TFIIE zusammen mit TBP und MED1, andere mit TBP und ZZZ3, und eine dritte Gruppe schien hauptsächlich für TFIIE selbst angereichert zu sein, mit wenig Anzeichen des kanonischen Mediator. Eine genaue Betrachtung der Rohsignale deutete darauf hin, dass „nur‑TFIIE“‑Promotoren oft eine schwache, aber reale TBP‑Präsenz aufweisen, was auf ein Kontinuum der Besetzung statt strikter Alles‑oder‑Nichts‑Kategorien hinweist.
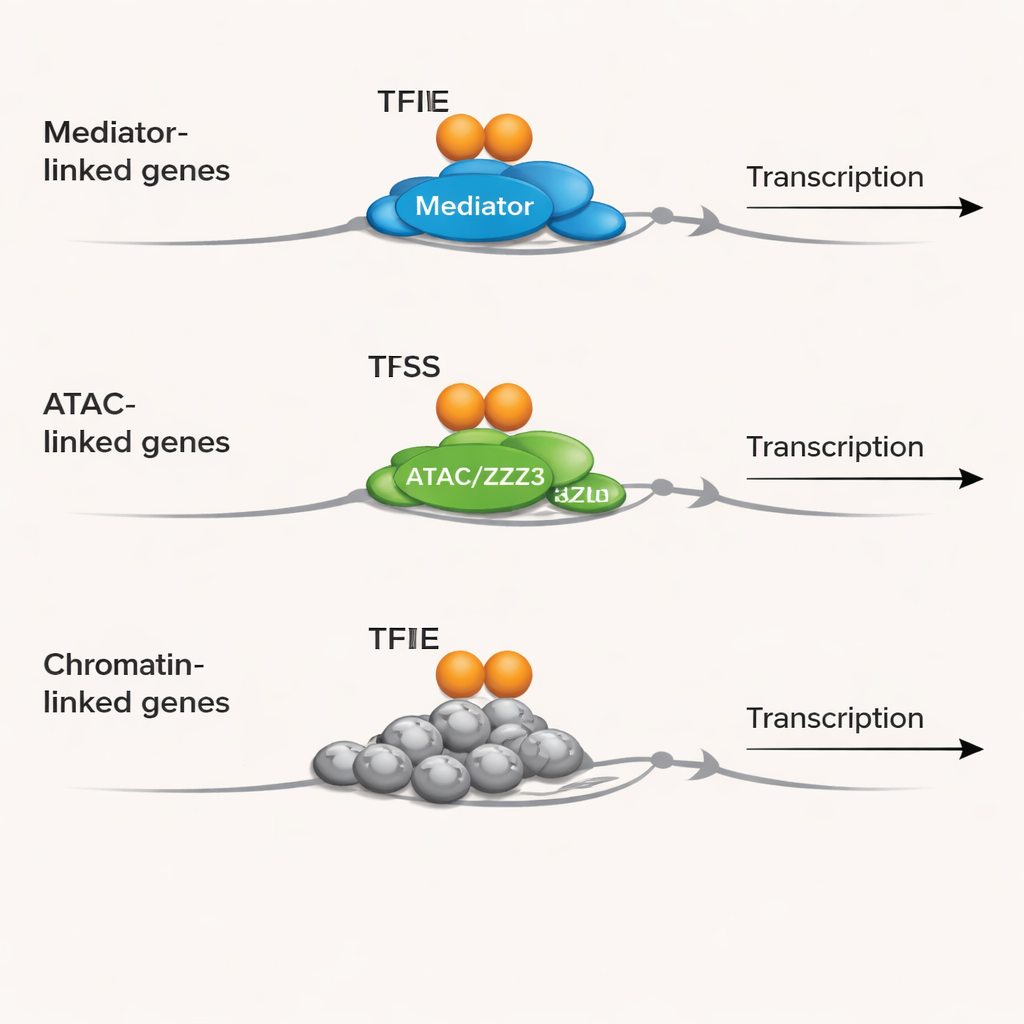
Unterschiedliche Partner, unterschiedliche Aufgaben
Durch die Verknüpfung dieser Promotor‑Gruppen mit bekannten Genfunktionen entdeckte das Team, dass TFIIE offenbar spezialisiert ist. Promotoren, bei denen TFIIE mit TBP und MED1 zusammenarbeitet, sind stark mit Genen assoziiert, die an RNA‑Spleißing, RNA‑Verarbeitung und der Kontrolle der Proteinproduktion beteiligt sind—Schritten, die die aus der DNA erzeugten Botschaften verfeinern und interpretieren. Promotoren, bei denen TFIIE mit TBP und ZZZ3 kooperiert, sind angereichert für Gene, die Ribosomen aufbauen, Protein‑RNA‑Komplexe zusammenbauen und DNA reparieren, und verbinden TFIIE mit grundlegendem Zellwachstum und Erhaltung des Genoms. Unterdessen sind Promotoren, die hauptsächlich von TFIIE markiert sind, reich an Genen, die das Chromatin formen—also wie DNA um Proteine gewickelt wird, um Nukleosomen zu bilden—und die epigenetische Regulation beeinflussen. Dieses Muster legt nahe, dass TFIIE dazu beiträgt zu koordinieren, wann und wie Chromatinstruktur und RNA‑Handhabung mit dem Start der Transkription gekoppelt werden.
Was das für unser Verständnis der Genkontrolle bedeutet
Insgesamt argumentiert die Studie, dass TFIIE kein starres, universelles Erfordernis ist, sondern ein flexibler Akteur, dessen Bedeutung vom lokalen Umfeld des Gens und dessen Ko‑Faktoren abhängt. In stark vereinfachten Systemen führt das Entfernen von TFIIE zum Stillstand der Transkription, doch in der reichen Umgebung des Zellkerns können andere Proteine teilweise kompensieren, sodass bestimmte Gene dennoch aktiviert werden. Gleichzeitig zeigen genomweite Karten, dass TFIIE dazu tendiert, sich an Promotoren zu konzentrieren, die RNA‑Verarbeitung, Ribosomenproduktion, DNA‑Reparatur und Chromatinorganisation steuern. Für eine allgemeine Leserschaft lautet die Quintessenz: Einer der vermeintlich „grundlegenden“ Teile der Genlesemaschine trägt tatsächlich dazu bei, spezialisierte Programme abzustimmen, die unsere DNA organisiert halten und den Informationsfluss der Zellen in Balance halten—Erkenntnisse, die möglicherweise künftig Einfluss darauf haben, wie wir über Krebs, Entwicklungsstörungen und andere Erkrankungen denken, in denen Genregulation aus dem Gleichgewicht gerät.
Zitation: Cevher, M.A., Wijerathne, P.N., Yozgat, Y. et al. Biochemical and epigenomic dissection of TFIIE function reveals gene-selective requirement in human transcription. Sci Rep 16, 5797 (2026). https://doi.org/10.1038/s41598-026-36090-4
Schlüsselwörter: Genregulation, Transkriptionsinitiation, TFIIE, Chromatinorganisation, Mediator‑Komplex