Clear Sky Science · de
R5- und R7-Positionen an Fluorchinolon-Gerüsten treiben die Disruption von F-Aktin-Filamenten
Antibiotika als Helfer fürs Gehirn
Viele verbreitete Hirnerkrankungen, von Alzheimer bis Parkinson, teilen einen versteckten Übeltäter: winzige, strukturgebende Stäbchen in Nervenzellen, die mit der Zeit verklemmen und starr werden. Diese Stäbchen bestehen aus dem Protein Aktin, das normalerweise flexibel Teil des inneren Zellgerüsts ist. Diese Studie untersucht eine überraschende Möglichkeit — dass eine bekannte Antibiotikaklasse, die Fluorchinolone, so umgestaltet werden könnte, dass sie diese schädlichen Aktinbündel vorsichtig auflösen und dadurch potenziell das Gehirn schützen.
Wenn das Zellgerüst versagt
Gesunde Nervenzellen formen und remodeln ständig ihr internes Skelett, um Verbindungen zu bilden und anzupassen. Aktinfilamente sind zentral für diesen Prozess: sie entstehen und lösen sich je nach Bedarf. Unter Stress jedoch kann Aktin in hartnäckige, stäbchenartige Aggregate erstarren, die die Zelle verstopfen, den Transport lebenswichtiger Fracht stören und die Anlagerung krankheitsassoziierter Proteine wie Amyloid und Tau begünstigen. Im Laufe von Jahren können diese Stäbchen zu dichten Strukturen heranreifen, den sogenannten Hirano-Körpern, die häufig in Gehirnen von Menschen mit verschiedenen neurodegenerativen Erkrankungen zu finden sind. Da vorhandene Aktin‑zielende Wirkstoffe oft hochtoxisch sind, suchen Forschende nach sichereren kleinen Molekülen, die diese Aggregate lockern können, ohne Zellen zu schädigen.
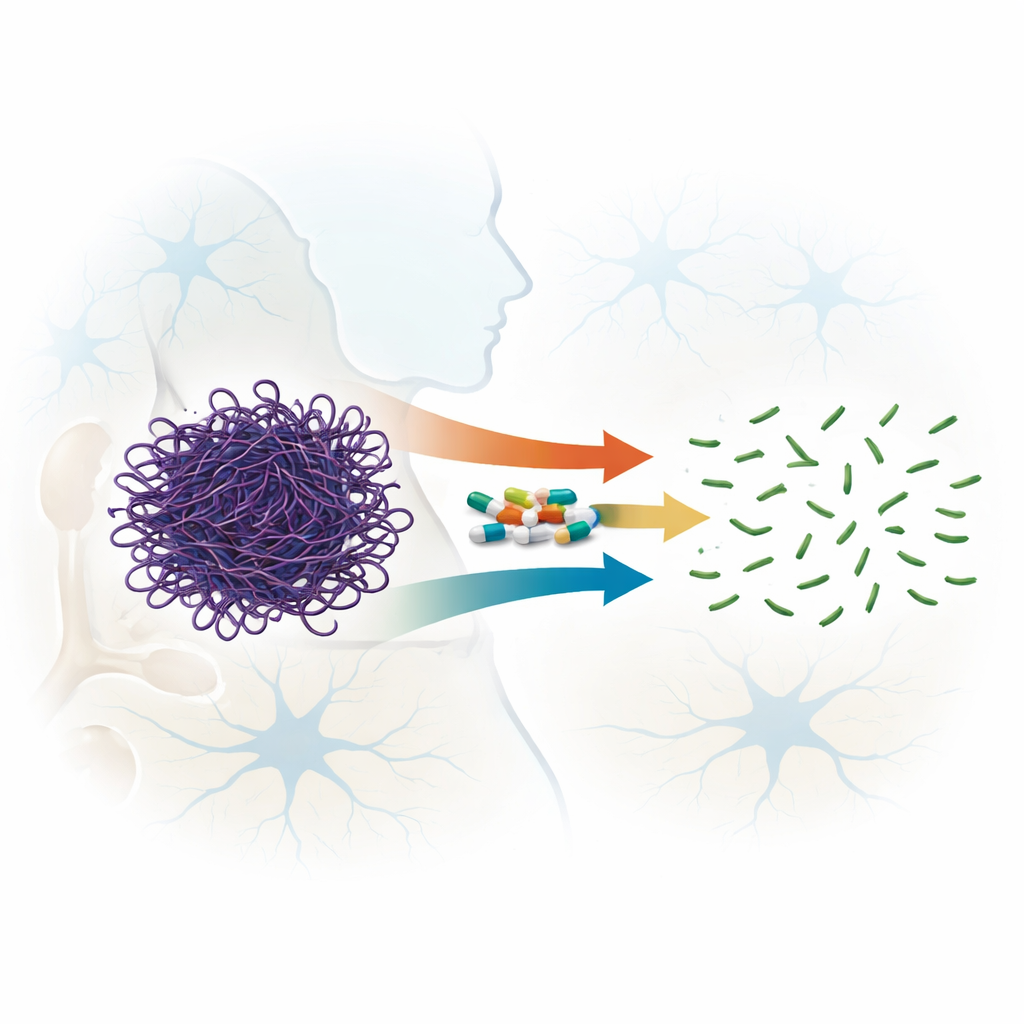
Eine unerwartete Fähigkeit bekannter Medikamente
Fluorchinolone sind Breitbandantibiotika, die weltweit zur Behandlung von Infektionen eingesetzt werden; einige neuere Vertreter dieser Familie können die Blut‑Hirn‑Schranke passieren. Frühere Hinweise legten nahe, dass bestimmte Fluorchinolone Aktinfilamente destabilisieren könnten. In dieser Arbeit verglichen die Autorinnen und Autoren systematisch sieben verwandte Verbindungen aus vier Generationen der Wirkstofffamilie, um zu prüfen, wie gut sie bereits gebildete Aktinfilamente aufspalten, anstatt nur deren Bildung zu verhindern. Mithilfe von Lichtstreumessungen, Elektronenmikroskopie und Gel‑Filtration zeigten sie, dass alle getesteten Wirkstoffe Aktinfilamente stören konnten, jedoch mit sehr unterschiedlicher Stärke. Zwei Substanzen — Sparfloxacin (dritte Generation) und Moxifloxacin (vierte Generation) — stachen hervor: sie zerteilten lange Filamente schnell und irreversibel in deutlich kleinere Stücke, selbst bei relativ niedrigen Wirkstoff‑zu‑Protein‑Verhältnissen.
Filamente beim Auseinanderfallen beobachten
Hochauflösende Aufnahmen und biophysikalische Tests zeigten, wie sich die Filamente unter Wirkstoffeinfluss verändern. Die Elektronenmikroskopie ergab, dass unbehandeltes Aktin lange, durchgehende Stränge bildet, während wirksame Fluorchinolone diese in kurze, verstreute Fragmente verwandeln. Weniger potente Vertreter erzeugten geknickte und gebogene Filamente, die jedoch nicht vollständig durchtrennt wurden. Wärmebasierte Messungen zur Proteinstabilität bestätigten diese physikalische Disruption: Nach Behandlung verhielt sich Aktin eher wie seine freie, unassemblierte Form mit niedrigeren Schmelztemperaturen, wobei seine grundlegende Bausteinstruktur jedoch nahezu unverändert blieb. Das deutet darauf hin, dass die Wirkstoffe Aktin nicht entfalten oder beschädigen — sie lösen hauptsächlich die Verbindungsstellen, mit denen die Einheiten in Filamenten zusammenhalten.
Ein Blick auf den molekularen Griff
Um zu verstehen, warum einige Fluorchinolone besser wirken als andere, kombinierten die Forschenden fortgeschrittene Kernspinresonanzexperimente mit Computersimulationen von Wirkstoff‑Protein‑Interaktionen. Sie fanden heraus, dass alle Verbindungen auf einem gemeinsamen ringförmigen „Kern“ basieren, der Kontakt zu Aktin herstellt, insbesondere an zwei Positionen dieses Kerns, die wiederholt das Filament berühren. Zusätzliche chemische Gruppen an spezifischen Stellen — bezeichnet R5 und R7 — beeinflussen jedoch stark, wie fest und wo jedes Molekül bindet. Bei den wirksamsten Disruptoren tragen diese Positionen eine Aminogruppe und sperrige Ringsysteme, die in eine kleine Tasche an der Schnittstelle benachbarter Aktinstränge reichen. Dort stören sie wichtige stabilisierende Kontakte, darunter eine bedeutende Salzbrücke, die normalerweise Filamente zusammenhält.
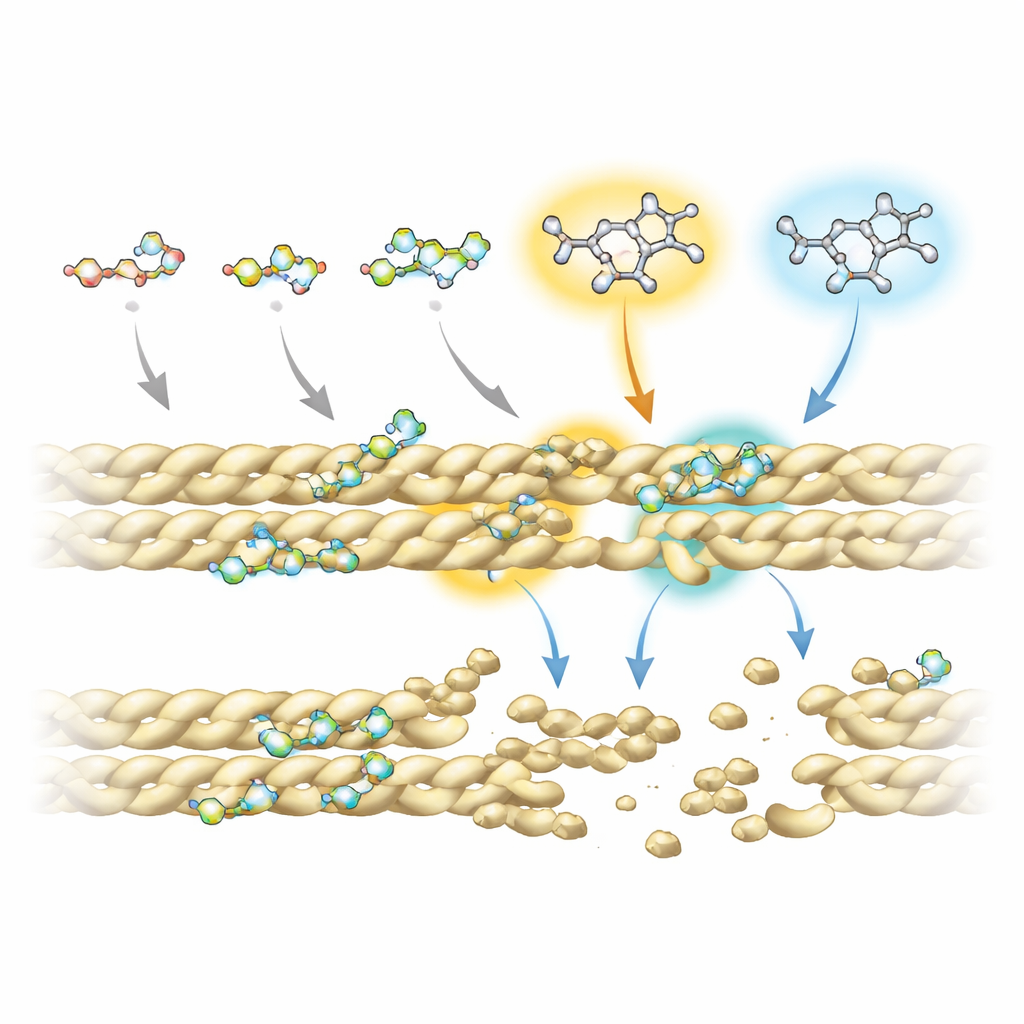
Von Hefezellen zu zukünftigen Therapien
Die Forschenden testeten die Wirkstoffe außerdem in einem Hefestamm, der natürlicherweise Aktinbündel akkumuliert und damit Aspekte erkrankter Zellen nachahmt. Unter dem Mikroskop zeigten unbehandelte Hefezellen große, helle Aktinklumpen, während Zellen, die Fluorchinolonen ausgesetzt waren — insbesondere Sparfloxacin, Moxifloxacin und in höheren Dosen Nalidixinsäure — deutlich diffusere, punktartige Muster aufwiesen, was anzeigt, dass die Bündel aufgelöst worden waren. Wichtig ist, dass die Wirkung der Wirkstoffe relativ schonend zu sein schien: Sie schwächten die Filamentverpackung, ohne die zugrunde liegende Form von Aktin grob zu verzerren, und ihre Bindung war schwächer als die klassischer Aktin‑Toxine, was das Risiko schwerer Nebenwirkungen potenziell verringern könnte.
Intelligentere Aktin‑zielende Wirkstoffe entwerfen
Insgesamt zeigt die Studie, dass kleine Änderungen an bekannten Antibiotika ihr Zusammenspiel mit dem inneren Zellgerüst dramatisch verändern können. Indem die Autorinnen und Autoren R5 und R7 als wichtige „Regelknöpfe“ für sowohl Aktin‑Disruption als auch Hirndurchgängigkeit identifizieren, skizzieren sie eine Blaupause zur Entwicklung neuer, von Fluorchinolonen inspirierter Moleküle, die gezielt schädliche Aktinaggregate demontieren. Obwohl diese Ergebnisse einen frühen, laborbasierten Wirkungsnachweis darstellen, eröffnen sie die Möglichkeit, dass künftig aus bekannten Antibiotika abgeleitete Wirkstoffe toxische Gerüste in Nervenzellen entfernen und so das Fortschreiten mancher Formen von Neurodegeneration verlangsamen oder verhindern könnten.
Zitation: Gupta, R.J., Nair, H., Sarhadi, T.R. et al. R5 and R7 positions on fluoroquinolone scaffolds drive F-actin filament disruption. Sci Rep 16, 9517 (2026). https://doi.org/10.1038/s41598-026-36089-x
Schlüsselwörter: Aktinaggregate, Fluorchinolon-Antibiotika, neurodegenerative Erkrankung, Arzneimittel-Repositionierung, Zytoskelett