Clear Sky Science · de
Die Rolle von zellulären Seneszenz‑assoziierten Genen bei Ischämie‑Reperfusions‑Schäden und die Identifizierung ihrer Biomarker
Warum sich Herzschäden verschlimmern können, wenn das Blut zurückkehrt
Wenn jemand einen Herzinfarkt erleidet oder sich einer Herzoperation unterzieht, kämpfen Ärztinnen und Ärzte darum, die Durchblutung des unterversorgten Herzmuskels wiederherzustellen. Paradoxerweise kann genau dieser lebensrettende Schritt zusätzlichen Schaden verursachen — ein Problem, das als Ischämie‑Reperfusions‑Schaden bekannt ist. Diese Studie untersucht, warum einige Herzmuskelzellen so schlecht auf die Wiederzufuhr von Blut reagieren, mit Schwerpunkt auf der Biologie zellulären Alterns, und identifiziert eine kleine Gruppe von Genen, die Ärzten helfen könnte, diesen verborgenen Schaden genauer zu erkennen und möglicherweise zu behandeln.
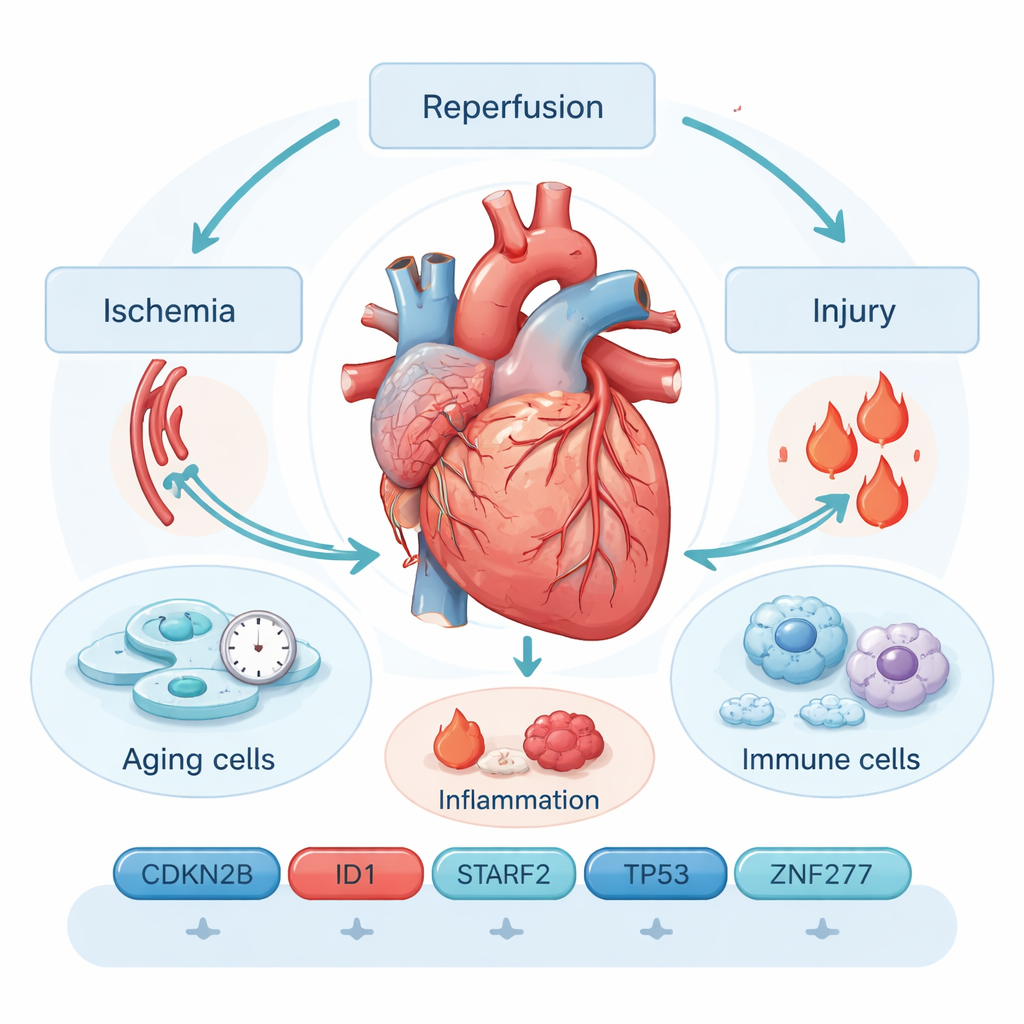
Wenn Rettung zu erneutem Schaden wird
Ischämie‑Reperfusions‑Schaden verläuft in zwei Akten. Zuerst ist eine Koronararterie blockiert und das Herzgewebe wird von Sauerstoff abgeschnitten (Ischämie). Wenn die Blockade beseitigt ist und das Blut zurückströmt (Reperfusion), kann ein Ausbruch reaktiver Moleküle und eine Entzündungsreaktion bereits angeschlagene Zellen weiter schädigen. Aktuelle Werkzeuge — wie EKG, bildgebende Verfahren und Bluttests auf Proteine wie Troponin — übersehen oft frühe oder subtile Schädigungen und können schlecht vorhersagen, wer langfristige Probleme entwickelt. Diese Lücke hat Forscher dazu veranlasst, tiefer zu schauen, auf die molekularen Ereignisse innerhalb der Herzmuskelzellen selbst.
Zelluläres Altern als verborgener Treiber
Die Autorinnen und Autoren konzentrieren sich auf die zelluläre Seneszenz, einen Zustand, in dem Zellen dauerhaft die Teilung einstellen und ein „Alarm‑sendenes“ Verhalten annehmen. Seneszente Herzmuskelzellen sezernieren ein Gemisch aus entzündlichen Molekülen und Enzymen, das als seneszenz‑assoziiertes sekretorisches Phänotyp bezeichnet wird. Diese chemische Wolke kann die Narbenbildung verschlimmern, Immunzellen anlocken und die Gewebereparatur stören und so einen Teufelskreis aus Schäden und chronischer Funktionsstörung erzeugen. Durch das Auswerten öffentlicher Genexpressionsdatensätze aus Mausherzen nach Ischämie‑Reperfusion und das Abgleichen mit Hunderten von Genen, die mit zellulärem Altern verbunden sind, begrenzte das Team die Liste auf 26 Gene, deren Expression sich nach der Schädigung deutlich verändert.
Sechs Gene, die einen diagnostischen Fingerabdruck bilden
Um aus diesen 26 Genen die aussagekräftigsten Signale zu finden, nutzten die Forscher mehrere Methoden des maschinellen Lernens. Diese Algorithmen suchen nach Genkombinationen, die verletzte Herzen am besten von gesunden unterscheiden. Nach Analysen mit logistischer Regression, LASSO und Support‑Vector‑Machine traten sechs Gene als leistungsfähiges diagnostisches Panel hervor: CDKN2B, ID1, STAT3, TERF2, TP53 und ZNF277. Zusammen konnten ihre Aktivitätsmuster Ischämie‑Reperfusions‑Schäden in den kombinierten Datensätzen mit sehr hoher Genauigkeit identifizieren und übertrafen in internen Tests viele traditionelle Blutmarker. Gen‑Weg‑Analysen verbanden diese Marker mit Stress‑Antwort‑Schaltkreisen, die oxidativen Schaden, Programme des Zelltods und bekannte Signalwege wie MAPK und PI3K–AKT umfassen — alles Prozesse, die mitentscheiden, ob eine Zelle sich erholt oder in dauerhafte Seneszenz abrutscht.
Wie das Immunsystem die Geschichte ergänzt
Schäden durch wiederhergestellte Durchblutung entstehen nicht isoliert; Immunzellen strömen schnell ins Herz ein. Durch Schätzung der Aktivität von Immunzellen aus denselben Genexpressionsdaten fand die Studie deutliche Hinweise auf verstärkte Immunbeteiligung in verletzten Herzen, einschließlich verschiedener Typen von T‑Zellen, B‑Zellen, Makrophagen und Mastzellen. Ein altersassoziiertes Gen, CDKN2B, korrelierte stark mit zentralen Gedächtnis‑CD4‑T‑Zellen, während TP53 mit aktivierten Mastzellen verknüpft war. Diese Verbindungen deuten darauf hin, dass Alterungswege in Herzmuskelzellen und Veränderungen im Immunsystem sich gegenseitig verstärken: älter wirkende Zellen rufen Immunhilfe herbei, und diese Immunreaktionen können wiederum Schaden und Vernarbung vertiefen.
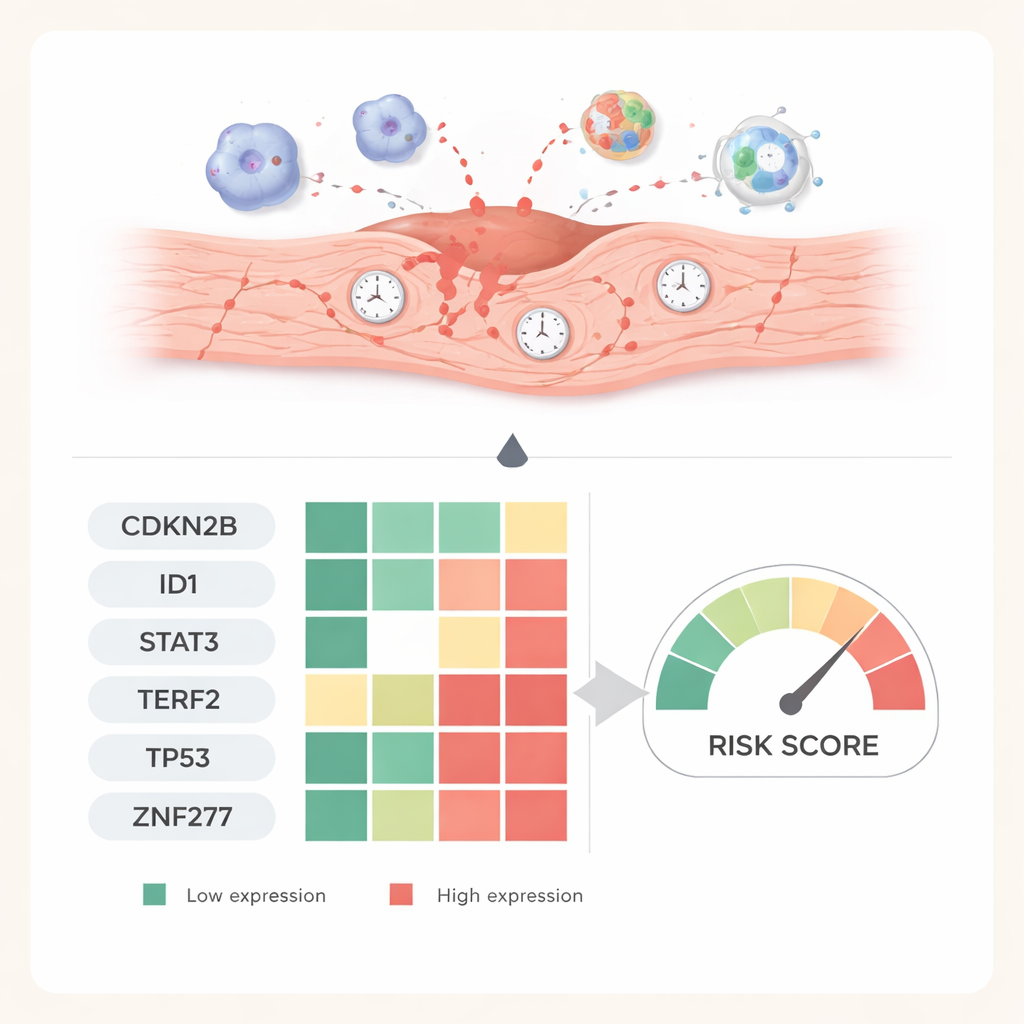
Von Computer‑Vorhersagen zu lebenden Herzen
Um zu prüfen, ob diese sechs Gene über Computeranalysen hinaus bedeutsam sind, erzeugten die Forschenden ein Mausmodell des Ischämie‑Reperfusions‑Schadens. Sie maßen die Genaktivität zu verschiedenen Zeitpunkten nach Wiederherstellung der Durchblutung und nutzten Gewebefärbungen, um die entsprechenden Proteine in Herzschnitten zu visualisieren. Ein Gen, CDKN2B, stieg über eine Woche hinweg kontinuierlich an, was darauf hindeutet, dass es hilft, geschädigte Zellen in einen langfristigen seneszenten Zustand zu versperren. Andere Gene, darunter ID1, STAT3, TP53, TERF2 und ZNF277, fielen früh stark ab und erholten sich dann allmählich, was Verschiebungen zwischen akutem Stress, aktiver Schädigung und späterer Reparatur widerspiegelt. Diese zeitabhängigen Muster stützen die Idee, dass jedes Gen eine andere Phase der Reaktion des Herzens erfasst.
Was das für Patientinnen und Patienten bedeuten könnte
Für Laien ist die Kernaussage, dass die Studie Herz‑infarkt‑assoziierte Schäden mit der Biologie zellulären Alterns verknüpft und einen sechs‑Gen‑„Fingerabdruck“ identifiziert, der diesen Schaden in experimentellen Modellen markiert. Obwohl die Arbeit noch präklinisch ist und hauptsächlich auf Mäusedaten sowie öffentlichen Datenbanken beruht, bietet sie eine Roadmap für neue Blut‑ oder Gewebetests, die Ischämie‑Reperfusions‑Schäden früher und spezifischer erkennen könnten als heutige Werkzeuge. Langfristig könnte das Verständnis, wie diese alternsbezogenen Gene Entzündung, Vernarbung und Reparatur steuern, Wege zu Behandlungen eröffnen, die nicht nur blockierte Arterien wiedereröffnen, sondern dem wiederbelebten Herzen auch helfen, vollständiger zu heilen.
Zitation: Sun, L., Liu, H., Jia, T. et al. The role of cellular senescence-related genes in ischemia–reperfusion injury and the identification of their biomarkers. Sci Rep 16, 5211 (2026). https://doi.org/10.1038/s41598-026-36076-2
Schlüsselwörter: Ischämie‑Reperfusions‑Schaden, zelluläre Seneszenz, Herzinfarkt, Biomarker, Immun‑Entzündung