Clear Sky Science · de
Expression des Sphingosin-1-phosphat-Rezeptors 1 im Gehirn bei tödlichem zerebralen Malaria
Warum dieser Gehirn–Malaria-Zusammenhang wichtig ist
Zerebrale Malaria ist eine der tödlichsten Komplikationen einer Malaria-Infektion und tötet viele Patienten, selbst wenn sie moderne Medikamente erhalten. Diese Studie schaut ins Gehirn, um zu verstehen, warum Blutgefäße bei den schwerst Erkrankten zu lecken beginnen und versagen. Indem sie sich auf ein fettartiges Signalmolekül namens Sphingosin-1-phosphat (S1P) und dessen Rezeptor S1PR1 konzentrieren, untersuchen die Forschenden, ob diese chemische Kommunikation zwischen Blut und Gehirn erklären könnte, wer überlebt, wer stirbt und wie wir das Gehirn in künftigen Therapien besser schützen könnten.
Was im Gehirn bei schwerer Malaria passiert
Bei zerebraler Malaria werden von dem Parasiten Plasmodium falciparum infizierte Erythrozyten klebrig und haften an der Innenwand kleiner Gehirngefäße. Das Team untersuchte konserviertes Hirngewebe von Menschen, die an Malaria gestorben waren, und verglich es mit Patienten mit milderer, nicht-zerebraler Malaria sowie mit Nicht-Malaria-Kontrollen. In den tödlichen zerebralen Fällen sahen sie Gefäße, die mit parasitenbefüllten roten Blutkörperchen verstopft waren, winzige punktförmige Blutungen, ringförmige Blutungszonen und Ansammlungen von Stützzellen, sogenannte Dürck-Granulome. Diese Veränderungen deuten auf verstopfte Gefäße, schlechte Sauerstoffversorgung und Schäden an der normalerweise dichten Blut‑Hirn‑Schranke hin, die das Milieu des Gehirns stabil hält. 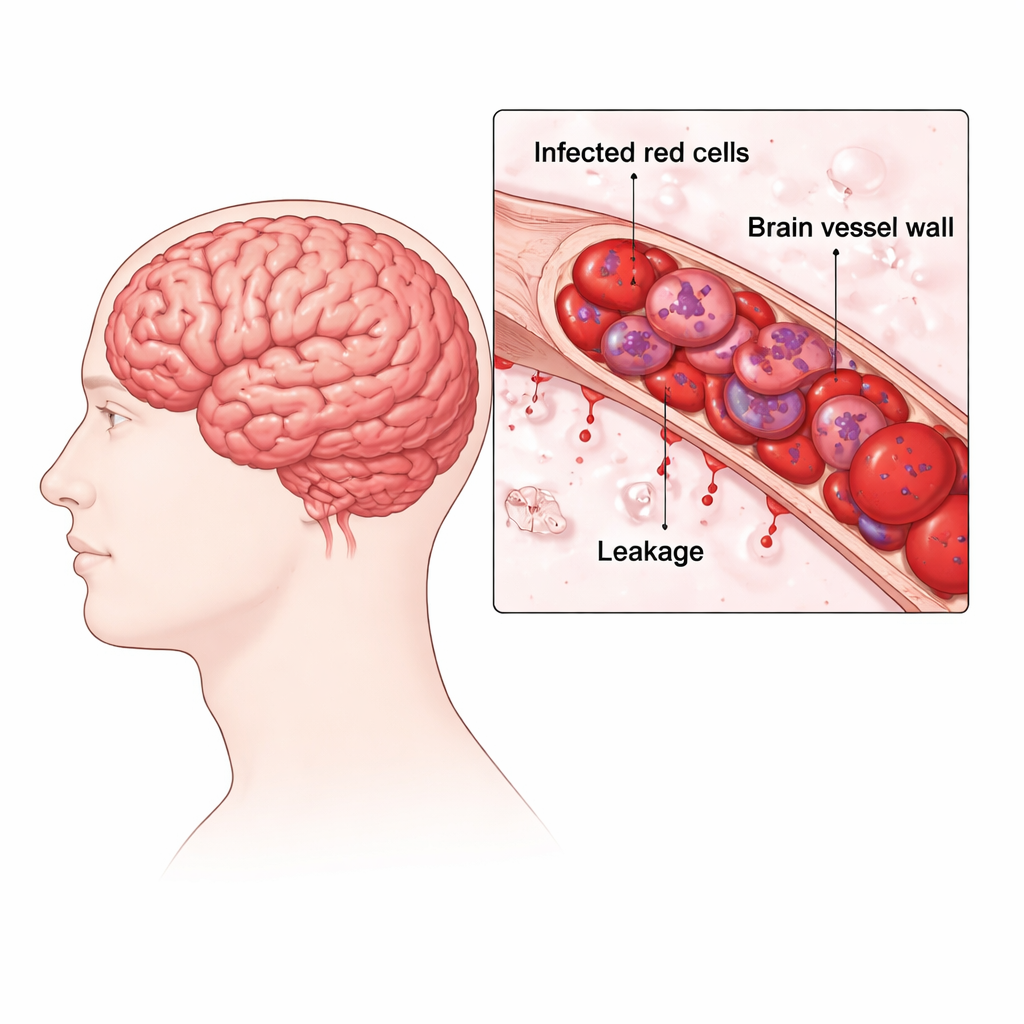
Ein chemischer Wächter der Gefäßdichtheit
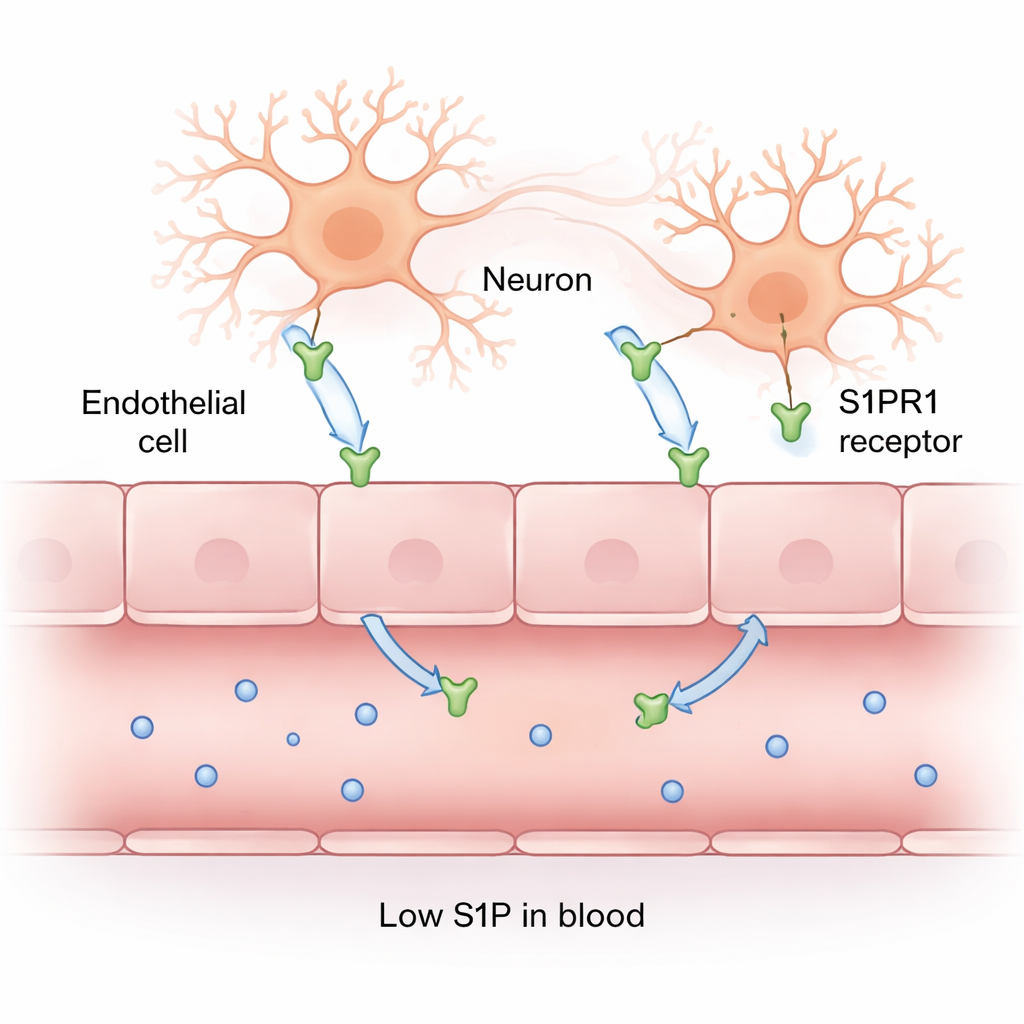
Unter gesunden Bedingungen hilft S1P — das hauptsächlich in Erythrozyten und Thrombozyten gespeichert ist — dabei, Blutgefäße verschlossen zu halten. Es bindet an Rezeptoren wie S1PR1 an der Oberfläche von Gefäßauskleidungszellen und Gehirnzellen und verstärkt so die Verbindungen zwischen ihnen. Die Forschenden maßen S1P‑Spiegel in Blutproben und fanden bei Patienten mit zerebraler Malaria einen markanten Abfall: Ihre S1P‑Werte lagen etwa viermal niedriger als bei Menschen ohne Malaria und ungefähr halb so hoch wie bei Patienten mit nicht-zerebraler Malaria. Das legt nahe, dass mit der Zerstörung oder Verformung roter Blutkörperchen durch die Malaria und der Schädigung von Gefäßzellen die körpereigene Versorgung mit diesem schützenden Molekül gerade dann schwindet, wenn sie am dringendsten gebraucht wird.
Wo und wie der Rezeptor aufleuchtet
Als Nächstes nutzte das Team Immunhistochemie — eine Färbemethode, die bestimmte Proteine unter dem Mikroskop sichtbar macht —, um S1PR1 im Gehirn zu kartieren. In gesunden Kontrollgehören und bei nicht-zerebraler Malaria war die S1PR1-Färbung in Neuronen und Gefäßen schwach. Im Gegensatz dazu zeigten Gehirne von Patienten mit zerebraler Malaria eine intensive S1PR1-Färbung in den Gefäßwandzellen und in Neuronen, während benachbarte Stützzellen, die Glia, wenig bis kein Signal zeigten. Als die Wissenschaftler dies quantifizierten, waren die S1PR1‑„Werte“ in Gefäßen und Neuronen bei zerebraler Malaria deutlich höher als in den anderen Gruppen. Je mehr parasitengefüllte rote Blutkörperchen in den Gefäßen festsaßen, desto höher war die S1PR1‑Expression und desto niedriger der S1P‑Spiegel im Blut — ein enger Zusammenhang zwischen Parasitenlast, Rezeptoraktivierung und Verlust des schützenden Signals.
Ein mögliches Teufelskreis-Modell
Das Muster deutet auf einen möglichen Teufelskreis hin. Wenn infizierte Zellen Gehirngefäße verstopfen, fällt der Sauerstoffgehalt und die Entzündung nimmt zu. Die Blutspiegel von S1P sinken wahrscheinlich, weil geschädigte Erythrozyten, Thrombozyten und Gefäßzellen die normalen Vorräte nicht mehr aufrechterhalten können. Gleichzeitig erhöhen Gefäßzellen und Neuronen die S1PR1‑Expression, möglicherweise um das wenige verbleibende S1P zu binden und die Barrierefunktion wiederherzustellen. Doch diese verstärkte Rezeptoraktivität könnte weiter S1P aus dem Kreislauf ziehen und sogar die entzündlichen Signalwege im Gehirn verändern. Das Ergebnis sind zunehmende Gefäßundichtigkeit, mehr Blutungen ins Hirngewebe und eine Vertiefung neurologischer Schäden.
Was das für zukünftige Behandlungen bedeuten könnte
Für Nicht-Spezialisten lautet die Kernbotschaft: Das S1P–S1PR1‑System wirkt wie ein stabilisierender „Klebstoff“ für Gehirngefäße, und dieser Klebstoff scheint bei zerebraler Malaria zu versagen. Patienten, die an dieser Erkrankung sterben, zeigen sehr niedrige S1P‑Spiegel im Blut und sehr hohe Spiegel seines Rezeptors an Gefäßen und Neuronen im Gehirn. Die Studie beweist noch keine Kausalität, stärkt aber die Idee, dass Medikamente, die das S1P‑Signaling fördern oder S1PR1 gezielt modulieren — einige davon existieren bereits für andere Krankheiten — eines Tages zusammen mit Antimalariamitteln eingesetzt werden könnten, um die Gefäße im Gehirn intakt zu halten und Todesfälle durch diese verheerende Erkrankung zu verringern.
Zitation: Srisook, C., Nintasen, R., Punsawad, C. et al. Expression of sphingosine-1-phosphate receptor 1 in the brain of fatal cerebral malaria. Sci Rep 16, 5641 (2026). https://doi.org/10.1038/s41598-026-36072-6
Schlüsselwörter: zerebrale Malaria, Blut-Hirn-Schranke, Sphingosin-1-phosphat, Endothelzellen, Hirnentzündung