Clear Sky Science · de
ACE2-Expression in kolorektalen Epithelzellen steht im Zusammenhang mit Virusinfektion, Immunität und Energiestoffwechsel
Warum der Darm bei einem Atemwegsvirus wichtig ist
Wenn wir an COVID-19 denken, stellen wir uns Lungen vor, die sich mit Flüssigkeit füllen, und Patientinnen und Patienten, die schwer atmen. Viele Menschen mit einer SARS-CoV-2-Infektion entwickeln jedoch auch Bauchschmerzen, Durchfall und lang anhaltende Darmbeschwerden. Diese Studie untersucht, warum der Darm — insbesondere der Dickdarm — ein wichtiges Ziel für das Virus sein könnte. Indem die Forschenden einzelne Zellen aus Kinderkolonproben genau untersuchen, zeigen sie, dass ein wichtiges virales Eintrittstor, das ACE2-Protein, in bestimmten Darmzellen stark aktiv ist und nicht nur mit Virusinfektion, sondern auch mit unseren Immunabwehrmechanismen und der zellulären Energieverwaltung verknüpft ist.
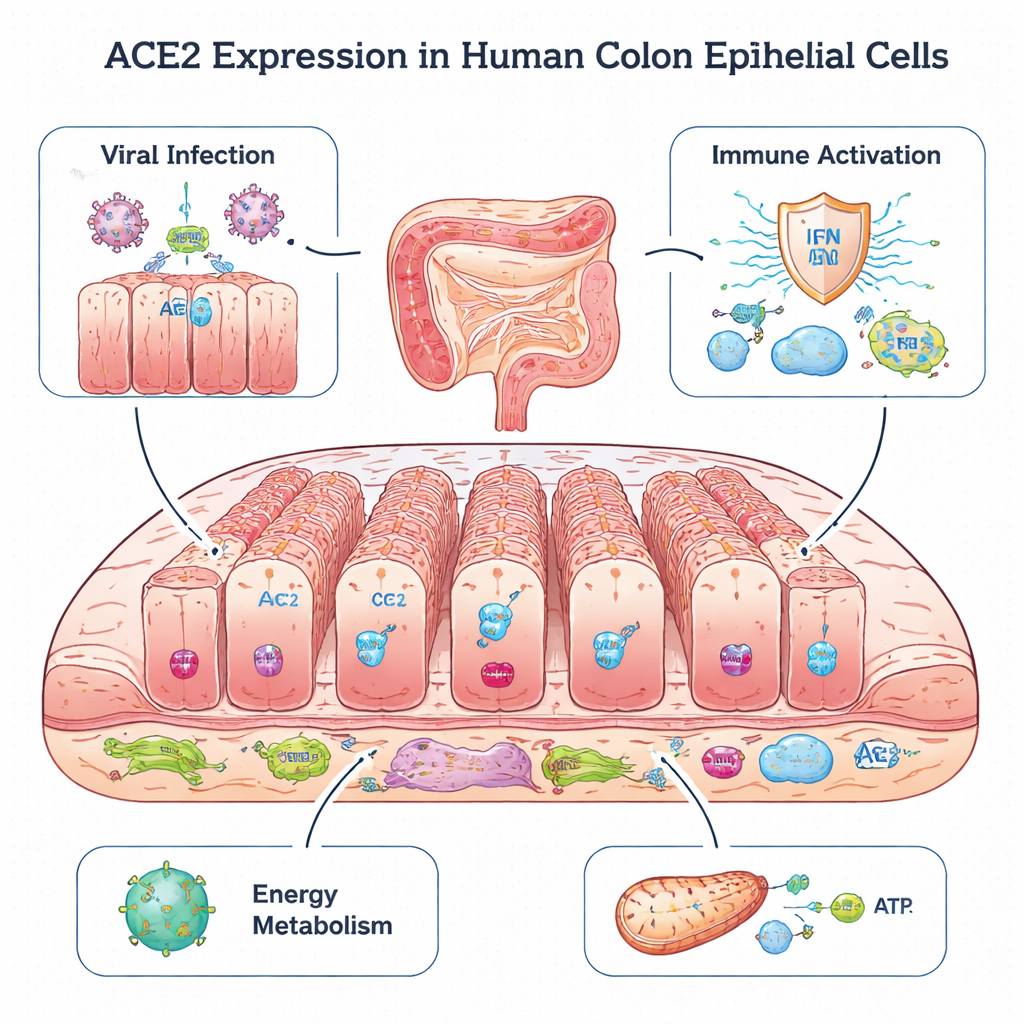
Eine zelluläre Tür im Dickdarm
ACE2 ist vor allem als Haupteintrittspunkt bekannt, den sowohl das ursprüngliche SARS-Virus als auch SARS‑CoV‑2 zur Infektion von Lungenzellen nutzen. Paradoxerweise deuten Tierversuche darauf hin, dass ACE2 Gewebe auch vor Schäden schützen kann, indem es ein Hormonsystem, das den Blutdruck steuert, im Gleichgewicht hält. Im Darm ist bekannt, dass ACE2 eine gesunde Mikrobiota unterstützt und Entzündungen verhindert. In dieser Arbeit werteten die Wissenschaftler erneut Einzelzell-RNA-Sequenzierungsdaten aus Kolonbiopsien von 17 Kindern aus: Einige hatten gesunde Darmschleimhaut, andere Kolitis oder entzündliche Darmerkrankungen wie Colitis ulcerosa und Morbus Crohn. Diese Methode ermöglichte es ihnen, zu sehen, welche Gene in Tausenden einzelner Zellen aktiv sind, und genau zu bestimmen, wo ACE2 eingeschaltet ist.
Kolonozyten: bevorzugte Ziele und erste Reaktionszellen
Die Analyse zeigte, dass ACE2 nahezu ausschließlich in Kolonozyten konzentriert ist, einer wichtigen Epithelzellart, die das Innere des Dickdarms auskleidet und dem Darminhalt zugewandt ist. Im Vergleich zu anderen Epithelzellen zeigten Kolonozyten außerdem eine höhere Aktivität von Genen, die Viren beim Eintritt, bei der Abschnürung und beim Austritt aus der Zelle helfen. Gleichzeitig exprimierten diese Zellen viele Gene, die virale genetische Signale erkennen und Typ‑I- sowie Typ‑III-Interferonantworten auslösen — zentrale frühe Alarmsysteme der Immunabwehr. Sie produzierten außerdem Entzündungssignale und Moleküle, die virale Fragmente T-Zellen präsentieren, was darauf hindeutet, dass Kolonozyten sowohl potenzielle virale Ziele als auch wichtige frühe Wächter sind, die das Immunsystem alarmieren.
Verknüpfte Netzwerke von Immunität und Energieverbrauch
Die Forschenden fragten anschließend, welche anderen Gene in Kolonozyten typischerweise gemeinsam mit ACE2 ein- oder ausgeschaltet werden. Sie fanden über 3.400 Gene, deren Expression mit steigenden ACE2-Spiegeln zunahm, und mehr als 2.100 Gene, die mit zunehmendem ACE2 abnahmen. Gene, die positiv mit ACE2 korrelierten, waren angereichert in Prozessen, die mit viralen Eintritts- und Freisetzungsmechanismen, angeborener Immunantwort, der tödlichen Aktivität natürlicher Killerzellen und T-Zellen sowie mehreren energieerzeugenden Stoffwechselwegen innerhalb der Zelle zusammenhängen — einschließlich mitochondrialer Funktion und Verarbeitung von Fetten und Zucker. Im Gegensatz dazu standen Gene, die in die entgegengesetzte Richtung liefen — hoch, wenn ACE2 niedrig war — in Zusammenhang mit der humoralen (antikörpervermittelten) Immunität, der zellulären Proteinbaufabrik, zellulären „Fress“-Prozessen wie Phagozytose und dem Komplementsystem, einem weiteren Arm der Immunabwehr. Dieses Muster legt nahe, dass ACE2 einen Zustand markiert, in dem Kolonozyten auf schnelle antivirale Erkennung und Energieproduktion eingestellt sind, während andere, langsamere Immunprogramme heruntergeregelt sind.
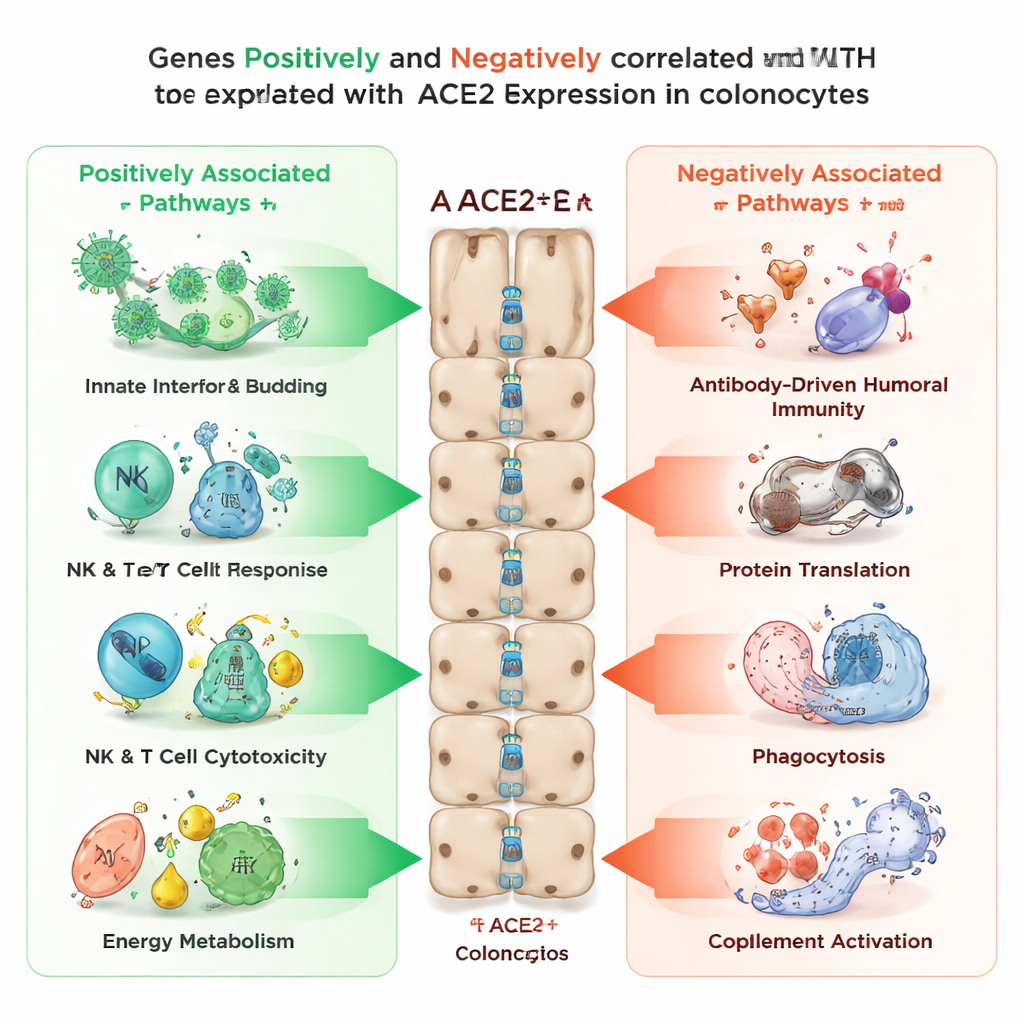
Hinweise aus entzündetem Darmgewebe
Um zu prüfen, ob diese Muster auch in tatsächlichen Geweben vorkommen, verwendete das Team Multiplex-Immunfluoreszenz — eine Technik, die spezifische Proteine in verschiedenen Farben sichtbar macht — an Kolonproben von Kindern mit Colitis ulcerosa, Morbus Crohn und von Kontrollpersonen. Sie bestätigten, dass das ACE2-Protein hauptsächlich auf Epithelzellen sitzt, die durch EPCAM markiert sind. Bei Patientinnen und Patienten mit entzündlichen Darmerkrankungen zeigten ACE2-positive Zellen höhere Werte von IFNA4 und RSAD2, zwei Proteinen, die stark mit Interferon-Signalisierung und antiviraler Aktivität assoziiert sind. Das deutet darauf hin, dass ACE2-tragende Kolonzellen im entzündeten Darm nicht nur potenzielle Eintrittstore für Viren sind, sondern auch Brennpunkte antiviraler Reaktion.
Was das für Patientinnen und Patienten und künftige Therapien bedeutet
Für Nicht‑Fachleute lautet die Botschaft: Der Dickdarm ist bei COVID‑19 kein passiver Zuschauer. Dasselbe Protein, das dem Virus den Eintritt in Zellen ermöglicht, hilft auch dabei, Darmimmunität und Energiehaushalt zu koordinieren — besonders bei Kindern mit bereits bestehender Darmentzündung. Diese doppelte Rolle könnte erklären, warum manche Patientinnen und Patienten gastrointestinale Symptome entwickeln und warum Menschen mit entzündlichen Darmerkrankungen komplexe, aber nicht einheitlich schlechtere Verläufe bei COVID‑19 zeigen. Die Arbeit fließt auch in breitere Diskussionen über Medikamente ein, die auf Blutgerinnung und Blutdruckwege wirken, von denen einige Lungen- und Gefäßschäden bei schweren Infektionen abschwächen könnten. Zwar beruhen die Befunde auf Korrelationen und können keine Ursache‑Wirkung‑Beziehung beweisen, doch heben sie ACE2-reiche Kolonozyten als wichtige Akteurinnen und Akteure an der Schnittstelle von Viruseintritt, Immunabwehr und Metabolismus hervor — und weisen den Darm als ein zentrales, potenziell therapeutisch zugängliches Feld bei der Coronavirus-Erkrankung aus.
Zitation: Qi, Y., Huang, Y., Chen, H. et al. ACE2 expression by colonic epithelial cells is associated with viral infection, immunity, and energy metabolism. Sci Rep 16, 5738 (2026). https://doi.org/10.1038/s41598-026-36052-w
Schlüsselwörter: ACE2, Kolonozyten, COVID-19 Darm, entzündliche Darmerkrankung, antivirale Immunität