Clear Sky Science · de
Proteomische Analyse des Sekretoms von endothelialen Vorläuferzellen identifiziert Serpine 1 als starken Regulator der Osteogenese
Gebrochenen Knochen heilen ohne Spendertransplantate
Wenn ein Knochen schwer beschädigt ist oder ein Stück fehlt, tun sich Chirurgen oft schwer, sowohl Festigkeit als auch Form wiederherzustellen. Die heute gebräuchlichen Optionen — Knochenentnahme aus einem anderen Körperbereich oder synthetische Transplantate — können schmerzhaft, riskant und nicht immer erfolgreich sein. Diese Studie untersucht eine andere Idee: Statt Zellen zu transplantieren, kann man genau die natürlichen Proteine liefern, die die körpereigene knochenbildende Maschinerie einschalten?
Warum manche Knochenverletzungen nicht heilen
Die meisten Brüche heilen von selbst, doch große Knochendefekte — etwa durch Trauma, Tumoren oder starken Knochenabbau im Kiefer — tun das häufig nicht. In solchen Fällen fehlen dem Körper lokal genügend Blutgefäßzellen und knochenbildende Stammzellen, um das fehlende Segment wieder aufzubauen. Forscher im Bereich Gewebeengineering versuchen, dies mit drei Komponenten zu lösen: lebenden Zellen, die neuen Knochen bilden können, einem Gerüst, an dem sie wachsen, und Signalen, die ihnen sagen, was zu tun ist. Zelltransplantationen können funktionieren, sind jedoch teuer, stark reguliert und nicht immer praktisch für den klinischen Alltag. Das hat Wissenschaftler dazu getrieben, nach „zellfreien“ Lösungen zu suchen, die auf intelligenten Biomaterialien und sorgfältig gewählten Proteinen basieren.
Geheime Signale von gefäßbildenden Zellen
Endotheliale Vorläuferzellen sind seltene Blutzellen, die beim Aufbau neuer Blutgefäße helfen. Frühere Arbeiten zeigten, dass diese Zellen, wenn sie in der Nähe von Knochen implantiert werden, die Heilung fördern — vor allem durch lösliche Signale, nicht dadurch, dass sie selbst zu Knochen werden. In der neuen Studie sammelten die Autoren das Kulturmedium, in dem diese Zellen gewachsen waren, und nutzten fortschrittliche Proteomanalysen, um hunderte sekretierter Moleküle zu katalogisieren. Sie konzentrierten sich auf acht Proteine, die stark mit Gefäßwachstum und Knochenbildung verknüpft sind. Mit humanen Knochenmarkstammzellen und humanen mikrovaskulären Endothelzellen im Labor testeten sie systematisch, welche dieser Proteine am besten Zellwachstum fördert, Migration lenkt und knochenähnliche Mineralablagerungen auslöst.
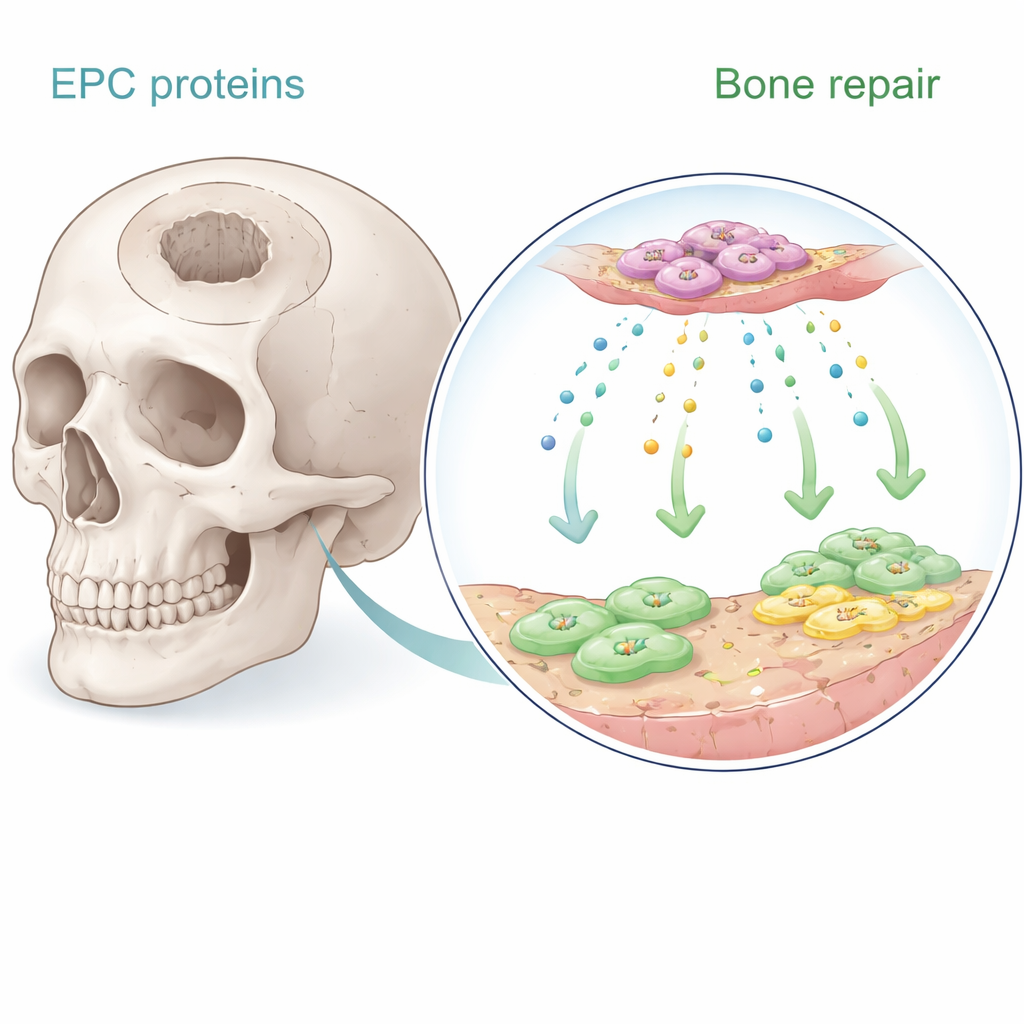
Ein überraschendes Protein übernimmt die Führung
Unter den Kandidaten stach ein Protein besonders hervor: Serpine-1, besser bekannt für seine Rolle bei der Blutgerinnungsregulation und Wundheilung. In Kulturschalen erhöhte Serpine-1 dosisabhängig die Proliferation sowohl von Knochenmarkstammzellen als auch von Endothelzellen deutlich und schnitt in dieser Hinsicht besser ab als bekannte Wachstumsfaktoren wie BMP-2 und SDF-1. Es förderte außerdem die Reifung von Stammzellen zu knochenbildenden Zellen, wie klassische Färbemethoden zeigten, die alkalische Phosphataseaktivität und calciumreiche Mineralablagerungen sichtbar machen. Andere Proteine, etwa Thrombozyten‑abgeleitete Wachstumsfaktoren und BMP-2, waren in Migrationsassays wirksamer darin, Zellen in eine "Wund"-Zone kriechen zu lassen, doch Serpine-1 bot die seltene Kombination, sowohl Zellzahl als auch knochenbildendes Verhalten zu steigern.
Ein Protein in ein praktikables Implantat verwandeln
Ein vielversprechendes Protein zu finden ist nur die halbe Herausforderung; es muss auch kontrolliert an die Verletzungsstelle abgegeben werden. Das Team kapselte Serpine-1 in winzige biologisch abbaubare Kügelchen aus dem medizinischen Polymer PLGA und mischte diese Mikrosphären in ein weiches Kollagengel. So entstand ein Gerüst, das das Protein über die Zeit langsam freisetzte. Sie testeten es in Mäusen, indem sie ein 4‑Millimeter‑rundes Loch in den Schädel bohrten — eine Defektgröße, die von selbst nicht heilt. Einige Defekte wurden nur mit Kollagen gefüllt, einige mit Kollagen plus leeren Mikrosphären, und einige mit dem Serpine-1-beladenen Gerüst. Nach acht Wochen zeigten hochauflösende Mikro‑CT‑Scans, dass die Serpine-1‑Gruppe signifikant höhere Knochenmasse, Dichte und Dicke im Defekt aufwies. Bemerkenswerterweise entwickelten nur diese Tiere neuen Knochen in der Mitte der Lücke und nicht nur entlang der Ränder.
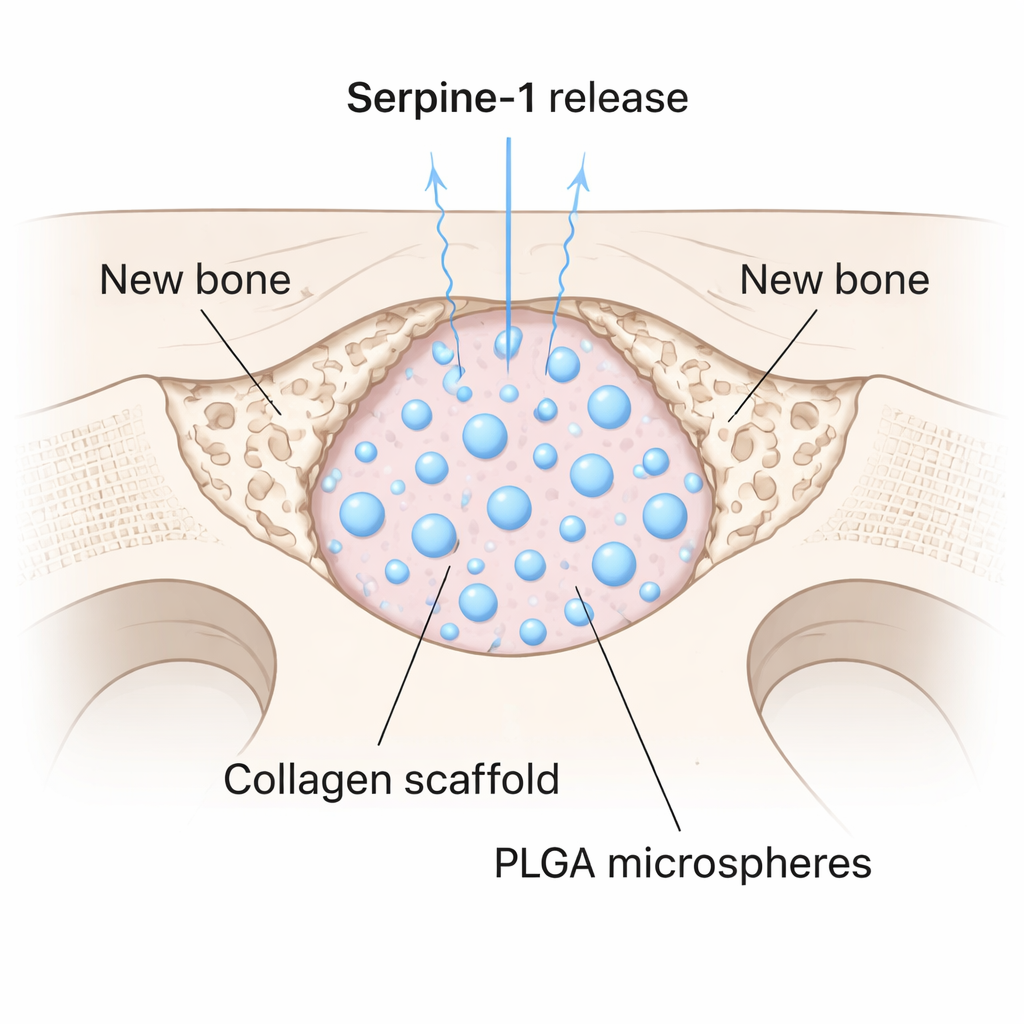
Was das für die zukünftige Knochenversorgung bedeuten könnte
Die Studie stellt Serpine-1 als ein starkes und bislang unterschätztes Signal für Knochenbildung vor. Durch die Kombination dieses Proteins mit einem langsam freisetzenden Gerüst erzielten die Forscher einen bedeutsamen Knochenneubau in einem Defekt, der normalerweise leer bleiben würde. Zwar zog Serpine-1 Zellen nicht so stark in den Defekt wie manche anderen Faktoren, doch seine Fähigkeit, vorhandene Zellen zu vermehren und zu reifen, legt nahe, dass es mit migrationsfördernden Proteinen kombiniert werden könnte, um noch bessere Ergebnisse zu erzielen. Für Patientinnen und Patienten könnten solche zellfreien, proteinbasierten Materialien eines Tages den Bedarf an Knochentransplantaten aus dem eigenen Körper oder an komplexen Zelltherapien verringern und einen einfacheren Weg bieten, hartnäckige Knochenverletzungen zur Heilung zu bringen.
Zitation: Asbi, T., Tamari, T., Doppelt-Flikshtain, O. et al. Proteomic analysis of endothelial progenitor cells secretome identifies Serpine 1 as a potent regulator of osteogenesis. Sci Rep 16, 5165 (2026). https://doi.org/10.1038/s41598-026-36048-6
Schlüsselwörter: Knochenregeneration, Serpine-1, Gewebeengineering, endotheliale Vorläuferzellen, Kollagengerüst