Clear Sky Science · de
Alzheimer-bezogene Demenzschwereklassifikation aus Magnetresonanztomographie mittelsableitungsfreier Optimierung eines Faltungsneuronalen Netzes
Ärzten helfen, Demenz früher zu erkennen
Mit dem Älterwerden der Bevölkerung sorgen sich viele Familien um Gedächtnisverlust und Demenz. Hirnscans können frühe Veränderungen im Zusammenhang mit Alzheimer aufzeigen, doch das visuelle Auswerten tausender Bilder ist selbst für Expertinnen und Experten zeitaufwändig und schwierig. Diese Studie stellt ein intelligentes Computerwerkzeug vor, das MRT-Aufnahmen des Gehirns analysiert und Personen in vier Demenzschweregrade einordnet – von keiner Demenz bis zu mäßiger Beeinträchtigung. Das System ist so konzipiert, dass es sowohl hohe Genauigkeit erzielt als auch schlank genug ist, um auf gewöhnlichen Krankenhauscomputern zu laufen, wodurch fortgeschrittene Bildanalyse breiter zugänglich wird.
Ein neuer intelligenter Helfer für Hirnscans
Die Forschenden konzentrieren sich auf eine Form künstlicher Intelligenz, das Faltungsneuronale Netz (Convolutional Neural Network, CNN), das besonders gut Muster in Bildern erkennt. Statt nur zu entscheiden, ob jemand Alzheimer hat, unterscheidet ihr Werkzeug vier Stadien: keine Demenz, sehr leicht, leicht und mäßig. Dazu trainierte das Team sein Modell an großen öffentlichen Sammlungen von MRT-Aufnahmen, die bereits von Expertinnen und Experten beschriftet waren. Das Ziel war zweigleisig: nahezu perfekte Genauigkeit zu erreichen und das Modell gleichzeitig kompakt und schnell zu halten, sodass es für den klinischen Alltag praktikabel ist und nicht nur in gut ausgestatteten Forschungslabors eingesetzt werden kann.
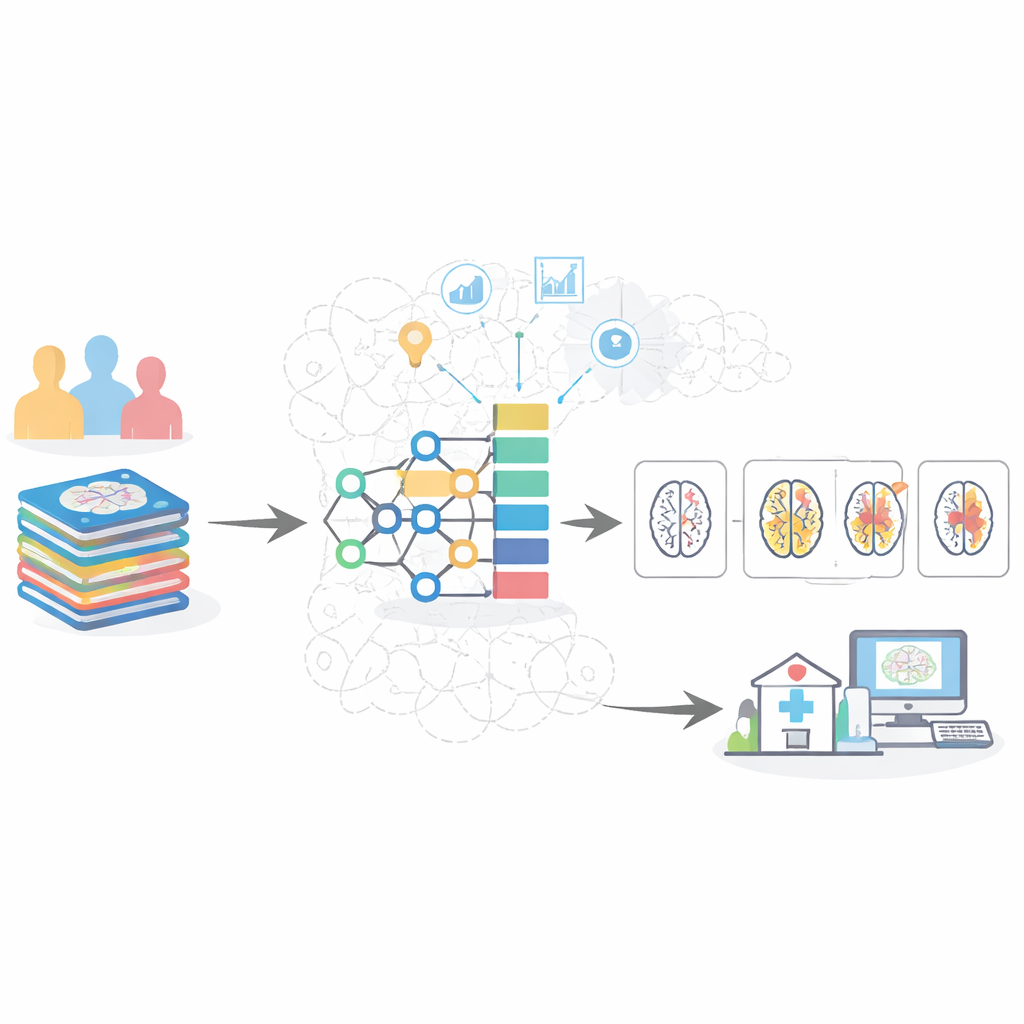
Ausbalancieren der Daten und Bereinigen der Bilder
Eine zentrale Herausforderung in medizinischen Daten ist, dass nicht alle Krankheitsstadien gleich häufig vertreten sind. In diesen Hirnscan-Sammlungen sind gesunde und sehr leichte Fälle häufig, während Scans mit mäßiger Demenz deutlich seltener sind. Konventionelle KI-Systeme neigen dann dazu, die häufigeren Klassen zu bevorzugen und frühe oder moderate Erkrankungen zu übersehen. Um dem entgegenzuwirken, nutzten die Autorinnen und Autoren eine Zweiphasenstrategie: Zunächst entfernten sie verwirrende Randfälle und anschließend erzeugten sie realistische synthetische Beispiele der unterrepräsentierten Stadien. Parallel dazu bereiteten sie jede MRT-Scheibe sorgfältig vor, indem sie filterten, das Gehirn vom umliegenden Gewebe isolierten und Helligkeit sowie Kontrast normalisierten, sodass das Modell sich auf medizinisch aussagekräftige Merkmale wie Schrumpfung tiefliegender Gedächtnisstrukturen und Weitung flüssigkeitsgefüllter Räume konzentrieren konnte.
Entwurf eines kleineren, schlaueren Netzes
Statt sich auf traditionelle Trainingsmethoden zu stützen, die Parameter über mathematische Gradienten anpassen, verwendete das Team eine Familie sogenannter ableitungsfreier Optimierungstechniken. Sie begannen mit einem größeren, konventionellen CNN und nutzten dann evolutionäre Suche und Neural Architecture Search, um ein einfacheres Design mit nur drei Faltungsschichten und deutlich weniger Filtern zu entwickeln. Bayesianische Optimierung verfeinerte anschließend die Trainingsparameter, während simuliertes Glühen (Simulated Annealing) und Pruning nach dem Training unnötige Verbindungen entfernten. Das Endergebnis, DAPA-CNN genannt, hat etwa 85 % weniger einstellbare Parameter als das Ausgangsmodell, benötigt rund ein Viertel des Speichers und trainiert in weniger als zwei Dritteln der Zeit, fängt aber dennoch die entscheidenden Muster in den Scans ein.
Beinahe perfekte Leistung und klare visuelle Erklärungen
Trotz seiner geringeren Größe erwies sich DAPA-CNN als bemerkenswert genau. In einem großen Alzheimer-Datensatz ordnete es das Demenzstadium in fast allen Fällen korrekt zu, wobei Genauigkeit und andere Leistungsmaße alle bei etwa 99 % lagen. Das Modell generalisierte zudem gut auf einen separaten, multizentrischen Datensatz, der auf anderen Geräten erhoben wurde, was auf Robustheit gegenüber realen Bildgebungsvariationen hindeutet. Um das System für Klinikerinnen und Kliniker transparenter zu machen, erzeugten die Autorinnen und Autoren Class Activation Maps – hitzeähnliche Überlagerungen, die zeigen, welche Regionen des Gehirns eine bestimmte Entscheidung beeinflusst haben. In frühen Stadien heben diese Karten Bereiche hervor, die an Gedächtnisprozessen beteiligt sind und bei Alzheimer zuerst geschädigt werden; in späteren Stadien weiten sie sich auf größere kortikale Regionen aus und stimmen so mit dem klinischen Verständnis des Krankheitsverlaufs überein.
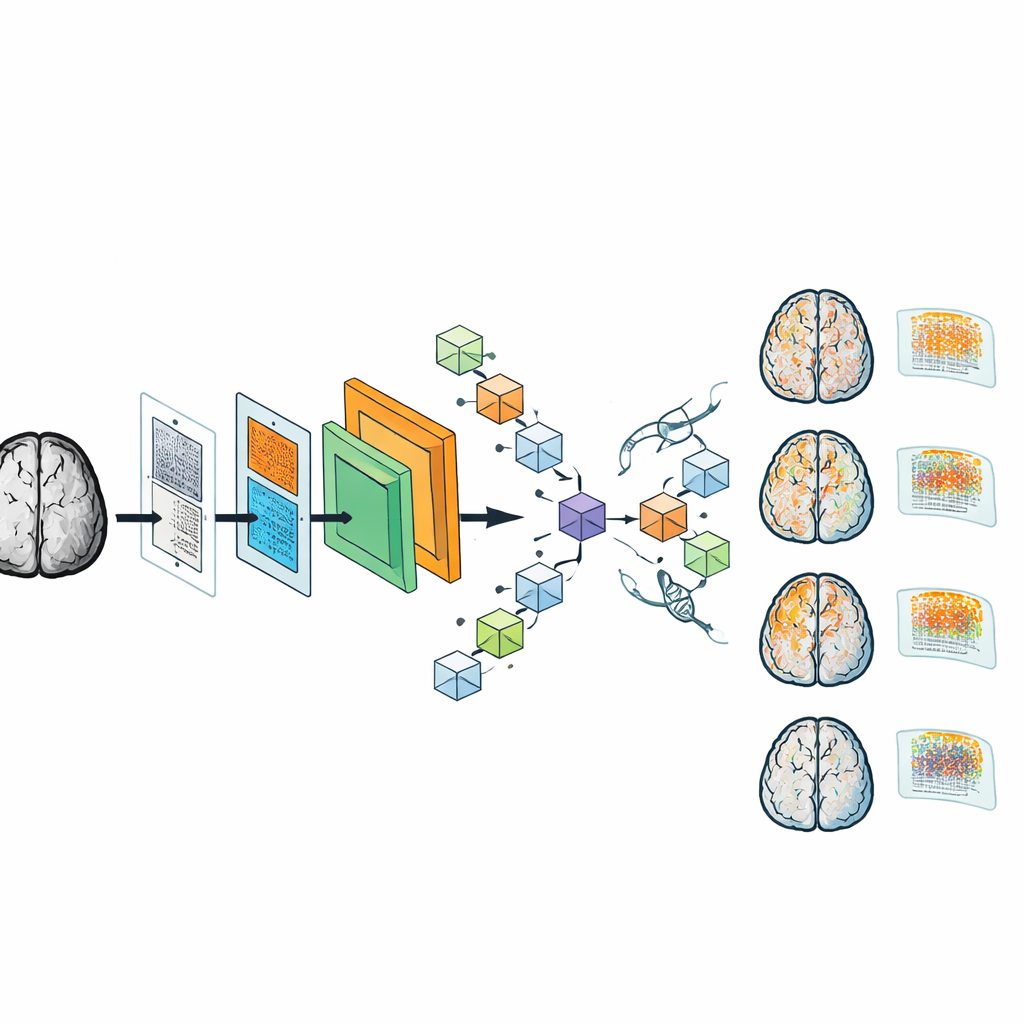
Was das für Patientinnen, Patienten und Kliniken bedeutet
Für Nicht-Spezialisten ist die Hauptaussage, dass die Studie ein schnelles, kompaktes und interpretierbares Werkzeug zur Einstufung der Demenzschwere aus Routine-MRTs bietet. Durch das Ausbalancieren der Trainingsdaten und die gezielte Formgebung des Netzes mittels ableitungsfreier Optimierung schufen die Autorinnen und Autoren ein Modell, das auf bescheidener Hardware läuft, dabei nahezu perfekte Genauigkeit liefert und die Hirnregionen hervorhebt, die seinen Entscheidungen zugrunde liegen. Wenn dies in zukünftigen prospektiven klinischen Studien bestätigt wird, könnte eine solche Technologie frühere Diagnosen, konsistentere Stadieneinteilung zwischen Krankenhäusern und eine bessere Nachverfolgung der Veränderungen im Gehirn durch die Alzheimer-Krankheit im Zeitverlauf unterstützen.
Zitation: Ganesan, S.K., Velusamy, P., Parthsarathy, P. et al. Alzheimer’s related dementia severity classification from magnetic resonance imaging using derivative-free optimization of convolutional neural network. Sci Rep 16, 10077 (2026). https://doi.org/10.1038/s41598-026-36037-9
Schlüsselwörter: Alzheimer-Krankheit, Hirn-MRT, Demenzstadieneinteilung, Deep Learning, medizinische Bildgebung KI