Clear Sky Science · de
Perivaskuläre Pathologie, nicht makrovaskuläre Komplexität, bestimmt glymphatische‑bezogene Dysfunktion bei präklinischer zerebraler Kleingefäßerkrankung
Warum die Entwässerung des Gehirns vor dem Auftreten von Symptomen wichtig ist
Lange bevor ein Schlaganfall oder Gedächtnisverlust sichtbar wird, können winzige Blutgefäße tief im Gehirn still und schleichend ausfallen. Diese Studie untersucht, wie das Abfallentsorgungssystem des Gehirns, manchmal als „glymphatischer“ Weg bezeichnet, bei vermeintlich gesunden, berufstätigen Erwachsenen beeinträchtigt ist. Durch die Kombination fortschrittlicher Gehirnscans mit Messungen der Gefäßform und des mikroskopischen Flüssigkeitsflusses stellen die Autorinnen und Autoren eine auf den ersten Blick einfache Frage: Wird frühe Störung eher durch die großen Arterien, die das Gehirn versorgen, oder durch Schäden um die kleinsten darin eingebetteten Gefäße verursacht?
Winzige Flüssigkeitskanäle, die das Gehirn reinigen
Das Gehirn produziert ständig Abfallprodukte, während Nervenzellen arbeiten. Um gesund zu bleiben, ist es auf Flüssigkeit angewiesen, die entlang der Außenseiten von Blutgefäßen fließt und über enge Korridore, die perivaskulären Räume genannt werden, Ablagerungen wegspült. Wenn diese Kanäle anschwellen und in der MRT sichtbar vergrößert erscheinen, gilt das als Hinweis darauf, dass dieses Reinigungssystem Schwierigkeiten hat. Diese vergrößerten perivaskulären Räume, oder ePVS, sind zudem ein Kennzeichen der zerebralen Kleingefäßerkrankung, eines langsamen, oft „stillen“ Prozesses, der schließlich zu Schlaganfall und Demenz führen kann. Die Forschenden konzentrierten sich auf Personen ohne Symptome und mit nur niedrigem bis mittlerem kardiovaskulären Risiko, um diesen Prozess in einem sehr frühen, präklinischen Stadium zu erfassen.
Test: Große Arterien versus Schaden an kleinen Gefäßen
Um zu prüfen, ob die Gestalt großer Hirnarterien für dieses Reinigungssystem eine Rolle spielt, untersuchte das Team den Circulus arteriosus Willisi – einen ringförmigen Zusammenfluss großer Arterien an der Hirnbasis. Mit einem mathematischen Maß, der Fraktaldimension, quantifizierten sie, wie verzweigt und raumausfüllend dieses arterielle Netzwerk ist, als Proxy dafür, wie gut es Blut und Pulsationen verteilen könnte, die den Flüssigkeitsfluss antreiben. Gleichzeitig verwendeten sie eine Diffusions‑MRT‑Methode (den DTI‑ALPS‑Index), die erfasst, wie leicht Wasser entlang perivaskulärer Bahnen wandert und damit eine indirekte Messung glymphatischer Aktivität liefert. Schließlich beurteilten sie die ePVS‑Last jeder Person in strukturellen MRTs und maßen gängige kognitive Fähigkeiten, darunter Arbeitsgedächtnis und Verarbeitungsgeschwindigkeit.
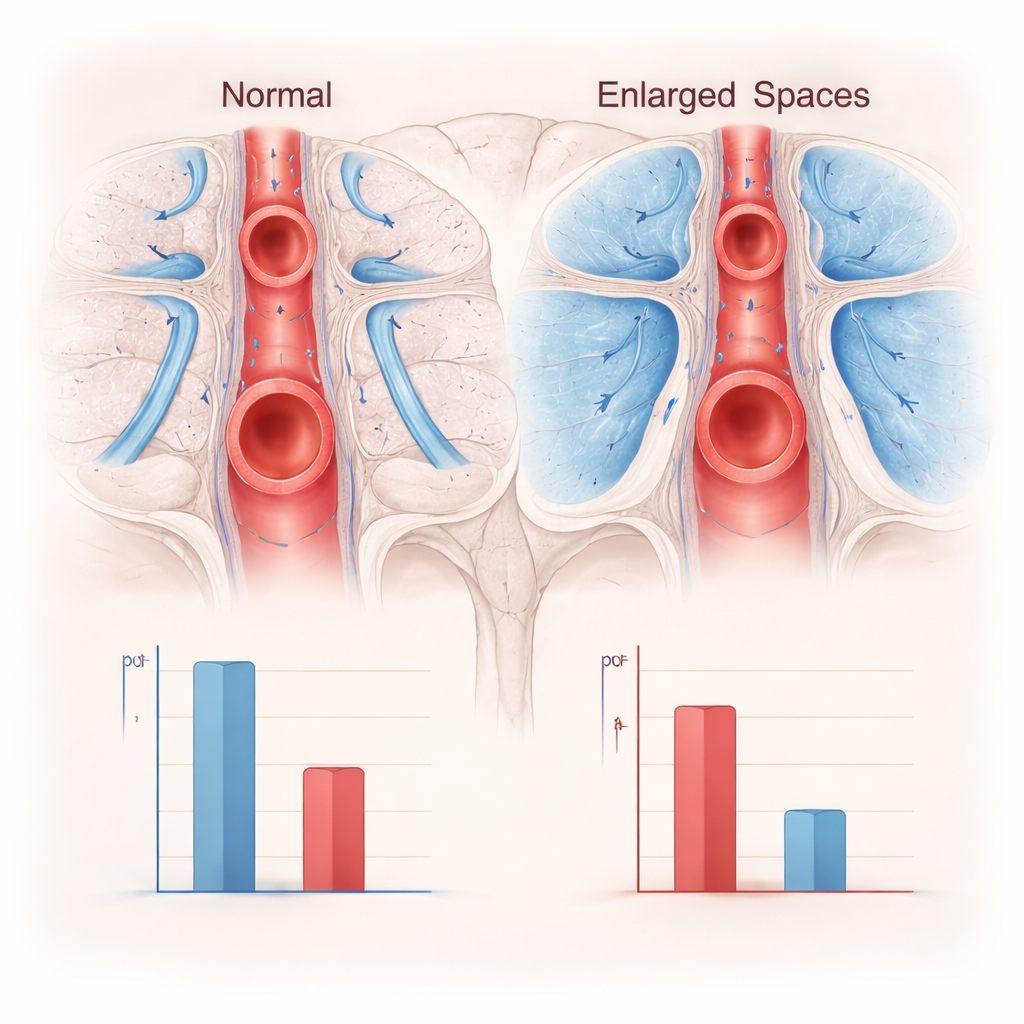
Was die Gehirnscans zeigten
Unter 60 Erwachsenen zeigten etwa 4 von 10 bereits sichtbare ePVS, obwohl keiner eine diagnostizierte Hirnerkrankung hatte und die allgemeinen kardiovaskulären Risikowerte niedrig waren. Personen mit ePVS waren tendenziell etwas älter, häufiger auf Blutdruckmedikation und hatten höhere langfristige vaskuläre Risikoscores, was zur Vorstellung passt, dass diese winzigen Läsionen kumulativen Gefäßstress widerspiegeln. Entscheidend war, dass die ePVS‑Gruppe sowohl einfacherer aussehende Circuli Willisi als auch deutlich niedrigere DTI‑ALPS‑Werte aufwies, was auf verminderten Flüssigkeitsfluss entlang perivaskulärer Routen hinweist. Auf den ersten Blick hing die Komplexität der großen Arterien mit der Flüssigkeitsfluss‑Messung zusammen, und beide standen in Verbindung mit der ePVS‑Last.
Mikrogefäße rücken in den Vordergrund
Nachdem die Forschenden jedoch Alter, Geschlecht, Blutdruckbehandlung, das allgemeine vaskuläre Risiko und ePVS berücksichtigt hatten, verschwand der scheinbare Zusammenhang zwischen der Komplexität der großen Arterien und dem Flüssigkeitsfluss weitgehend. Statistische Modelle zeigten, dass der stärkste einzelne Prädiktor für reduzierte perivaskuläre Diffusivität das Vorhandensein von ePVS selbst war. Anders ausgedrückt: Wie geschädigt oder angeschwollen das Umfeld der Kleingefäße war, war weitaus entscheidender als wie kunstvoll der Hauptarterienring aussah. Eine detailliertere Mediationsanalyse bestätigte, dass Veränderungen im Circulus Willisi nicht erklären konnten, wie ePVS mit schlechterer Flüssigkeitsdynamik verknüpft sind. Die kognitiven Testergebnisse lagen insgesamt im Normbereich, mit nur subtilen, nicht signifikanten Tendenzen, wonach Personen mit besserem Arbeitsgedächtnis und schnellerer Verarbeitungsgeschwindigkeit zu effizienterer perivaskulärer Diffusion neigten.
Was das für den Schutz der Gehirngesundheit bedeutet
Für Nichtfachleute lautet die Botschaft: Frühe „Sanitär“-Probleme im Gehirn zeigen sich zuerst rund um die winzigsten Gefäße, nicht in der großartigen Architektur der Hauptarterien. Sichtbar vergrößerte perivaskuläre Räume in der MRT heben sich als praxisrelevanter, klinisch nützlicher Marker hervor, dass das Abfallentsorgungssystem des Gehirns unter Belastung steht, selbst bei Menschen, die sich wohlfühlen und in standardisierten Denktests normal abschneiden. Dagegen steuerte die feingliedrige Geometrie des Circulus Willisi zwar interessante Veränderungen bei Betroffenen mit Kleingefäßschäden bei, sie bestimmte diese Clearance‑Messung jedoch nicht unabhängig. Diese Befunde stützen eine Verschiebung hin zur Überwachung der Mikrovaskulatur als Weg, Kleingefäßerkrankungen und damit verbundenen kognitiven Abbau lange vor dem Auftreten von Symptomen zu erkennen und möglicherweise zu verhindern.
Zitation: Hein, Z.M., Che Mohd Nassir, C.M.N. Perivascular pathology, not macrovascular complexity, governs glymphatic-related dysfunction in preclinical cerebral small vessel disease. Sci Rep 16, 4528 (2026). https://doi.org/10.1038/s41598-026-36001-7
Schlüsselwörter: Gehirn‑Abfallentsorgung, Kleingefäßerkrankung, perivaskuläre Räume, glymphatisches System, Gehirn‑MRT