Clear Sky Science · de
Molekulare Crowding‑Effekte auf die Proteinstabilität im bakteriellen Proteom
Warum das beengte Dasein von Proteinen wichtig ist
In jeder lebenden Zelle erfüllen Proteine ihre Aufgaben in einem Raum, der so dicht mit anderen Molekülen gefüllt ist, dass nahezu die Hälfte des Volumens eingenommen werden kann. Dennoch untersuchen die meisten Laborstudien Proteine in verdünnten, fast leeren Lösungen. Dieses Papier stellt eine einfache, aber wichtige Frage: Wie verändert diese beengte Realität die Stabilität und das Verhalten von Proteinen, und was bedeutet das für das Verständnis des Lebens auf molekularer Ebene?
Ein Blick in eine dichte zelluläre Welt
Um dies zu untersuchen, arbeiteten die Forscher mit dem Bakterium Cupriavidus necator, einem Mikroorganismus von Interesse für grüne Technologien wie Kohlenstoffbindung und die Produktion von Biokunststoffen. Sie öffneten die Zellen schonend, sodass Hunderte verschiedener Proteine ihrer natürlichen Form nahe blieben. Anschließend fügten sie hohe Konzentrationen großer, wasserliebender Polymere hinzu — gängige „Crowding‑Agenten“ wie PEG, Dextran und Ficoll — die oft verwendet werden, um das dichte Zellinnere nachzuahmen.
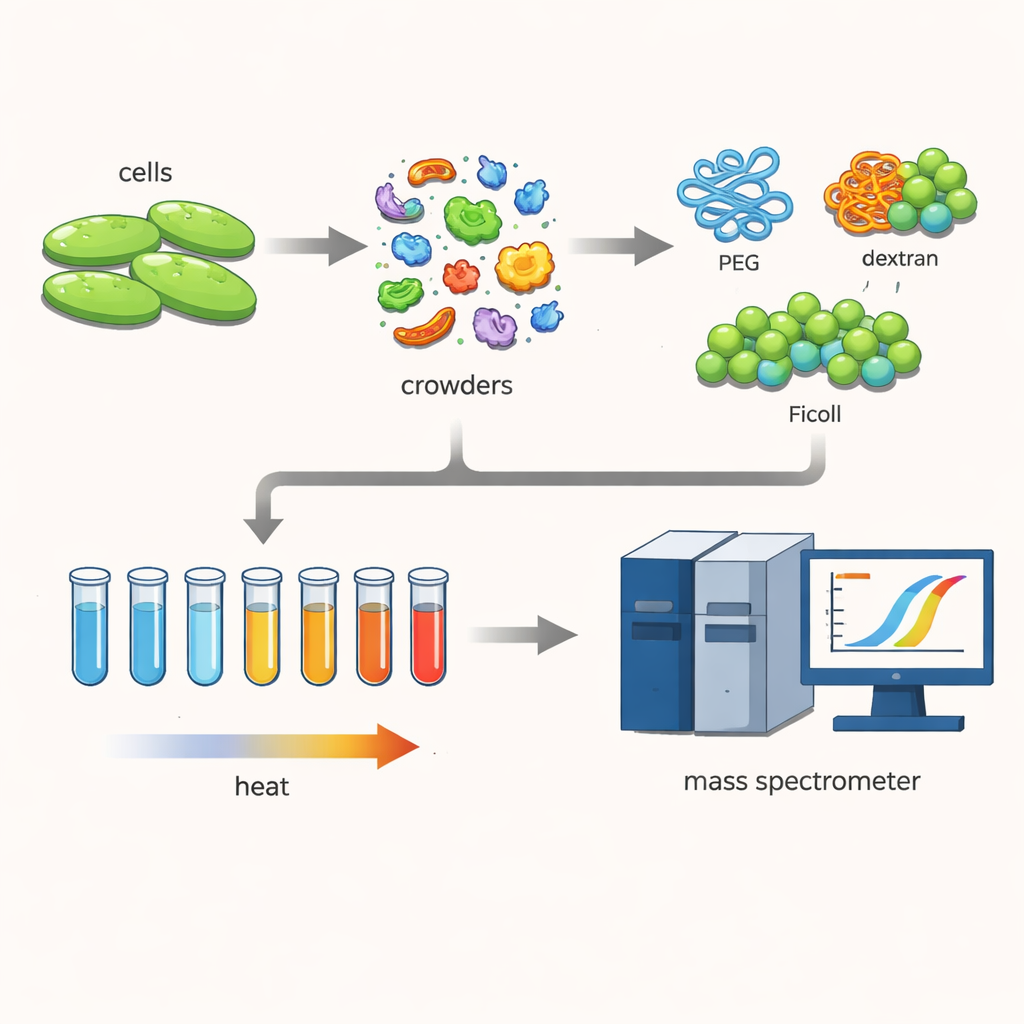
Proteine beim Schmelzen beobachten
Das Team verwendete eine Technik, die als thermales Proteom‑Profiling bekannt ist. Sie erhitzten viele kleine Proben des Proteinmischguts schrittweise von 30 bis 70 °C. Mit steigender Temperatur entfalteten sich weniger stabile Proteine und verklumpten, wodurch sie aus der Lösung fielen. Indem die verbleibenden löslichen Proteine markiert und mit einem empfindlichen Massenspektrometer gemessen wurden, konnten die Wissenschaftler Schmelzkurven für jedes Protein rekonstruieren und dessen Schmelztemperatur bestimmen — den Punkt, an dem die Hälfte des Proteins den löslichen, funktionellen Zustand verlassen hat. Der Vergleich dieser Temperaturen mit und ohne Crowding‑Agenten zeigte, wie die beengte Umgebung die Proteinstabilität verschob.
Ein gemischtes Bild: manche Proteine stabiler, andere labiler
Im Mittel senkte die Zugabe eines der sechs Polymer‑Crowder die Schmelztemperaturen im bakteriellen Proteom, was auf einen leicht insgesamt destabilisierenden Effekt hinweist. Doch dieser globale Trend verbarg eine weitaus nuanciertere Geschichte. Bei Dutzenden einzelner Proteine hoben die Crowding‑Agenten die Stabilität deutlich an oder senkten sie, manchmal um mehrere Grad. Die meisten Proteine reagierten nur auf einen der sechs Wirkstoffe, aber einige sprachen auf mehrere an — und fast alle davon wurden entweder konsistent stabilisiert oder konsistent destabilisiert, was auf gemeinsame zugrunde liegende Merkmale ihrer Wechselwirkung mit den Crowdern hindeutet.
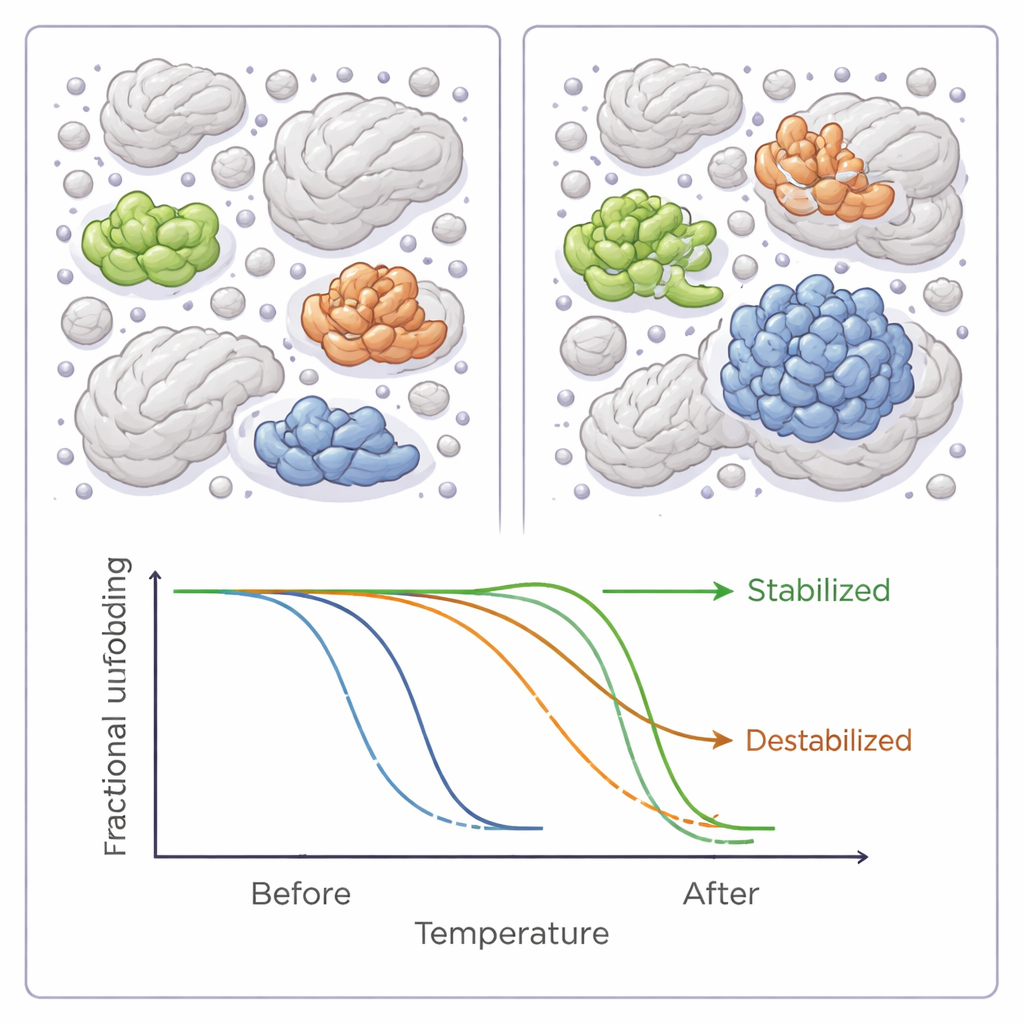
Was ein Protein in der Menge gewinnen oder verlieren lässt
Beim genaueren Blick auf die Eigenschaften dieser empfindlichen Proteine zeichnete sich ein Muster ab. Proteine, die unter Crowding stabiler wurden, waren tendenziell hydrophober — also mit mehr wasserabweisenden Oberflächen — und häufiger klassische Enzyme mit gut definierten aktiven Zentren. Sie waren auch eher an Protein‑Protein‑Interaktionen beteiligt oder trugen chemische Modifikationen, die ihre Funktion feinjustieren. Im Gegensatz dazu waren destabilisierte Proteine im Durchschnitt kleiner und weniger mit solchen Modifikationen versehen. Diese Befunde stimmen mit Computermodellen und anderen Experimenten überein, die nahelegen, dass Crowding je nach Größe, Form und den üblichen Wechselwirkungen mit Partnern manche Proteine begünstigen und andere verwundbarer machen kann.
Jenseits einfachen Zusammendrängens: wie Crowder wirklich wirken
Traditionelle Erklärungen für molekulares Crowding fokussieren auf das „ausgeschlossene Volumen“, die Idee, dass große Moleküle einfach weniger Raum lassen und Proteine dazu drängen, gefaltet zu bleiben. Wäre das die ganze Erklärung, würde man erwarten, dass Crowding‑Agenten hauptsächlich stabilisieren und starke Zusammenhänge mit der Sperrigkeit oder Viskosität der Crowder zeigen. Stattdessen fanden die Autoren nur schwache Verknüpfungen zu Größe und Dickflüssigkeit der Polymere. Ihre Daten passen besser zu einem Bild der „präferentiellen Ausschließung“: Crowder und Proteine meiden einander chemisch, was indirekt bestimmte gefaltete Zustände begünstigt, zugleich aber auch empfindliche Wechselwirkungen stören kann, die andere Proteine stabil halten. Kurz: Es ist nicht nur physisches Zusammendrängen, sondern ein feines chemisches Ziehen und Drücken, das das Proteindruckverhalten formt.
Was das für das Verständnis der Chemie des Lebens bedeutet
Für Nicht‑Spezialisten lautet die Kernbotschaft: Proteine in Zellen lassen sich nicht vollständig verstehen, wenn man sie isoliert in klarem Puffer betrachtet. Der dichte molekulare Dschungel um sie herum kann einige Proteine robuster und andere fragiler machen und so das Verhalten ganzer Reaktionsnetzwerke verändern. Diese Studie zeigt durch die Messung von Stabilitätsänderungen für Hunderte von Proteinen gleichzeitig, dass Crowding‑Effekte komplex und proteinspezifisch sind und wohl ebenso sehr von direkten Wechselwirkungen wie von einfachem Packen getrieben werden. Wenn Forscher Medikamente, industrielle Enzyme oder gentechnisch veränderte Mikroben entwickeln, wird die Anerkennung dieser beengten Realität entscheidend sein, um vorherzusagen, wie Proteine in lebenden Systemen tatsächlich funktionieren.
Zitation: McKeever, K., Dillon, E.T., Wynne, K. et al. Molecular crowding effects on protein stability in a bacterial proteome. Sci Rep 16, 5908 (2026). https://doi.org/10.1038/s41598-026-35990-9
Schlüsselwörter: molekulares Crowding, Protein‑Stabilität, thermales Proteom‑Profiling, bakterielles Proteom, zelluläre Umgebung