Clear Sky Science · de
Identifizierung diagnostischer und prognostischer Biomarker beim Lungenadenokarzinom durch integrierte bioinformatische Analyse und Validierung mittels Echtzeit‑PCR
Warum frühes Erkennen von Lungenkrebs wichtig ist
Lungenkrebs gehört zu den tödlichsten Krebsarten, vor allem weil er häufig zu spät entdeckt wird. Die häufigste Form, das Lungenadenokarzinom, kann jahrelang still wachsen, bevor Symptome auftreten. Diese Studie untersucht, ob Muster in Blut und Tumorgewebe die Krankheit deutlich früher aufzeigen können. Durch die Kombination großer genetischer Datensätze mit künstlicher Intelligenz und anschließender Überprüfung der Ergebnisse an realen Patienten wollen die Forscher einfache Blutmarker finden, die Ärzten eines Tages helfen könnten, Lungenkrebs früher zu erkennen und die Behandlung zu steuern.
Auf der Suche nach Warnsignalen in Genen
Das Team begann mit RNA‑Sequenzierungsdaten von 522 Personen, darunter 506 mit Lungenadenokarzinom und 16 gesunde Kontrollen. RNA ist die «Arbeitskopie» unserer Gene und spiegelt wider, welche Gene in Zellen ein‑ oder ausgeschaltet sind. Nach sorgfältiger Bereinigung und Normalisierung der Daten verglichen sie die Genaktivitätsniveaus zwischen Krebs‑ und Nicht‑Krebsproben. Dabei wurden 3.513 Gene gefunden, deren Aktivität bei Patienten signifikant unterschiedlich war. Diese Gene, sogenannte differentielle Expressionsgene, bildeten das Rohmaterial für ein Computermodell, das lernen konnte, Krebs von gesundem Gewebe anhand von Genmustern zu unterscheiden.

Computern beibringen, Krebs zu erkennen
Um Tausende von Genen zu durchforsten, nutzten die Forschenden einen Deep‑Learning‑Ansatz, eine Form künstlicher Intelligenz, die von neuronalen Netzwerken des Gehirns inspiriert ist. Sie bauten ein neuronales Netz mit mehreren verborgenen Schichten, das Genaktivitätsdaten aufnahm und lernte, jede Probe als krebsartig oder gesund zu klassifizieren. Das Modell wurde mit dem größten Teil der Daten trainiert und anschließend an einem separaten, zuvor unbekannten Datensatz getestet. Die Leistung war beeindruckend: Das System identifizierte Fälle und Kontrollen mit etwa 98 % Genauigkeit, einer Fläche unter der Kurve von 1,0 (nahezu perfekte Punktzahl) und einer extrem niedrigen Fehlerquote bei seinen Wahrscheinlichkeitsaussagen. Aus diesem Modell extrahierten sie 20 Gene, die am stärksten zu den Entscheidungen beitrugen und eine kurze Liste vielversprechender Kandidaten für weitere Untersuchungen hervorhoben.
Von Computerprognosen zu realen Bluttests
Muster in großen Datenbanken zu finden ist nur nützlich, wenn diese Muster auch bei echten Menschen auftreten. Um dies zu prüfen, sammelten die Forschenden Blut von 30 Lungenadenokarzinom‑Patienten (alle in frühem bis mittlerem Stadium und ohne vorausgegangene Behandlung) und 30 alters‑ und geschlechtsangepassten gesunden Freiwilligen. Mit einer Labormethode namens Echtzeit‑PCR maßen sie, wie stark mehrere vorhergesagte Markergene in Blut‑zellen exprimiert waren. Vier Gene fielen besonders auf. CYP2C9, KRT14 und PECAM1 waren im Blut der Patienten deutlich stärker aktiv als bei Gesunden, während A2M weniger aktiv war. Beispielsweise waren die CYP2C9‑Spiegel etwa viermal und KRT14 etwa achtmal höher bei Patienten, während A2M ungefähr halb so häufig vorkam. Diese klaren Unterschiede deuten darauf hin, dass ein kombinierter Bluttest für diese Marker helfen könnte zu erkennen, wer ein Lungenadenokarzinom hat.
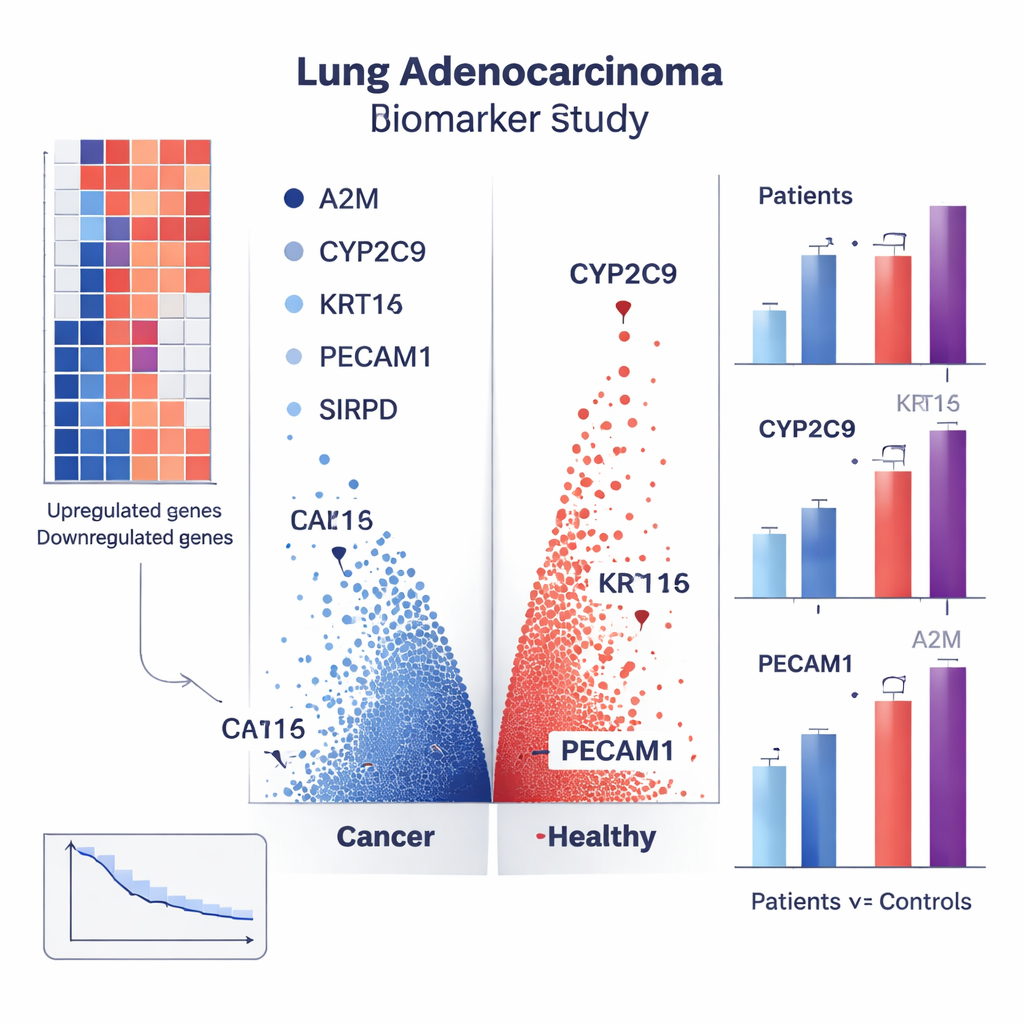
Hinweise auf Prognose und Krankheitsverhalten
Die Studie ging über eine einfache Ja‑/Nein‑Diagnose hinaus. Durch die Verknüpfung von Genaktivität mit klinischen Informationen wie Tumorgröße, Ausbreitung, Stadium und Überleben identifizierte das Team Gene, die vorhersagen könnten, wie sich ein Krebs verhält. Mehrere Gene, darunter CYP2C9, KCNV1, KRT24, SIRPD, PECAM1 und ein nicht kodierendes Gen namens LOC730668, standen in Zusammenhang mit dem Verlauf der Patienten. Einige scheinen mit der Bildung von Blutgefäßen, die Tumore versorgen, verbunden zu sein, andere mit der Interaktion von Krebszellen mit dem Immunsystem oder mit Resistenz gegen Zelltod. Externe Prüfungen in mehreren unabhängigen Datensätzen zeigten, dass die meisten dieser Kandidatenmarker konsistent reagierten, was das Vertrauen stärkt, dass die Ergebnisse keine Zufälligkeit eines einzelnen Datensatzes sind.
Was das für Patienten bedeuten könnte
Einfach gesagt zeigt diese Arbeit, dass eine intelligente Kombination aus fünf Genen — A2M, CYP2C9, KCNV1, KRT24 und SIRPD — Lungenadenokarzinome in genetischen Daten mit hoher Sensitivität markieren kann und dass mindestens vier davon deutliche, messbare Veränderungen im Blut zeigen. Obwohl diese Marker noch nicht für das routinemäßige Screening bereit sind, liefern sie einen vielversprechenden Entwurf für künftige Bluttests, die Lungenkrebs früher erkennen könnten, wenn er besser behandelbar ist. Sie könnten außerdem Ärzten helfen, die Aggressivität eines Tumors abzuschätzen und die Behandlung entsprechend anzupassen. Weitere Studien an größeren und vielfältigeren Patientengruppen sind nötig, doch die Ergebnisse deuten darauf hin, dass künstliche Intelligenz in Kombination mit sorgfältiger laborbasierter Validierung die Suche nach praktischen, minimalinvasiven Werkzeugen im Kampf gegen Lungenkrebs beschleunigen kann.
Zitation: Hossein Zadeh, R., Hossein Zadeh, R., Hajimoradi, M. et al. Identification of diagnostic and prognostic biomarkers in lung adenocarcinoma through integrated bioinformatics analysis and real time PCR validation. Sci Rep 16, 6679 (2026). https://doi.org/10.1038/s41598-026-35971-y
Schlüsselwörter: Lungenadenokarzinom, Biomarker, Deep Learning, Bluttest, früher Krebsnachweis