Clear Sky Science · de
Negr1-Mangel verändert Glutamatsignale und den Kynureninweg in einem Mausmodell psychiatrischer Erkrankungen
Warum diese Hirnstudie wichtig ist
Viele verbreitete psychische Erkrankungen, von Depression bis Schizophrenie, stehen im Zusammenhang mit feinen Veränderungen darin, wie Nervenzellen miteinander kommunizieren. Diese Studie untersucht ein Risikogen namens NEGR1 bei Mäusen, um zu sehen, wie dessen Verlust die Hirnchemie und das Verhalten verändert. Indem die Forscher verfolgen, wie sich diese Mäuse nach einem Wirkstoff bewegen, der kurzzeitig einen wichtigen Hirnrezeptor stört, und indem sie verwandte Hirnchemikalien messen, zeigen sie, wie Genetik, Geschlecht und Hirnstoffwechsel zusammenwirken können, um die Anfälligkeit für psychiatrische Erkrankungen zu formen.
Ein Gen, das Hirnsignale im Gleichgewicht hält
Das NEGR1-Gen codiert für ein Zelloberflächenprotein, das Nervenzellen hilft, Verbindungen zu bilden und zu stabilisieren. Frühere Arbeiten zeigten, dass das Entfernen dieses Gens bei Mäusen die Hirnstruktur verändert, bestimmte beruhigende (GABA) Verbindungen reduziert und die Reaktionen auf dopaminvermittelte Drogen wie Amphetamin verändert. Da diese Veränderungen auf eine Verschiebung zugunsten stärkerer exzitatorischer Signale hindeuten, konzentrierte sich das Team auf ein weiteres wichtiges exzitatorisches System: Glutamat und seine NMDA-Rezeptoren, die zentral für Lernen, Gedächtnis und adaptives Verhalten sind. Außerdem untersuchten sie den „Kynureninweg“, einen Stoffwechselweg, der die Aminosäure Tryptophan in Verbindungen abbaut, die NMDA-Rezeptoren entweder stärken oder blockieren können.
Verhaltensprüfungen mit einem bewusstseinsverändernden Wirkstoff
Um die Funktion der NMDA-Rezeptoren zu testen, setzten die Forscher MK-801 ein, ein bekanntes Mittel, das diese Rezeptoren kurzzeitig blockiert und Aspekte der Glutamatstörung nachbilden kann, die bei psychiatrischen Erkrankungen beobachtet wird. Männliche und weibliche Mäuse trugen entweder das normale Negr1-Gen oder fehlten komplett dieses Gen. Die Tiere erhielten täglich Injektionen von MK-801 und wurden in einem offenen Feld getestet, wo ihre Gesamtlaufaktivität, die Zeit in den Ecken und drehungsähnliche Rotationsbewegungen automatisch aufgezeichnet wurden. Bei drogen-naiven Männchen führte eine einzige Dosis MK-801 zu einem stärkeren Aktivitätsschub bei Negr1-defizienten Mäusen als bei normalen Tieren, was darauf hindeutet, dass ihre Gehirne ungewöhnlich empfindlich auf die Störung der Glutamatsignalisierung reagieren.
Ein überraschendes Muster schneller Toleranz
Bei wiederholter Verabreichung von MK-801 änderte sich das Muster. Bei Männchen stieg die Aktivität an manchen Tagen stark an, fiel jedoch an jedem zweiten Tag ab, wodurch ein Zickzack-Muster entstand, das auf eine schnelle, teilweise Toleranz gegenüber den Effekten des Wirkstoffs hindeutete. Über neun Tage zeigten normale Männchen eine zunehmende Reaktion, die mit Sensibilisierung vereinbar ist, während Negr1-defiziente Männchen einen abgeschwächten Aufbau der Aktivität und mildere tägliche Schwankungen zeigten, was auf veränderte NMDA-Rezeptor-Empfindlichkeit hinweist. Weibliche Tiere beider Genotypen passten sich noch schneller an: Etwa ab Tag fünf erzeugte MK-801 keine starken Verhaltenswirkungen mehr, sodass die Behandlung abgebrochen wurde. Insgesamt hatte das Geschlecht einen großen Einfluss, und klare Genotyp-Effekte traten vor allem bei Männchen auf.
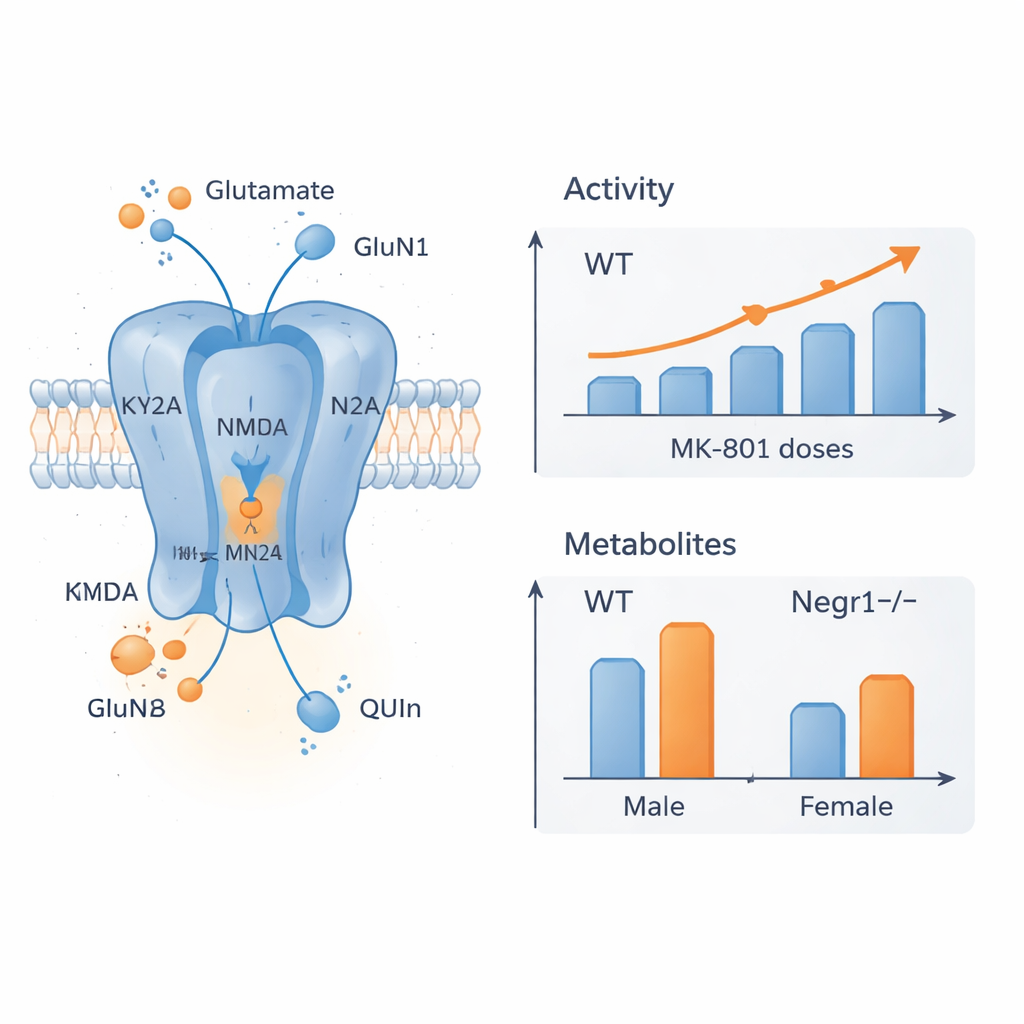
Verschiebungen bei Rezeptoren und Hirnchemikalien
Um die Ursachen dieser Verhaltensunterschiede zu ergründen, maßen die Forschenden die Genaktivität für wichtige NMDA-Rezeptor-Untereinheiten und für ein Enzym, das D‑Serin produziert, einen Kofaktor für diese Rezeptoren. Sie konzentrierten sich auf Hirnregionen, die für Stimmung und Kognition entscheidend sind: den Frontalkortex und den Hippocampus. Im Frontalkortex zeigten weibliche Negr1-defiziente Mäuse, die mit MK-801 behandelt wurden, eine reduzierte Expression zentraler Rezeptor-Untereinheiten, was darauf hindeutet, dass ihre Gehirne die Rezeptorzusammensetzung als Reaktion auf sowohl die Mutation als auch das Medikament anpassen. Im Hippocampus der Männchen hatten Negr1-defiziente Mäuse eine höhere Basalausprägung bestimmter NMDA-Untereinheiten, im Einklang mit früheren Hinweisen auf mehr verfügbare Rezeptoren; die MK-801-Behandlung brachte diese Werte dann wieder in Richtung Normalniveau. Parallel dazu zeigten detaillierte chemische Analysen von Blut und mehreren Hirnregionen, dass mehrere Metaboliten des Kynureninwegs und Glutamat selbst in geschlechts- und regionsspezifischer Weise verändert waren, wobei der Frontalkortex am stärksten betroffen war und einige Veränderungen mit dem Alter deutlicher wurden.
Was das für das Verständnis psychischer Erkrankungen bedeutet
Zusammen zeichnen diese Befunde NEGR1 als einen molekularen Organisator, der dazu beiträgt, exzitatorische und inhibitorische Signale im Gehirn im Gleichgewicht zu halten, teilweise indem er die Funktion von NMDA-Rezeptoren und den Tryptophanstoffwechsel beeinflusst. Wenn Negr1 fehlt, reagieren Mäuse anders auf die Blockade von NMDA-Rezeptoren, zeigen geschlechtsabhängige Verschiebungen in Hirnchemikalien und entwickeln allmählich auf ungewöhnliche Weise Toleranz. Für Nichtfachleute ist die zentrale Botschaft: Ein einzelnes Risikogen wirkt nicht isoliert – seine Effekte hängen von Geschlecht, Hirnregion und Stoffwechsellage ab. Diese Arbeit stützt die Idee, dass die gezielte Behandlung von Pfaden, die mit NEGR1 verknüpft sind – statt nur einzelner Rezeptoren – langfristig helfen könnte, Therapien für psychische Erkrankungen mit Glutamatungleichgewicht zu präzisieren.
Zitation: Kuuskmäe, C., Mikheim, K., Mohammadrahimi, N. et al. Negr1 deficiency alters glutamate signalling and kynurenine pathway in a mouse model of psychiatric disorders. Sci Rep 16, 5317 (2026). https://doi.org/10.1038/s41598-026-35968-7
Schlüsselwörter: NEGR1-Gen, NMDA-Rezeptor, Glutamatsignalisierung, Kynureninweg, psychische Erkrankungen