Clear Sky Science · de
Strukturanalyse der OCT4-Bindung an menschliche LIN28B-Nukleosomen
Wie Zellen auf verborgene genetische Anweisungen zugreifen
Jede Zelle in Ihrem Körper trägt dieselbe DNA, dennoch wird in einem bestimmten Zelltyp nur ein Bruchteil dieser genetischen Anweisungen genutzt. Viel von dieser Kontrolle entsteht dadurch, dass DNA eng um Proteine namens Histone gewickelt ist und so Strukturen bildet, die als Nukleosomen bezeichnet werden. Diese dichte Verpackung kann entscheidende DNA-Abschnitte vor der zellulären Maschinerie verbergen, die Gene abliest. Die hier beschriebene Studie untersucht, wie ein spezielles Protein, OCT4, sein Ziel-DNA findet und daran bindet, selbst wenn diese DNA in Nukleosomen eingewickelt und teilweise verdeckt ist — ein Prozess, der für die Identität von Stammzellen und die zelluläre Reprogrammierung zentral ist.
Warum Pionierfaktoren für Stammzellen wichtig sind
OCT4 gehört zu einer kleinen, aber mächtigen Gruppe von Proteinen, den sogenannten Pionier-Transkriptionsfaktoren. Im Gegensatz zu den meisten DNA-bindenden Proteinen können Pioniere in kompakte, „ausgeschaltete“ Bereiche des Genoms eindringen und dabei helfen, Gene zu aktivieren. Sie spielen eine entscheidende Rolle bei der Formung der Zellidentität und bei der Reprogrammierung ausgereifter Zellen zurück in einen stammzellähnlichen Zustand. OCT4 wirkt zusammen mit Partnern wie SOX2, KLF4 und c-MYC, um Pluripotenz zu induzieren — die Eigenschaft, die es Stammzellen erlaubt, nahezu jeder Zelltyp zu werden. Genau zu verstehen, wie OCT4 an in Nukleosomen verpackte DNA anbindet, ist unerlässlich, um zu entschlüsseln, wie Zellen ihr Schicksal wechseln, und um präzisere Methoden zur Manipulation der Zellidentität in Forschung und Medizin zu entwickeln.
Prüfung, ob Artenunterschiede eine Rolle spielen
Die meisten Strukturstudien an Nukleosomen verwenden Histonproteine entweder von Fröschen (Xenopus laevis) oder von Menschen, da diese Proteine sehr ähnlich, aber nicht identisch sind. Kleine Unterschiede in ihren Aminosäuresequenzen könnten theoretisch verändern, wie DNA gewickelt ist oder wie regulatorische Proteine wie OCT4 binden. In früheren Arbeiten zeigten die Autorinnen und Autoren, dass OCT4 an eine spezifische regulatorische DNA-Sequenz des humanen LIN28B-Gens bindet, wenn diese DNA in Nukleosomen eingebettet ist, die mit Frosch-Histonkomplexen hergestellt wurden. In der neuen Studie stellten sie eine einfache, aber wichtige Frage: Verhält sich OCT4 genauso, wenn die Nukleosomen aus menschlichen Histonen statt aus Frosch-Histonen aufgebaut sind?
Aufbau und Untersuchung von LIN28B-Nukleosomen
Um dies zu beantworten, rekonstituierten die Forschenden Nukleosomen im Labor mit einem 182 Basenpaare langen Abschnitt der LIN28B-DNA und entweder menschlichen oder Frosch-Histonproteinen, zusammengesetzt durch eine sorgfältige „Slow-Dialyse“-Methode, die die Bedingungen in Zellen nachahmt. Gelbasierte Tests bestätigten, dass beide Arten von Histonoktameren Nukleosomen effizient bildeten. Anschließend untersuchten sie, wie diese Nukleosomen auf der LIN28B-DNA positioniert sind. Sowohl Gel-Experimente als auch DNA-Schnitt gefolgt von Sequenzierung (MNase-seq) zeigten, dass die LIN28B-DNA mehrere Positionen auf dem Histon-Kern einnehmen kann, und dieses Verhalten änderte sich nicht, wenn die Nukleosomen auf Körpertemperatur erwärmt wurden. Entscheidend war, dass es keinen erkennbaren Unterschied machte, ob die Histone von Fröschen oder Menschen stammten, weder hinsichtlich der DNA-Positionierung noch der Bindungsstärke von OCT4.
Visualisierung von OCT4 auf dem Nukleosom
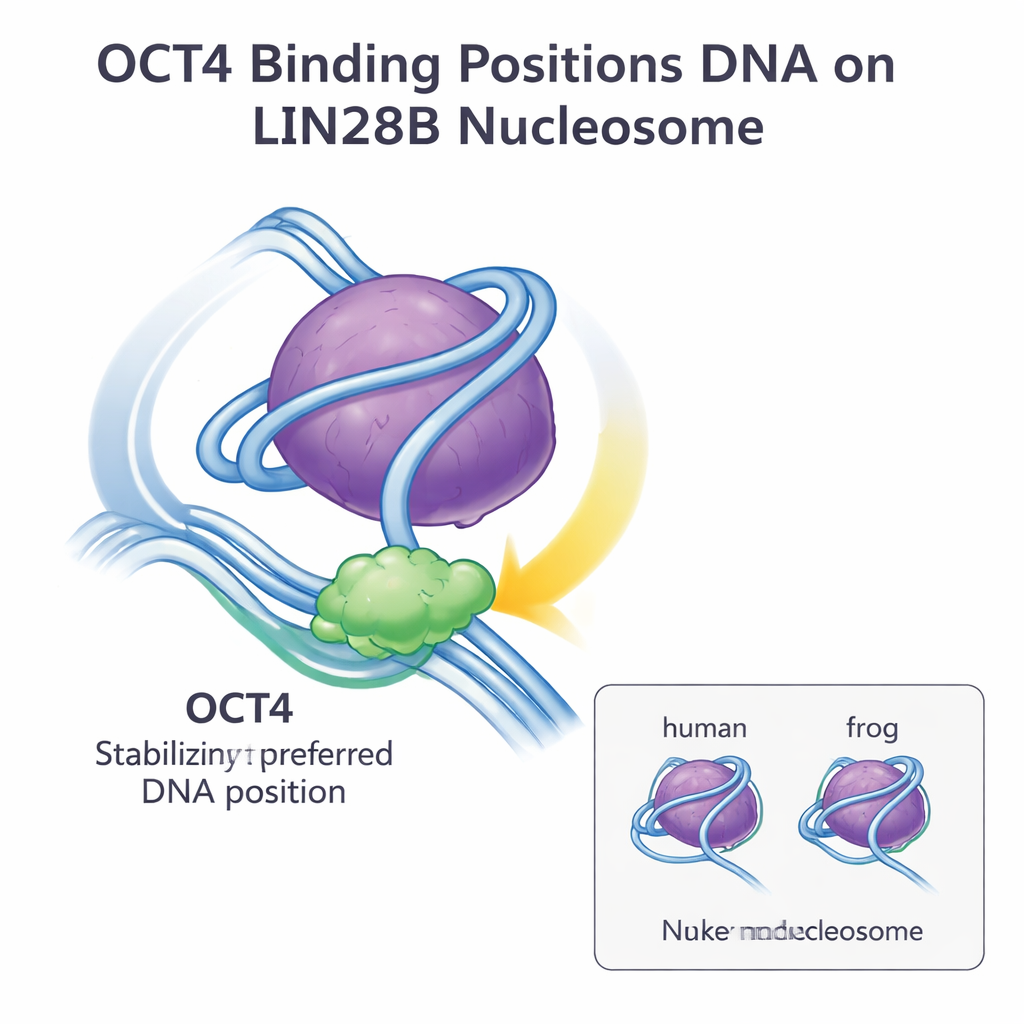
Als Nächstes nutzte das Team kryogene Elektronenmikroskopie (cryo-EM), um die Struktur von OCT4 gebunden an LIN28B-Nukleosomen mit menschlichen Histonen zu visualisieren. Aus etwa 15.000 Partikeln rekonstruierten sie eine dreidimensionale Karte mit ungefähr 6-Ångström-Auflösung. Die Bilder zeigten, dass beide DNA-bindenden Domänen von OCT4 mit demselben exponierten DNA-Abschnitt in der Nähe des Ein- und Austrittspunkts des Nukleosoms Kontakt aufnehmen, der sogenannten Linkerregion. Dies ist genau die Stelle und Orientierung, die zuvor gesehen wurde, als OCT4 an Nukleosomen mit Frosch-Histonen gebunden war. Als das ältere Modell in die neue cryo-EM-Karte eingefügt wurde, stimmte es hervorragend überein, was darauf hinweist, dass die Gesamtarchitektur des OCT4–LIN28B-Nukleosom-Komplexes für beide Arten im Wesentlichen identisch ist.
Eine allgemeine Strategie zum Öffnen von Chromatin
Zusammen zeigen diese Befunde, dass kleine Sequenzunterschiede zwischen Frosch- und Humanhistonen nicht verändern, wie OCT4 das LIN28B-Nukleosom erkennt und bindet. Die LIN28B-DNA liegt natürlicherweise in mehreren möglichen Positionen auf dem Histon-Kern, doch die OCT4-Bindung wählt eine bevorzugte Position aus und stabilisiert sie, wodurch weitere Bindungsstellen für OCT4 und seine Partner zugänglicher werden. Diese „DNA-Positionierungs- und Stabilisierung“-Strategie scheint ein allgemeiner Mechanismus zu sein, mit dem Pionierfaktoren Zugang zu geschlossenem Chromatin erhalten und die kooperative Bindung anderer Regulatoren fördern. Für ein allgemeines Publikum lautet die Quintessenz, dass das grundlegende Design des Nukleosoms und die Art und Weise, wie Schlüsselregulatoren wie OCT4 mit ihm zusammenarbeiten, über Arten hinweg stark konserviert sind — ein Befund, der die Aussage stützt, dass Erkenntnisse aus Modellorganismen zuverlässig unser Verständnis der menschlichen Genkontrolle und Stammzellbiologie informieren können.
Zitation: Sinha, K.K., Halic, M. Structural analysis of OCT4 binding to human LIN28B nucleosomes. Sci Rep 16, 5704 (2026). https://doi.org/10.1038/s41598-026-35959-8
Schlüsselwörter: Pionier-Transkriptionsfaktoren, OCT4, Nukleosomenstruktur, Chromatinzugänglichkeit, Regulation von Stammzellgenen