Clear Sky Science · de
APOBEC3B verbessert die Wirksamkeit von PARP-Inhibitoren bei der Eliminierung von Eierstockkrebs-Stammzellen
Warum diese Forschung für Patientinnen mit Eierstockkrebs wichtig ist
Viele Frauen mit fortgeschrittenem Eierstockkrebs sprechen anfangs gut auf moderne Medikamente an, die als PARP-Inhibitoren bezeichnet werden und Schwächen im DNA-Reparatursystem des Tumors ausnutzen. Mit der Zeit kehrt die Krankheit jedoch oft zurück, weil Krebszellen lernen, diesen Behandlungen zu entkommen. Diese Studie untersucht einen unerwarteten Verbündeten in den Krebszellen selbst — ein DNA-veränderndes Enzym namens APOBEC3B — und zeigt, dass es unter bestimmten Bedingungen die Eierstockkrebs-Stammzellen tatsächlich anfälliger für PARP-Inhibitoren machen kann.
Ein tödlicher Krebs, der immer wiederkehrt
Das hochgradig seröse Eierstockkarzinom ist die häufigste und tödlichste Form des Eierstockkrebses. Es wird meist spät diagnostiziert, wenn sich die Krankheit bereits im Abdomen ausgebreitet hat, und mehr als 80 % der Patientinnen mit fortgeschrittenem Befund erleiden innerhalb von fünf Jahren ein Wiederauftreten. Ein zentraler Verdächtiger für diese Rückfälle ist eine kleine Population von „Krebsstammzellen“. Diese Zellen können sich selbst erneuern, Chemotherapien überleben und Tumore nach der Behandlung wieder aufbauen. Zu verstehen, was diese stammzellähnlichen Zellen widerstandsfähig macht — und wie man sie gezielt angreift — ist entscheidend, um das Langzeitüberleben zu verbessern.
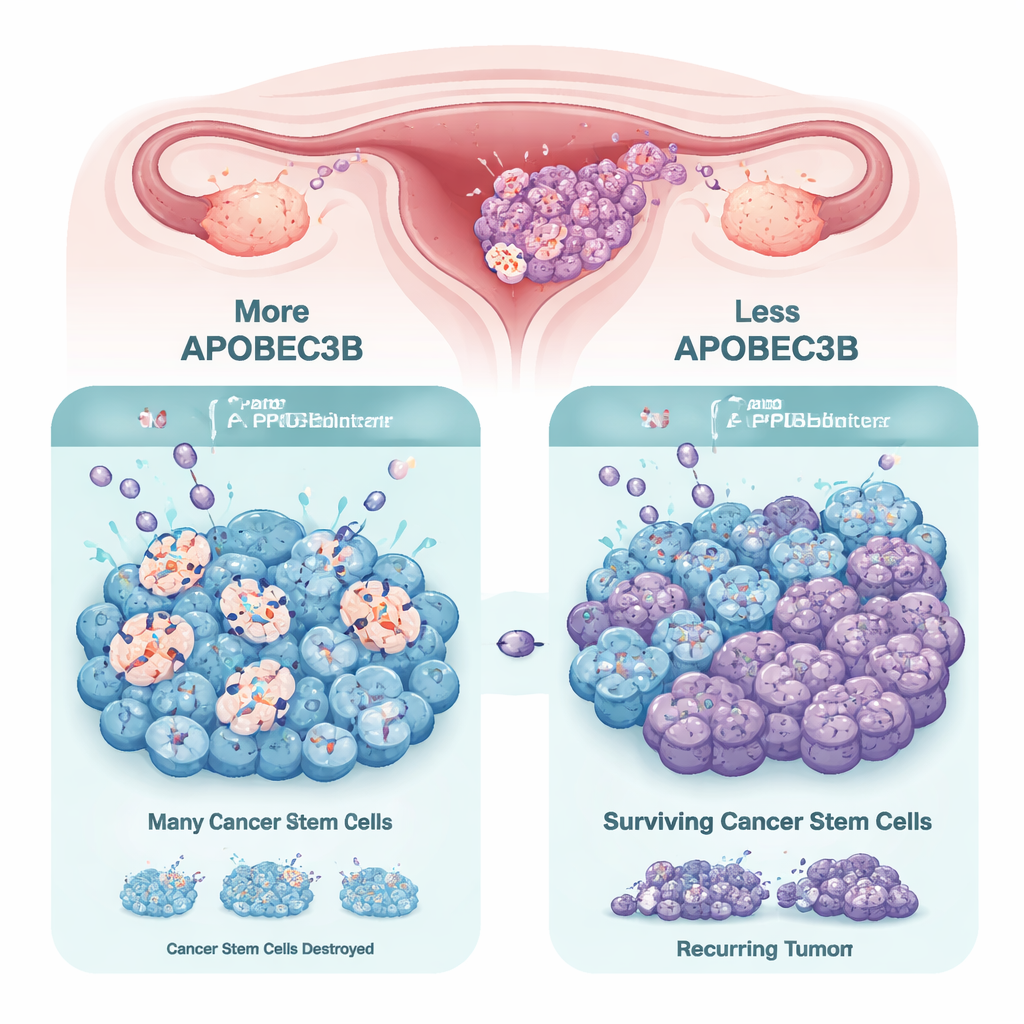
Ein mutierendes Enzym mit doppeltem Gesicht
Die APOBEC3-Enzymfamilie schützt unsere Zellen normalerweise vor Viren, indem sie bestimmte DNA-Basen verändert, was Mutationen erzeugen kann. In vielen Krebserkrankungen ist ein Familienmitglied, APOBEC3B, überaktiv und trägt zu DNA-Schäden und genetischem Chaos bei, was die Tumorentwicklung und Therapie‑Resistenz antreiben kann. In Eierstocktumoren und patientenabgeleiteten Modellen bestätigten die Forschenden, dass APOBEC3B in der Regel das am stärksten vertretene APOBEC3-Enzym ist. Beim Vergleich gewöhnlicher Tumorzellen mit stammzellähnlichen „Tumorsphären“, die dreidimensional gezüchtet wurden, stellten sie jedoch fest, dass die stammzellähnlichen Zellen APOBEC3B konsistent herunterregulieren. Das legt nahe, dass Krebsstammzellen ihre Mutationslast reduzieren könnten, um ihr Überleben und ihre Selbst erneuerungsfähigkeit zu bewahren.
Weniger APOBEC3B macht Stammzellen widerstandsfähiger
Um zu testen, ob APOBEC3B tatsächlich die Stammzell-Eigenschaften beeinflusst, nutzte das Team genetische Werkzeuge, um seine Expression in patientenabgeleiteten Eierstockkrebs‑Modellen und etablierten Zelllinien herunterzufahren. Bei verringerten APOBEC3B‑Werten bildeten die Krebszellen effizienter Tumorsphären und zeigten höhere Spiegel klassischer Stammzellmarker wie SOX2, OCT4 und NANOG. Der Anteil der Zellen mit stammzellähnlichen Eigenschaften stieg, was darauf hinweist, dass der Verlust von APOBEC3B den Krebszellen hilft, in einen widerstandsfähigeren, stammzellähnlichen Zustand zu wechseln. In Mäusen wuchsen Tumore ohne APOBEC3B nicht schneller von selbst, verhielten sich nach Behandlung mit PARP-Inhibitoren jedoch anders.
Mehr APOBEC3B, mehr Schäden — und bessere Arzneimittelwirkung
Die Forschenden untersuchten dann, wie APOBEC3B die Wirkung von PARP-Inhibitoren wie Olaparib beeinflusst, die die DNA‑Reparatur blockieren und Krebszellen durch tödliche DNA‑Schäden überfordern. In mehreren Eierstockkrebs‑Zelllinien machte die Reduktion von APOBEC3B die Zellen resistenter gegen PARP‑Inhibitoren, insbesondere in 3D‑Tumorsphären, die für stammzellähnliche Zellen angereichert waren. Umgekehrt sensibilisierte eine Erhöhung von APOBEC3B bestimmte Zellen für PARP‑Inhibitoren und verringerte deren Überleben deutlich. In Mausversuchen schrumpften oder verlangsamten Tumore mit normalem APOBEC3B‑Level unter Olaparib deutlich, während APOBEC3B‑defiziente Tumore trotz Behandlung weiterwuchsen. Molekulare Analysen erklärten das: Hohe APOBEC3B‑Spiegel verstärkten Replikationsstress und Doppelstrangbrüche und aktivierten DNA‑Schadens‑Signalwege. Wurde APOBEC3B herunterreguliert, nahmen PARP‑Inhibitor‑induzierte DNA‑Schäden, Checkpoint‑Aktivierung und Replikationsstress ab, und die Zellen blieben eher sicher im Zellzyklus stehen, anstatt abzusterben.
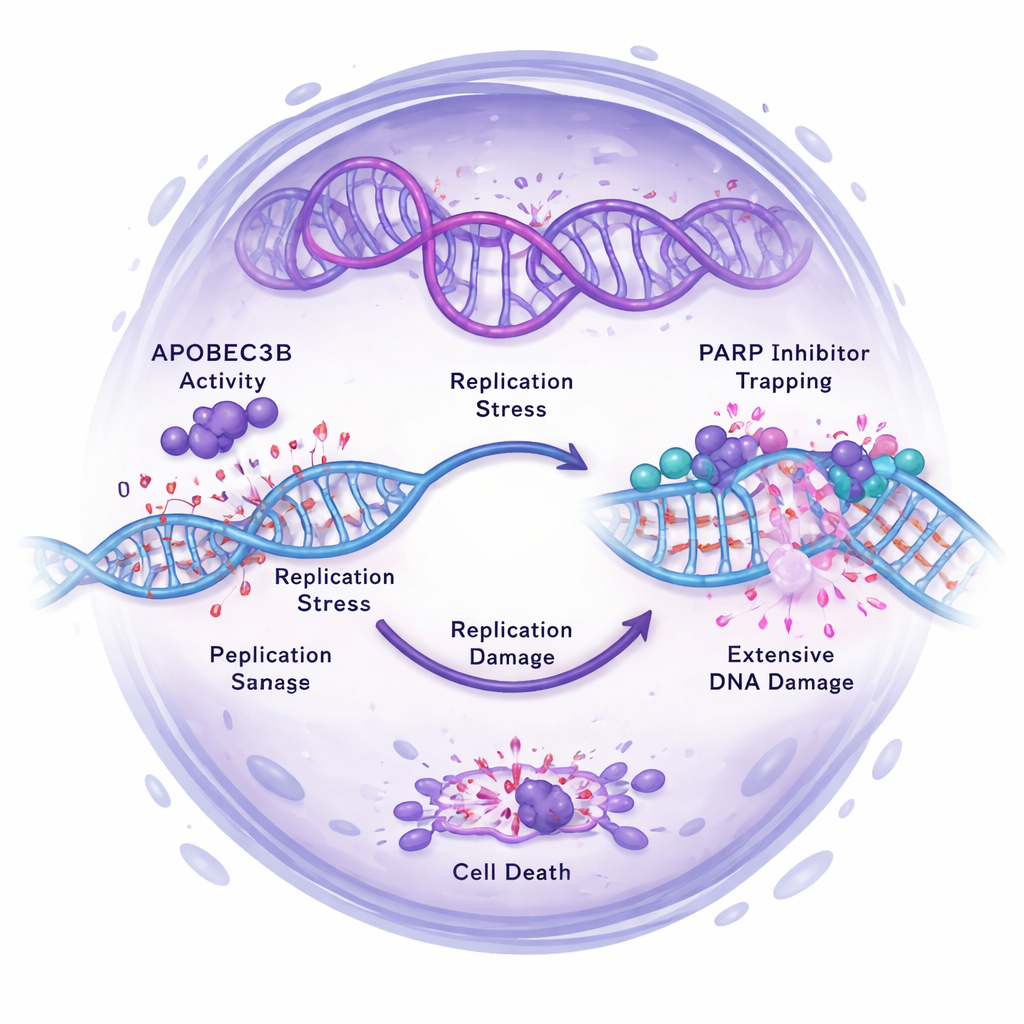
Eine neue Sicht auf Resistenz und Therapiedesign
Mithilfe von RNA‑Sequenzierung zeigte das Team, dass die Kombination aus Verlust von APOBEC3B und PARP‑Hemmung viele Gene umprogrammiert, die an DNA‑Replikation und ‑Reparatur beteiligt sind, und damit unterstützt, dass APOBEC3B die schädlichen Effekte von PARP‑Inhibitoren auf das Genom von Krebszellen verstärkt. Sie prüften auch, ob ein anderes Reparaturenzym, UNG, für diesen Effekt erforderlich ist, und fanden heraus, dass die Empfindlichkeit gegenüber PARP‑Inhibitoren in Zellen mit hohem APOBEC3B größtenteils unabhängig von UNG war. Insgesamt deuten die Daten darauf hin, dass APOBEC3B‑getriebener Replikationsstress — nicht nur seine mutagene Aktivität — der entscheidende Faktor ist, der PARP‑Inhibitoren dabei hilft, Eierstockkrebs‑Stammzellen zu töten.
Was das für Patientinnen und künftige Therapien bedeutet
Für Laien lautet die Botschaft: Nicht alles genetische Chaos in einem Tumor ist automatisch schlecht. In dieser Studie machten höhere Spiegel des mutierenden Enzyms APOBEC3B Eierstockkrebs‑Stammzellen tatsächlich verwundbarer für PARP‑Inhibitoren, indem sie deren DNA‑Reparaturkapazität überlasteten. Wurde APOBEC3B reduziert, wurden Krebsstammzellen stammzellähnlicher und widerstandsfähiger gegen Behandlung. Diese Erkenntnisse legen nahe, dass die Messung von APOBEC3B‑Spiegeln helfen könnte vorherzusagen, welche Patientinnen am meisten von PARP‑Inhibitoren profitieren, und dass das Timing oder die Kombination zukünftiger APOBEC3B‑gezielter Medikamente mit PARP‑Inhibitoren sorgsam erfolgen muss. Die Nutzung des „selbstsabotierenden“ Effekts von APOBEC3B auf Krebszellen könnte neue Strategien eröffnen, Rückfällen vorzubeugen und die Wurzeln von Eierstocktumoren effektiver zu beseitigen.
Zitation: Rivera, M., Liu, L., Enlund, S. et al. APOBEC3B enhances the efficacy of PARP inhibitors in elimination of ovarian cancer stem cell. Sci Rep 16, 5194 (2026). https://doi.org/10.1038/s41598-026-35939-y
Schlüsselwörter: Eierstockkrebs, PARP-Inhibitoren, Krebsstammzellen, APOBEC3B, Arzneimittelresistenz