Clear Sky Science · de
Maschinelles Lernframework zur Analyse alternativer mRNA-Spleißung identifiziert ein Progressions-Signatur beim kolorektalen Adenokarzinom
Warum diese Forschung für Patientinnen und Patienten wichtig ist
Kolorektales Karzinom gehört zu den häufigsten und tödlichsten Krebsarten, dennoch fällt es Ärzten oft schwer vorherzusagen, welche Tumoren ruhig bleiben und welche nach der Behandlung wieder aktiv werden. Diese Studie stellt eine neue Methode vor, um verborgene Signale in der Tumor‑RNA zu lesen – die Botschaften, mit denen Zellen Proteine herstellen – und nutzt maschinelles Lernen, um diese Signale in einen einfachen Risiko‑Score zu überführen, der helfen kann, die Intensität der Behandlung an den einzelnen Patienten anzupassen.

Versteckte Schnitte und Bearbeitungen in Krebsgenen
Unsere Gene werden nicht starr abgelesen. Wenn eine Zelle DNA in RNA überträgt, kann sie Stücke der RNA‑Botschaft in verschiedenen Kombinationen herausschneiden und zusammenfügen – ein Vorgang, der als alternative Spleißung bezeichnet wird. Diese Bearbeitung erlaubt es einem einzigen Gen, mehrere Proteinvarianten zu erzeugen, ähnlich wie verschiedene Werkzeuge aus demselben Werkzeugkasten. In gesunden Zellen ist diese Flexibilität streng reguliert. Bei Krebs dagegen kann das Schneiden und Kleben fehlgesteuert werden, wodurch Proteinvarianten entstehen, die Tumoren beim Wachstum, der Ausbreitung und der Therapie‑Resistenz unterstützen. Die Autoren vermuteten, dass das Muster dieser RNA‑Bearbeitungen im Tumor starke Hinweise darauf geben könnte, wie sich der Krebs im Verlauf verhalten wird.
RNA‑Muster in einen Risiko‑Score verwandeln
Die Forscher analysierten RNA‑Sequenzierungsdaten von Tumoren von 266 Patientinnen und Patienten mit kolorektalem Adenokarzinom aus dem Cancer Genome Atlas sowie von weiteren 348 Personen aus einer unabhängigen Studie. Für jeden Tumor maßen sie, wie oft bestimmte Spleißoptionen genutzt wurden, und fassten diese als Zahl zwischen null und eins zusammen. Anschließend bauten sie eine stufenweise Pipeline mit maschinellem Lernen auf, die zunächst Tausende von Spleißereignissen daraufhin durchsuchte, ob sie mit der Zeit bis zu einem Progressionsereignis zusammenhängen, und diese Liste dann systematisch verkleinerte, ohne redundante, überlappende Signale zu behalten. Das Ergebnis war eine kompakte „Signatur“ aus nur fünf spezifischen Spleißereignissen, deren kombiniertes Verhalten am besten mit einem früheren oder späteren Fortschreiten des Krebses korrelierte.
Einordnen von Patientengruppen in niedriges und hohes Risiko
Mithilfe dieser Fünf‑Ereignis‑Signatur definierten die Forschenden für jede Patientin bzw. jeden Patienten einen numerischen Risiko‑Score, indem sie die Spleißmessungen addierten, gewichtet nach der Stärke ihres Zusammenhangs mit Progression. Tumoren, die drei der Spleißmuster bevorzugten, waren tendenziell mit schlechterer Prognose verbunden, während zwei Muster mit besseren Ergebnissen assoziiert waren. Der Score teilte die Patientengruppe klar in Niedrig‑ und Hochrisiko: Sowohl in der ursprünglichen Kohorte als auch in der unabhängigen Validierungsgruppe traten bei denen mit hohen Scores Progressionen deutlich früher auf. In den Zeit‑bis‑Progression‑Kurven trennten sich die Linien deutlich, was zeigt, dass diese kleine Menge an RNA‑Bearbeitungen sinnvolle Unterschiede im Tumorverhalten über Hunderte von Individuen erfasst.
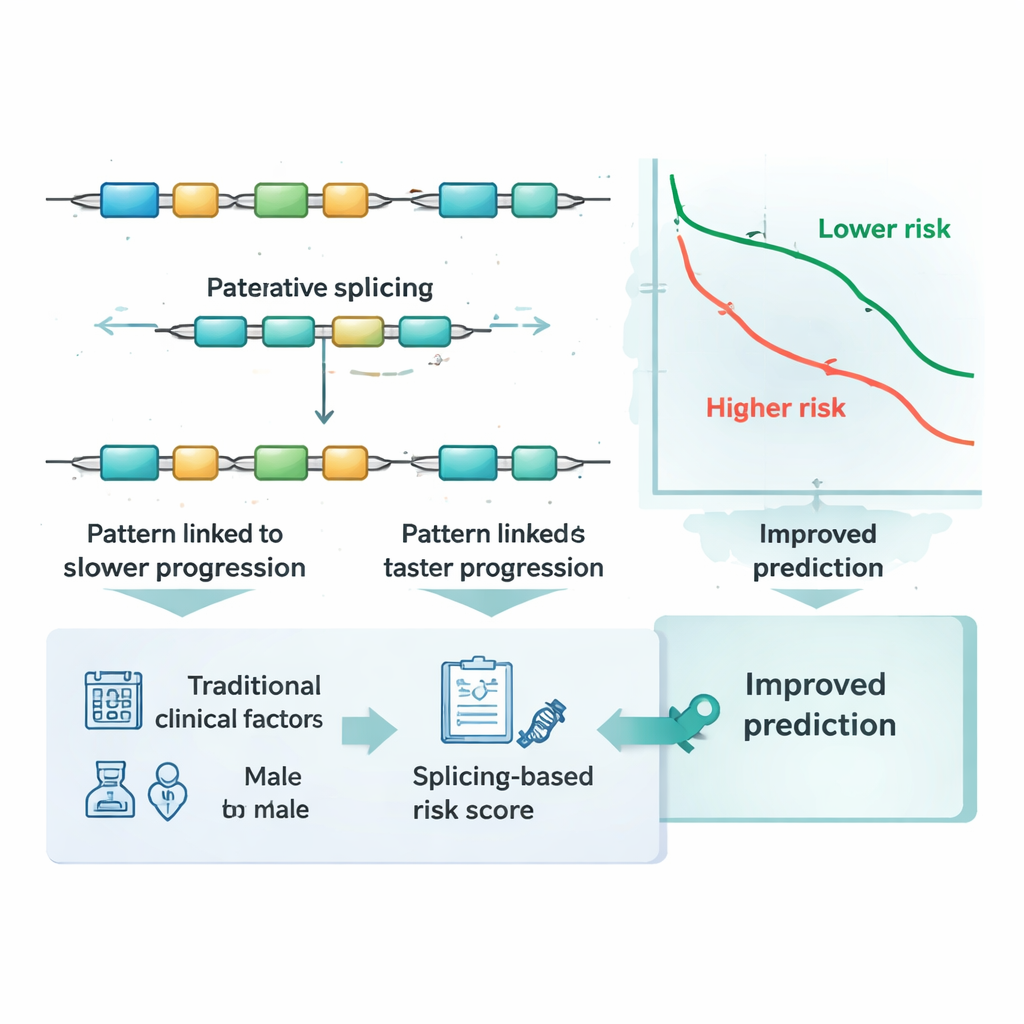
Über die Standard‑Stadieneinteilung und bekannte Marker hinaus
Ärzte stützen sich derzeit auf Tumorstadium, Alter und andere klinische Merkmale zur Risikoeinschätzung und gelegentlich auf bestimmte DNA‑Veränderungen oder Genexpressionsniveaus. Die Forschenden prüften, ob ihr Spleiß‑basierter Score einen Mehrwert gegenüber diesen etablierten Maßen bietet. Mit zeitabhängigen Genauigkeitstests zeigten sie, dass Vorhersagen, die nur auf Stadium, Alter und Geschlecht basierten, spürbar verbessert wurden, wenn der Spleiß‑Risiko‑Score hinzugefügt wurde. Sie verglichen den Score zudem mit Dutzenden bekannter molekularer Marker beim kolorektalen Krebs und mit mehreren gängigen statistischen Modellierungsansätzen. In beiden Patientengruppen entsprach die Fünf‑Ereignis‑Signatur diesen Alternativen oder übertraf sie und verbesserte die Prognose, wenn sie zusammen mit ihnen verwendet wurde, was darauf hindeutet, dass sie Informationen erfasst, die andere Marker nicht liefern.
Was das für die künftige Versorgung bedeuten könnte
Für Laien ist die zentrale Botschaft: Wie ein Tumor seine RNA „bearbeitet“, kann verraten, wie gefährlich er wahrscheinlich ist. Diese Studie zeigt, dass schon das Nachverfolgen von fünf spezifischen RNA‑Bearbeitungen in kolorektalen Tumoren Patientinnen und Patienten in Gruppen einteilen kann, die sich deutlich in der Wahrscheinlichkeit unterscheiden, progressionsfrei zu bleiben. Obwohl diese Arbeit noch in praktische Labortests übersetzt und in prospektiven klinischen Studien geprüft werden muss, deutet sie auf eine Zukunft hin, in der Ärztinnen und Ärzte einen solchen Score bei der Diagnose nutzen könnten, um zu entscheiden, wer eine intensivere Behandlung und engmaschigere Nachsorge benötigt und wer sicher einer Überbehandlung entgehen kann. Darüber hinaus bietet sie ein wiederverwendbares Framework, um Spleißmuster in anderen Krebsarten zu analysieren, die Prognose zu verfeinern und wirklich personalisierte Therapien zu steuern.
Zitation: Maimekov, U., Nosrati, M., Mahmoud, A. et al. Machine learning framework for mRNA alternative splicing analysis identifies a signature of progression in colorectal adenocarcinoma. Sci Rep 16, 7106 (2026). https://doi.org/10.1038/s41598-026-35903-w
Schlüsselwörter: kolorektales Karzinom, alternative Spleißung, RNA-Sequenzierung, maschinelles Lernen, Krebsprognose