Clear Sky Science · de
Supramolekulare Aggregation von Aquaporin-4 formt die kollektive Migration und Mechanik von Astrozyten
Wie Gehirnzellen gemeinsam wandern, um zu heilen
Wenn das Gehirn verletzt oder entzündet ist, eilen seine Stützzellen — die Astrozyten — herbei, um zu schützen, zu reparieren oder beschädigte Bereiche abzukapseln. Diese Studie untersucht einen überraschenden Faktor, der beeinflusst, wie gut diese Zellen gemeinsam vorankommen: winzige Wasserkanäle namens Aquaporin-4 (AQP4). Indem die Forschenden betrachten, wie AQP4-Moleküle in Astrozytenmembranen klumpen oder verteilt sind, zeigen sie, wie die "Wasserinstallation" des Gehirns die koordinierte kollektive Zellbewegung unterstützt und wie chronische Entzündung diesen Prozess entgleisen lassen kann.
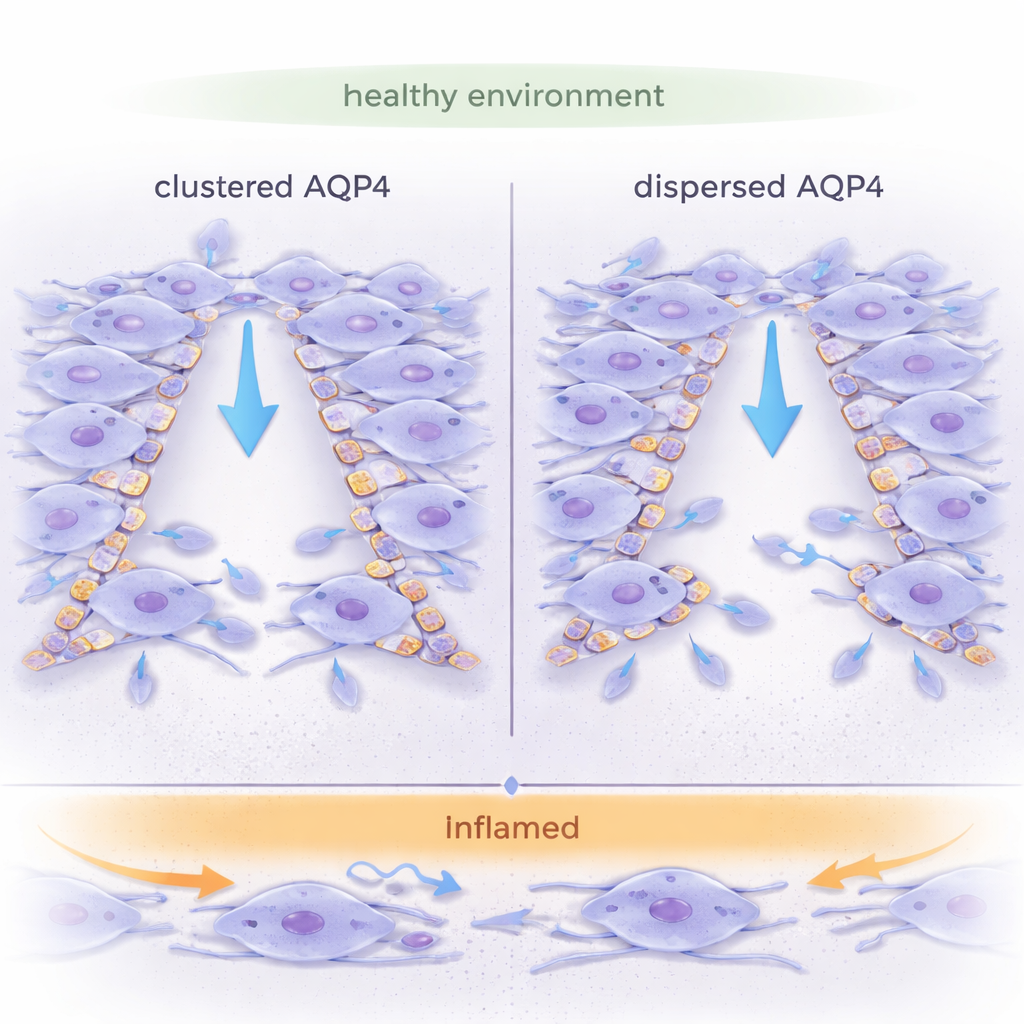
Wassertore an Gehirnzellen
Astrozyten sind sternförmige Zellen, die das Gleichgewicht im Gehirn erhalten, die Entwicklung lenken und auf Verletzungen reagieren. Sie sind reich an AQP4, einem Protein, das Poren bildet, durch die Wasser schnell ein- und austreten kann. Anders als viele andere Wasserkanäle kann sich AQP4 zu großen, kristallinen Plättchen zusammenlagern, den sogenannten orthogonalen Partikelarrays (OAPs), oder als kleinere, verstreute Einheiten (Tetramere) vorliegen. Man nimmt an, dass die Organisation von AQP4 beeinflusst, wie Zellen ihre Form ändern und sich bewegen, doch frühere Arbeiten konzentrierten sich meist auf einzelne Zellen. Diese Studie stellte eine realistischere Frage: Wie beeinflusst die AQP4-Organisation das Wanderverhalten ganzer Astrozytenlagen, wie sie beim Verschluss einer Wunde im Gehirngewebe auftreten würde?
Testen der Zellbewegung in Gesundheit und Entzündung
Die Forschenden züchteten zwei Typen von Maus-Astrozyten: normale Zellen, die AQP4-Arrays bilden können, und genetisch veränderte Zellen (OAP-null), denen die hauptsächliche Array-bildende AQP4-Variante fehlt und die daher überwiegend verstreute Tetramere aufweisen. Anschließend erzeugten sie einen "Kratz" in einer dichten Zellschicht, um eine Wunde zu simulieren, und beobachteten, wie schnell und gleichmäßig die Zellen die Lücke schlossen. Um ein chronisch geschädigtes Gehirn zu imitieren, behandelten sie einige Kulturen eine Woche lang mit den beiden Entzündungsmolekülen IL-1β und TNF-α vor den Tests. Mit Zeitrafferaufnahme und einer Computer-Vision-Methode namens Particle Image Velocimetry quantifizierten sie nicht nur, wie weit und wie schnell sich die Zellen bewegten, sondern auch, wie geradlinig, koordiniert oder verspannt ihre Bewegungen über die gesamte Schicht hinweg waren.
Verteilte Kanäle, gleichmäßigere Bewegung
Unter nichtentzündlichen Bedingungen waren Astrozyten mit verteilt vorliegendem AQP4 (OAP-null) deutlich besser in kollektiver Migration: Sie schlossen Wunden schneller und bewegten sich geradliniger als Zellen mit großen AQP4-Arrays. Ihre vordere Front war glatt und kontinuierlich, und benachbarte Zellen bewegten sich kohärent wie eine zusammenhängende "Schicht". Im Gegensatz dazu zeigten Astrozyten mit geklumpter AQP4 (Wildtyp) eine unregelmäßigere Vorderfront mit vielen einzelnen Vorwölbungen und inneren Verzerrungen, was darauf hindeutet, dass Zellen in leicht unterschiedlichen Richtungen zogen. Messungen der Dehnung innerhalb der Zellschicht bestätigten, dass OAP-null-Schichten weniger innere Zugkräfte und eine gleichmäßigere, koordiniertere Bewegung erfuhren.
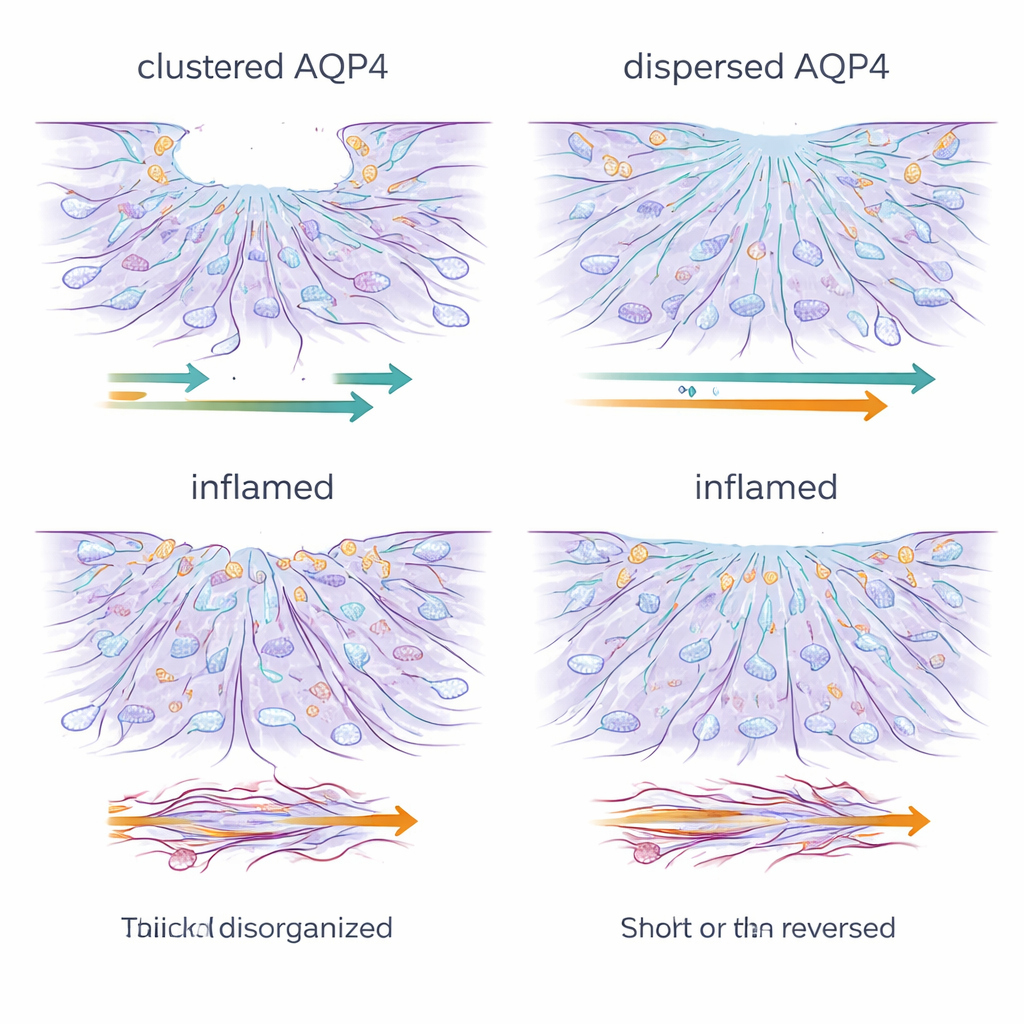
Entzündung bremst und verwirrt das Reparaturteam
Chronische Exposition gegenüber Entzündungssignalen veränderte dieses Bild grundlegend. Unabhängig von der AQP4-Organisation wurden behandelte Astrozyten zu schlechten Wundheilern: Sie bewegten sich kaum und drifteten in einigen Fällen sogar rückwärts, wodurch die Lücke größer wurde. Die Mikroskopie zeigte, dass die feinen, dynamischen Zellrandstrukturen für Vorwärtsbewegung — Lamellipodien und Filopodien — verloren gingen und durch dicke, starre Stressfasern aus Aktin, dem wichtigsten Strukturprotein der Zelle, ersetzt wurden. Gleichzeitig fielen die Spiegel von AQP4 und Connexin-43, einem Schlüsselprotein für Kommunikationskanäle zwischen Astrozyten, stark ab. Das Netzwerk der Gap-Junctions, das normalerweise hilft, Astrozyten als koordiniertes Ganzes agieren zu lassen, wurde gestört, und Farbstoff-Transfer-Experimente bestätigten, dass die Fernkommunikation zwischen Zellen deutlich geschwächt war.
Warum das für die Gehirngesundheit wichtig ist
Diese Ergebnisse legen nahe, dass nicht nur die Menge an AQP4 in einer Zelle wichtig ist, sondern auch dessen Anordnung, um Astrozyten eine effiziente Gruppenbewegung zu ermöglichen. Verteiltes AQP4 scheint den inneren Widerstand zwischen Zellen zu verringern und geradlinigere, besser koordinierte Bewegungen zu fördern, während große Cluster mit einem unruhigeren, verspannten Bewegungsmuster einhergehen. Chronische Entzündung überlagert diese Vorteile weitgehend, indem sie das Zellskelett umgestaltet, Wasser- und Kommunikationskanäle stilllegt und ein organisiertes Reparaturteam in eine starre, schlecht vernetzte Schicht verwandelt. Für Nichtfachleute lautet die Quintessenz: Die Wasserkanäle des Gehirns und die Systeme der Zell–Zell-Kommunikation leisten weit mehr als bloße Unterstützung der Neuronen — sie gestalten aktiv, wie Stützzellen nach einer Verletzung mobilisiert werden. Das Verständnis und die gezielte Beeinflussung der AQP4-Organisation und entzündlicher Signale könnten neue Wege eröffnen, um die Hirnreparatur zu verbessern, Vernarbung zu begrenzen oder sogar die Ausbreitung von Hirntumoren zu beeinflussen.
Zitation: Barile, B., Mennona, N.J., Mola, M.G. et al. Supramolecular aggregation of aquaporin-4 shapes astrocyte collective migration and mechanics. Sci Rep 16, 6021 (2026). https://doi.org/10.1038/s41598-026-35900-z
Schlüsselwörter: Astrozyten, Aquaporin-4, Gehirnentzündung, Zellmigration, gliale Narbe