Clear Sky Science · de
Isolation, Charakterisierung und potenzielle Anwendungen eines neuartigen Bakteriophagen, der beta‑Laktam‑resistenten Staphylococcus saprophyticus angreift
Warum winzige Viren bei hartnäckigen Infektionen helfen könnten
Harnwegsinfektionen gehören weltweit zu den häufigsten bakteriellen Erkrankungen, und viele davon werden inzwischen von Erregern verursacht, die gegenüber Standardantibiotika unempfindlich sind. Ein solcher Übeltäter, Staphylococcus saprophyticus, lebt harmlos auf unserer Haut und im Genitalbereich, kann aber in die Harnwege gelangen und besonders bei Frauen schmerzhafte, wiederkehrende Infektionen auslösen. Diese Studie untersucht einen ungewöhnlichen Verbündeten gegen dieses Mikroorganismus: ein neu entdecktes Virus, das Bakterien infiziert, ein sogenannter Bakteriophage, der beta‑laktamresistente S. saprophyticus abtöten und seine schützenden Schleimschichten sowie geruchsverursachende Kolonien auf Haut und Textilien entfernen kann.
Ein versteckter Störenfried im Alltag
Staphylococcus saprophyticus ist ein normaler Bewohner des menschlichen Körpers und besiedelt Darm, Harnröhre, Gebärmutterhals und Haut. Zugleich ist er die zweithäufigste Ursache von Harnwegsinfektionen bei Frauen und kann auch ältere Männer betreffen. Er bildet klebrige Biofilme—dichte bakterielle Gemeinschaften, die an Oberflächen haften—was Antibiotika die Wirkung erschwert und dem Keim hilft, an Blasen‑ und Harnröhrenzellen zu haften. Viele Stämme sind inzwischen gegen mehrere wichtige beta‑Laktam‑Antibiotika resistent, einschließlich solcher, die zum Schutz vor bakteriellen Penicillin‑spaltenden Enzymen entwickelt wurden. Über HWI hinaus wurde dieser Organismus mit Lebensmittelerkrankungen, Haut‑ und Augeninfektionen, Körpergeruch und sogar Fruchtbarkeitsproblemen bei Männern in Verbindung gebracht, was ihn zu einem breiteren Hygiene‑ und Gesundheitsproblem macht.
Einen Virus finden, der resistente Bakterien jagt
Um einen natürlichen Feind dieses Bakteriums zu finden, isolierten die Forschenden zunächst einen hartnäckigen, beta‑laktamresistenten S. saprophyticus‑Stamm aus stinkenden Socken. Anschließend screenten sie Abwasserproben—eine ergiebige Quelle bakterieller Viren—und identifizierten einen Phagen, den sie ØPh_SS01 nannten und der diesen Stamm spezifisch angreift. Unter dem Elektronenmikroskop zeigte der Phage eine klassische Kopf‑Schwanz‑Struktur, wie sie für viele Bakterienviren typisch ist. Labortests ergaben, dass ØPh_SS01 auch mehrere verwandte Staphylokokkenarten und eine Bacillus‑Art infizieren kann, was ihm eine mäßig breite Wirtsreichweite verleiht, die nützlich sein könnte, um mehrere problematische Haut‑ und Umweltbakterien zu bekämpfen, während er dennoch wesentlich gezielter ist als Standardantibiotika.
Ein robuster und wirksamer Bakterienkiller
ØPh_SS01 erwies sich als überraschend widerstandsfähig. Er blieb über einen weiten pH‑Bereich, bei Temperaturen von Kühlschrankkälte bis Körpertemperatur und bei hohen Salzkonzentrationen aktiv und tolerierte organische Lösungsmittelbehandlungen, die zu seiner Reinigung eingesetzt wurden. In Flüssigkultur führte die Zugabe des Phagen zu S. saprophyticus innerhalb von 24 Stunden zu einem Rückgang der Bakterienzahl um etwa sieben Log‑Stufen (zehn Millionen‑fach). Er war auch wirksam beim Verhindern und Auflösen von Biofilmen: bei hoher Phagendosis verhinderte er etwa drei Viertel der Biofilmbildung und entfernte etwa zwei Drittel bereits gebildeter Biofilme. Tests an menschlichen, hautähnlichen Zellen und blasenabgeleiteten Zellen zeigten, dass der Phage für Säugerzellen keine spürbaren Schäden verursachte, was seine Sicherheit für eine potenzielle Anwendung auf oder im Körper unterstützt.
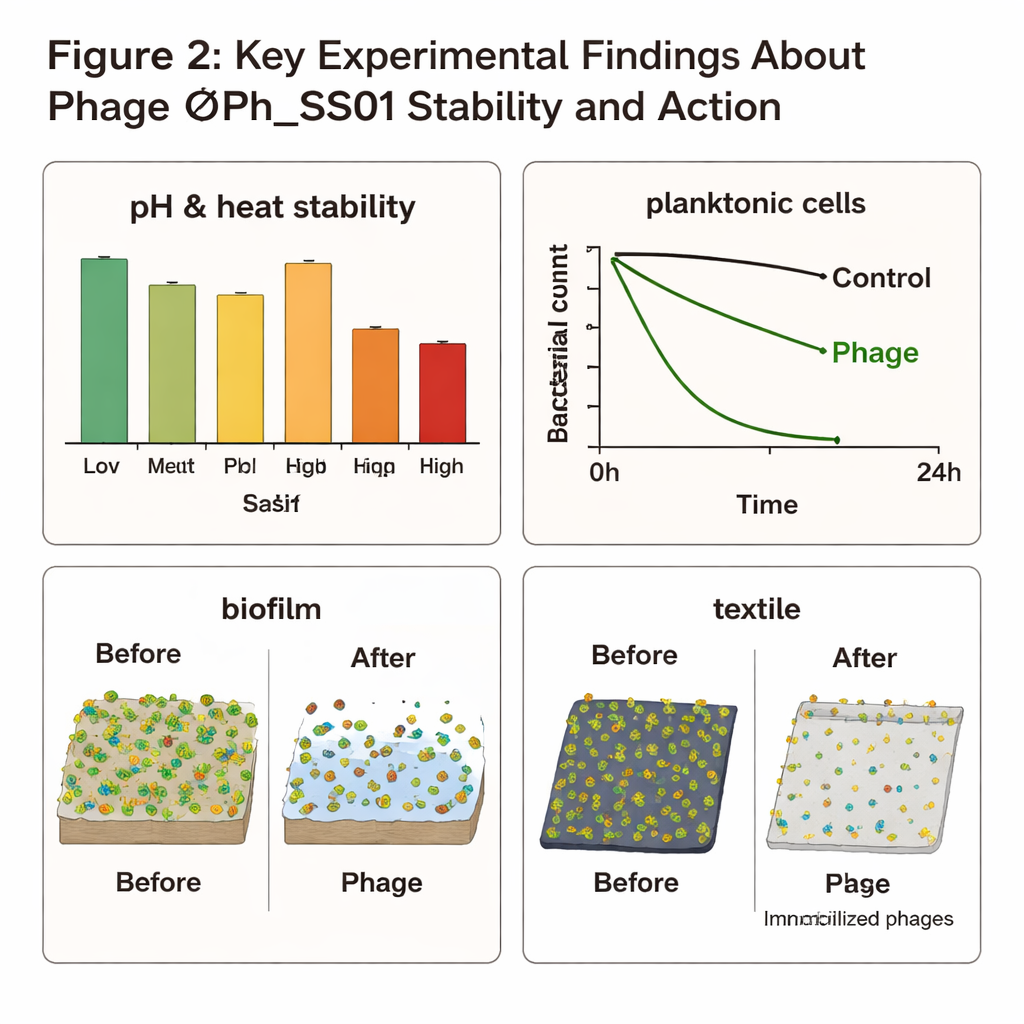
Vom Labortisch zu Textilien und Hygieneprodukten
Das Team untersuchte außerdem, wie dieser Phage in realen Umgebungen eingesetzt werden könnte. Wenn ØPh_SS01 auf Baumwollstücke immobilisiert und anschließend S. saprophyticus ausgesetzt wurde, sank die Zahl lebender Bakterien auf dem Gewebe im Verlauf um ungefähr sieben Größenordnungen, und in vielen Proben wurden die Bakterien nicht mehr nachgewiesen. Dieser Proof‑of‑Concept legt nahe, dass phagenbeschichtete Materialien—wie Socken, Unterwäsche, Damenbinden oder Wundauflagen—die Bakterienlast und damit verbundenen Geruch oder Infektionsrisiken aktiv reduzieren könnten, statt lediglich Feuchtigkeit zu binden. Die Genomanalyse zeigte, dass ØPh_SS01 ein zuvor unbeschriebenes Mitglied der Klasse Caudoviricetes mit einem 47‑Kilobasen‑dsDNA‑Genom ist und Gene trägt, die mit einem temperenten Lebensstil vereinbar sind, also der Phage die Bakterien entweder unmittelbar zerstören oder sich still in deren DNA integrieren kann.
Was das für die Gesundheit im Alltag bedeutet
Für Nichtfachleute lautet die Kernbotschaft: Sorgfältig ausgewählte „gute“ Viren können als Präzisionswerkzeuge gegen „schlechte“ Bakterien eingesetzt werden, die auf gängige Antibiotika nicht mehr ansprechen. Dieser neue Phage, ØPh_SS01, kann in Labortests eine UVI‑assoziierte, medikamentenresistente Bakterie dramatisch reduzieren, ihre Biofilme angreifen und gebunden an Textilien funktionieren, ohne menschliche Zellen zu schädigen. Obwohl weitere Arbeiten erforderlich sind, um einen temperenten Phagen in eine rein bakterienabtötende Therapie umzuwandeln und ihn an Tieren und Menschen zu testen, deutet die Studie auf zukünftige Seifen, Sprays, Verbände und Kleidung hin, die aktiv selbstdesinfizierend sind—und so helfen könnten, Infektionen zu verhindern und unsere Abhängigkeit von zunehmend unzuverlässigen Antibiotika zu verringern.
Zitation: Gopika, O., Sarat, N., Manikandan, M. et al. Isolation, characterisation and potential applications of a novel bacteriophage targeting beta-lactam-resistant Staphylococcus saprophyticus. Sci Rep 16, 7460 (2026). https://doi.org/10.1038/s41598-026-35899-3
Schlüsselwörter: Harnwegsinfektionen, Bakteriophagen‑Therapie, Staphylococcus saprophyticus, Antibiotikaresistenz, Biofilmkontrolle