Clear Sky Science · de
Lanthanid–Carbamazepin‑Komplexe: Synthese, spektroskopische Charakterisierung, DFT‑Einblicke, molekulares Docking und biologische Bewertung
Warum dieses Epilepsiemedikament ein High‑Tech‑Makeover bekommt
Carbamazepin ist ein seit langem eingesetztes Medikament zur Behandlung von Epilepsie und affektiven Störungen, hat aber Grenzen: Es löst sich schlecht in Wasser, kann als Schadstoff in Flüssen verbleiben und wurde nicht mit Blick auf moderne Krebstherapien oder Antiinfektionsstrategien entwickelt. In dieser Studie gaben Forscher dem Carbamazepin ein chemisches „Upgrade“, indem sie es an spezielle Metalle — die Lanthaniden — banden und dann prüften, ob diese neuen Verbindungen als potente, gezielte Wirkstoffe gegen Mikroben und Krebszellen fungieren können.
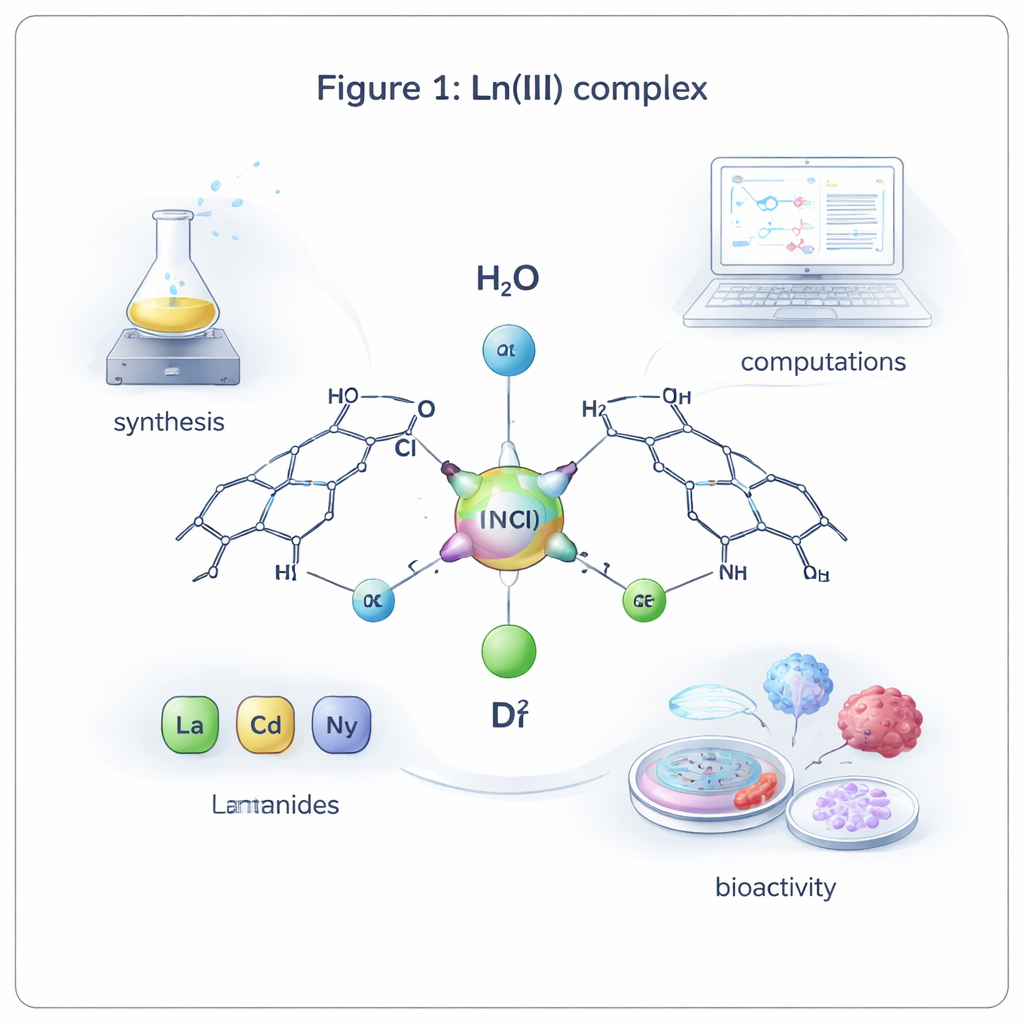
Neue Moleküle aus einer bekannten Tablette aufbauen
Das Team konzentrierte sich auf vier Lanthanidmetalle — Lanthan, Cer, Neodym und Dysprosium — ausgewählt wegen ihrer nützlichen magnetischen und optischen Eigenschaften und ihres wachsenden medizinischen Einsatzpotenzials. Sie reagierten jedes Metall mit Carbamazepin in einer warmen Alkohol‑Lösung und bildeten vier eng verwandte Metall‑Wirkstoff‑Komplexe im Verhältnis 1:2 (ein Metallion gebunden an zwei Carbamazepin‑Moleküle). Sorgfältige Laboruntersuchungen zeigten, dass jeder Komplex eine ähnliche Gesamtformel besitzt und sich als Elektrolyt verhält, was bedeutet, dass sich Teile des Moleküls in Lösung in geladene Bestandteile aufspalten können — eine Eigenschaft, die beeinflusst, wie es sich im Körper verteilt.
Blick auf Form und Struktur
Um zu verstehen, was sie hergestellt hatten, nutzten die Wissenschaftler ein Bündel spektroskopischer und struktureller Methoden, darunter Infrarot‑ und Kernspinresonanzspektroskopie, Röntgenbeugung und thermische Analyse. Diese Tests ergaben ein einheitliches Bild: In den neuen Verbindungen bindet Carbamazepin das Metall über zwei Atome seiner Amidgruppe — ein Stickstoff und ein Sauerstoff — sodass jedes Metall von sechs Partnern in einer leicht verzerrten oktaedrischen Anordnung umgeben ist. Rechnerische Methoden auf Basis der Dichtefunktionaltheorie bestätigten diese Geometrie und zeigten, dass sich die elektronischen Eigenschaften von Carbamazepin nach der Metallbindung so verändern, dass die Komplexe reaktiver und stabiler als das freie Arzneimittel sein können — eine vielversprechende Kombination für den medizinischen Einsatz.
Von Reagenzgläsern zu Mikroben und Krebszellen
Die nächste Frage war biologisch: Bewirken diese designten Moleküle überhaupt etwas Nützliches in lebenden Zellen? In Petrischalenversuchen wurden die Komplexe gegen mehrere krankheitserregende Bakterien und Pilze getestet. Das reine Carbamazepin zeigte kaum bis keine Wirkung, doch alle vier Metallkomplexe hemmten zumindest einige Mikroben, wobei die Lanthan‑Variante die größten klaren „Hemmzonen“ erzeugte und in einem Fall sogar mit oder besser als ein standardmäßiges Antimykotikum gegen einen Pilz konkurrierte. Die Forscher setzten anschließend menschliche Leber‑ (Hep‑G2) und Brust‑ (MCF‑7) Krebszelllinien derselben Verbindungen aus. Auch hier übertrafen die Metall‑Wirkstoff‑Komplexe das alleinige Carbamazepin und schädigten oder töteten Krebszellen bei weit niedrigeren Konzentrationen. Unter ihnen stach der Lanthan‑Komplex hervor, zeigte die stärkste Tumorzelltoxizität und blieb dabei in einem Bereich, der mit einem weit verbreiteten Chemotherapeutikum vergleichbar ist.
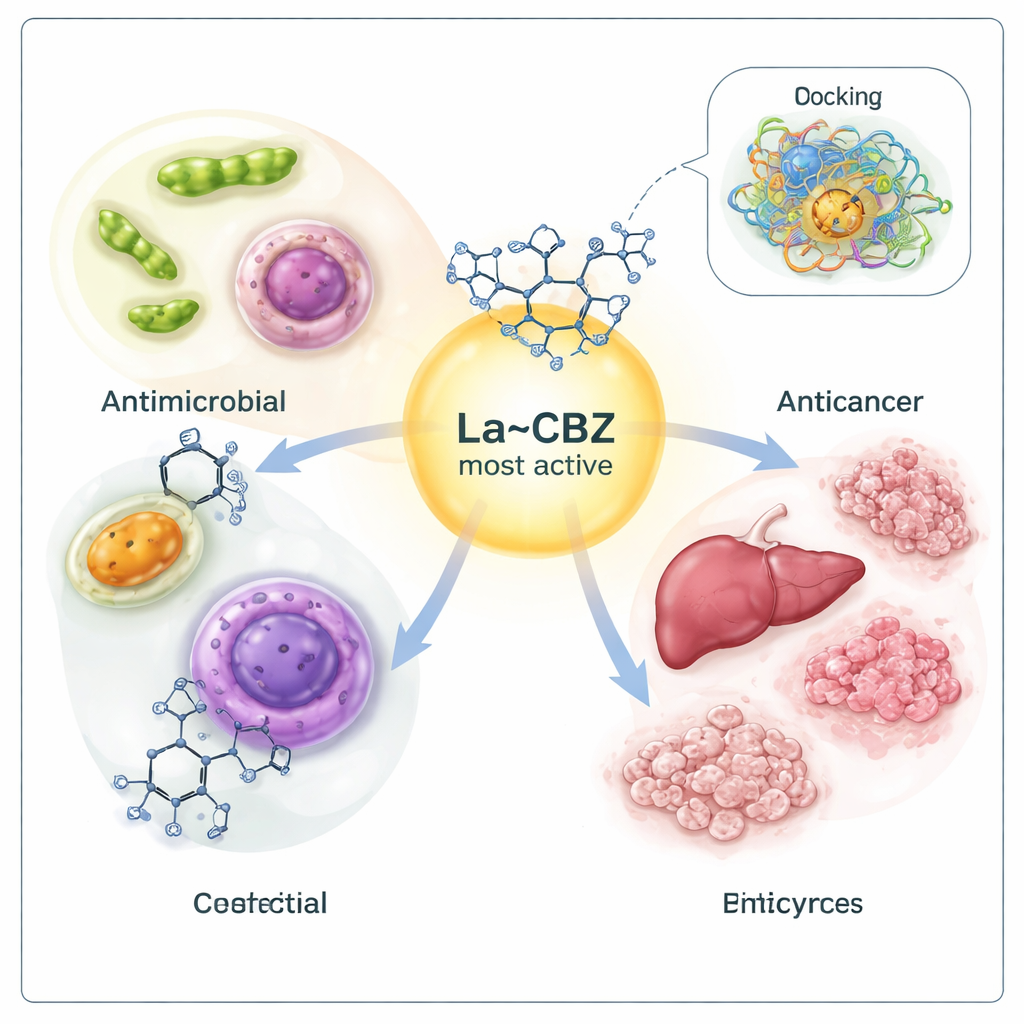
Wie die Moleküle an Krankheitsziele andocken könnten
Um zu untersuchen, warum der Lanthan‑Komplex so potent war, griff das Team zu molekularen Docking‑Simulationen — Computermodelle, die zeigen, wie ein kleines Molekül in die Taschen eines Proteins passen könnte. Sie untersuchten bakterielle Proteine und Schlüsselenzyme, die mit Leber‑ und Brustkrebs in Verbindung stehen. Die Simulationen deuteten darauf hin, dass der Lanthan‑Carbamazepin‑Komplex am besten in diese Proteinbindungsstellen passt und starke Wechselwirkungen eingeht, die die normale Funktion stören könnten. Energiebetrachtungen zeigten, dass niedrigere (negativere) Dockingenergien auf stärkere Bindung hindeuten, und der Lanthan‑Komplex lieferte konsequent die günstigsten Werte — im Einklang mit seiner überlegenen Leistung in den Laborversuchen.
Was das für zukünftige Medikamente bedeuten könnte
Insgesamt zeigt diese Arbeit, dass ein bekanntes Epilepsiemedikament in eine neue Klasse metallbasierter Verbindungen mit vielversprechendem antimikrobiellem und antitumoralem Verhalten verwandelt werden kann. Durch das Umgestalten von Carbamazepin um Lanthanidzentren schufen die Forscher stabile, kristalline Komplexe, die stärker mit biologischen Zielen interagieren als das Ausgangsmedikament. Obwohl diese Befunde noch in einem frühen präklinischen Stadium sind, weisen sie auf die Möglichkeit hin, solche Metall‑Wirkstoff‑Hybride künftig als Chemotherapie‑ oder Antiinfektionsmittel einzusetzen — und möglicherweise auch als Bildgebungs‑ oder Transportmittel, das die einzigartigen optischen und magnetischen Eigenschaften der Lanthanide nutzt.
Zitation: Mohamed, N.S., Mohamed, M.M.A., Shehata, M.R. et al. Lanthanide–carbamazepine complexes: synthesis, spectroscopic characterization, DFT Insights, molecular docking, and biological evaluation. Sci Rep 16, 6340 (2026). https://doi.org/10.1038/s41598-026-35893-9
Schlüsselwörter: Carbamazepin, Lanthanid‑Komplexe, metallbasierte Arzneimittel, Antikrebsmittel, antimikrobielle Aktivität